





高中第五章 化工生产中的重要非金属元素第一节 硫及其化合物课堂教学课件ppt
展开
这是一份高中第五章 化工生产中的重要非金属元素第一节 硫及其化合物课堂教学课件ppt,共34页。PPT课件主要包含了知识点一,Ag+,知识点二,火山口附近,地壳的岩层中,硫化物和硫酸盐,H2SO3,H2SO4,SO2,BaSO3等内容,欢迎下载使用。
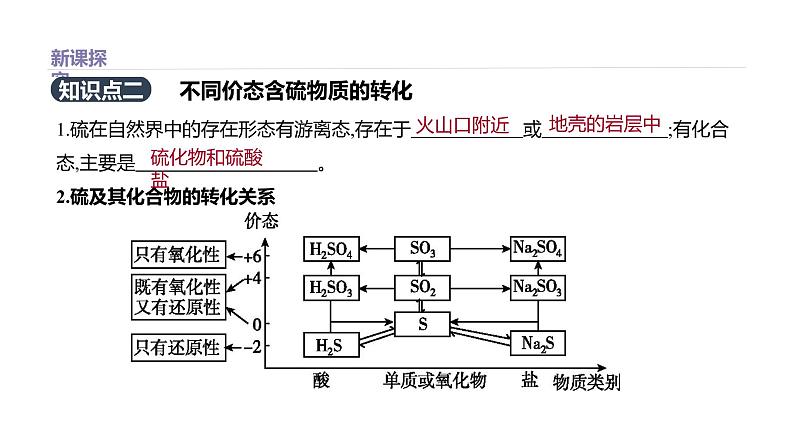
1.硫在自然界中的存在形态有游离态,存在于 或 ;有化合态,主要是 。 2.硫及其化合物的转化关系
不同价态含硫物质的转化
[素养养成] 1.怎样实现相同或不相同价态的含硫物质间的转化?
[答案]提示:不同价态的含硫物质间通过氧化还原反应规律来转化,相同价态的含硫物质间通过非氧化还原反应规律来转化。
2.能不能用浓硫酸来干燥二氧化硫气体?
[答案]提示:可以;虽然浓硫酸具有强氧化性,二氧化硫具有还原性,但两者之间不能发生氧化还原反应。
例3 硫黄在空气中燃烧生成气体甲,甲溶于水得溶液乙,向乙溶液中滴加溴水,溴水褪色,乙变成丙。在丙里加入Na2S生成气体丁,把丁通入乙得到沉淀戊。甲、乙、丙、丁、戊均含有硫元素,则它们正确的顺序是 ( )A.SO3 H2SO4 H2SO3 H2S S B.SO2 H2SO3 H2SO4 SO2 SO3C.SO3 H2SO4 H2SO3 SO2 Na2S2O3 D.SO2 H2SO3 H2SO4 H2S S
[解析] 硫黄在空气中燃烧生成SO2(甲),SO2溶于水得溶液H2SO3(乙),向乙溶液中滴加溴水生成H2SO4(丙)和HBr,在丙里加入Na2S生成气体H2S(丁),把H2S通入H2SO3中得到沉淀S(戊)。
[解析] Cu与浓硫酸反应时,Cu单质被氧化为硫酸铜,浓硫酸表现了氧化性,作氧化剂,A正确;SO2与NaOH反应产生亚硫酸钠和水,表明SO2有酸性氧化物的性质,B正确;S+Na2SO3=Na2S2O3,反应物全部变为生成物,原子利用率是100%,C正确;Na2S2O3与稀硫酸发生复分解反应,
产生硫代硫酸和硫酸钠,硫代硫酸不稳定,分解产生S单质、二氧化硫和水,所以硫酸起酸的作用,不是作还原剂,D错误。
[归纳总结] 含硫物质的连续氧化硫元素
[解析] A项,元素化合价没有发生变化,不是氧化还原反应,加入酸就能实现,故A项错误;B项,Cl元素化合价升高,被氧化,应加入氧化剂才能实现,故B项错误;C项,Na元素化合价升高,被氧化,应加入氧化剂,故C项错误;D项,S元素化合价降低,被还原,应加入还原剂才能实现,故D项正确。
2.不能通过一步反应实现的是 ( )A.H2S SO2 B.S SO3 C.SO2 H2SO4 D.H2SO4(浓) SO2
[解析] 硫化氢与足量氧气反应生成二氧化硫,故A正确;硫与氧气反应只能生成二氧化硫,SO2在催化剂加热条件下生成三氧化硫,故B错误;SO2被溴水氧化成硫酸,故C正确;浓硫酸具有强氧化性,与碳反应生成二氧化硫,故D正确。
4.如图所示是一系列含硫化合物的转化关系(部分反应产物已略去),下列说法正确的是( )A.反应①说明SO2具有漂白性,反应②说明SO2具有酸性B.若反应②中生成物n(Na2SO3)∶n(NaHSO3)=1∶1,则反应物n(SO2)∶n(NaOH)=1∶2C.反应③④⑤均属于氧化还原反应D.工业上可利用反应②和反应④回收SO2
[解析] 反应①中溶液先变蓝后褪色的原因是KIO3被还原先得到I2,最终得到I-,体现了SO2的还原性,反应②是酸性氧化物和碱的反应,体现了SO2的酸性氧化物的性质,故A错误;根据原子守恒,当n(Na2SO3)∶n(NaHSO3)=1∶1时,n(SO2)∶n(NaOH)=2∶3,故B错误;反应④中没有元素化合价的变化,所以反应④是非氧化还原反应,故C错误;反应②吸收了二氧化硫,SO2与NaOH反应生成NaHSO3,NaHSO3分解又得到SO2,所以工业上可利用反应②和反应④回收SO2,故D正确。
5.如图表示物质A~F之间的转化关系,其中A为淡黄色固体物质,B、C为无色溶液,D为气体,E、F为白色沉淀。请填写下列各空:(1)写出各物质的化学式:A为 ,B为 ,C为 ,D为 ,E为 ,F为 。
[解析] A为淡黄色固体,由转化关系可知,A为S,则D为SO2,与水反应生成的B为H2SO3,H2SO3具有还原性,可与氯气发生氧化还原反应,则C为H2SO4,B和氢氧化钡反应生成E,E为BaSO3,F为BaSO4。(1)根据以上分析可知,A为S,B为H2SO3,C为H2SO4,D为SO2,E为BaSO3,F为BaSO4。
5.如图表示物质A~F之间的转化关系,其中A为淡黄色固体物质,B、C为无色溶液,D为气体,E、F为白色沉淀。请填写下列各空:(2)写出下列反应的化学方程式:B→A: 。 B→C: 。 (3)写出C→F的离子方程式: 。
H2SO3+2H2S=3S↓+3H2O
H2SO3+Cl2+H2O=H2SO4+2HCl
5.如图表示物质A~F之间的转化关系,其中A为淡黄色固体物质,B、C为无色溶液,D为气体,E、F为白色沉淀。请填写下列各空:(4)在A~F六种物质中,既有氧化性又有还原性的是(填字母代号) 。
[解析]在A~F六种物质中,既有氧化性又有还原性,说明S元素的化合价既能升高,又能降低,S元素的化合价处于中间价态,有S、H2SO3、SO2、BaSO3。
1.某硫酸厂废气中SO2的回收利用方案如下图所示。下列说法错误的是 ( )A.X可能含有2种盐 B.Y可能含有(NH4)2SO4C.a是SO3 D.(NH4)2S2O8中S的化合价不可能为+7价
[解析] X可能含有亚硫酸铵、亚硫酸氢铵,A正确; X与过量硫酸反应生成硫酸铵和硫酸氢铵或硫酸氢铵,B正确; a应该是SO2,C错误;硫的最高价为+6价,不可能出现+7价,事实上H2S2O8的结构为
含有过氧键(—O—O—),过氧键中O的化合价为-1价;根据化合物中各元素的正、负化合价的代数和为0可知(NH4)2S2O8中S的化合价为+6价,D正确。
2.有一瓶Na2SO3溶液,可能已部分氧化,某学生进行如下实验:取少量溶液,滴入Ba(NO3)2溶液产生白色沉淀,再加入过量稀硝酸,充分振荡后仍有白色沉淀,结论正确的是( )A.Na2SO3溶液已部分氧化B.加入Ba(NO3)2溶液后生成的沉淀中一定含有BaSO4C.加硝酸后的不溶沉淀一定为BaSO4D.此实验能确定Na2SO3溶液是否部分氧化
[解析] 硝酸能将+4价的S氧化为+6价,加硝酸后的不溶沉淀一定为BaSO4,但加硝酸前的不溶沉淀可能为BaSO3或BaSO4或它们的混合物,所以该实验不能确定Na2SO3是否部分氧化。
4.如图甲是“碱法烟气脱硫法”示意图,如图乙是工业上“石灰-石膏烟气脱硫法”示意图,回答:已知: (1)图甲中,反应①的离子方程式为 ,该法的缺点之一是 。
(2)图乙中,反应⑤的目的是稳定固化硫元素形成高价态的化合物,氧气的作用是 ;该法的优点之一是 。
[解析]亚硫酸钙能被氧气氧化生成硫酸钙,氧气的作用是作氧化剂,石灰-石膏法所用原料易得、成本低,所以该法的优点之一是成本低。
相关课件
这是一份人教版 (2019)必修 第二册第五章 化工生产中的重要非金属元素第一节 硫及其化合物教学演示ppt课件,共26页。
这是一份高中人教版 (2019)第一节 硫及其化合物背景图课件ppt,共60页。PPT课件主要包含了课前自主学习,硫的物理性质,CS2,淡蓝色,蓝紫色,氧化性,还原性,刺激性气味,易溶于水,同一条件等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第二册第五章 化工生产中的重要非金属元素第一节 硫及其化合物教案配套课件ppt,共55页。PPT课件主要包含了硫1物理性质,必备知识·自主学习,刺激性,试管中液面上升,SO2易溶于水,溶液颜色变红色,SO2的水溶液显,振荡后溶液红色,褪去再加热溶液,又恢复红色等内容,欢迎下载使用。










