



- 鲁教版化学九年级下册 第八单元 海水中的化学 第二节 海水“晒盐” 第1课时 海水“晒盐”的过程【课件+素材】 课件 15 次下载
- 鲁教版化学九年级下册 第八单元 海水中的化学 第二节 海水“晒盐” 第2课时 溶解度【课件+素材】 课件 14 次下载
- 鲁教版化学九年级下册 第八单元 海水中的化学 第三节 海水“制碱” 第1课时 氨碱法制纯碱 纯碱的性质【课件+素材】 课件 15 次下载
- 鲁教版化学九年级下册 第八单元 海水中的化学 第三节 海水“制碱” 第2课时 盐的化学性质 复分解反应的实质【课件+素材】 课件 13 次下载
- 鲁教版化学九年级下册 第九单元 金属 第一节 常见的金属材料 第1课时 金属的物理性质 合金【课件+素材】 课件 13 次下载
化学九年级下册第二节 海水“晒盐“图片ppt课件
展开海水“晒盐”得到的粗盐,往往含有可溶性杂质(如氯化镁、氯化钙等)和不溶性杂质(如泥沙等),必须对其进行分离和提纯,才能用于工业生产和人们的日常生活。
这时得到的氯化钠晶体中仍含有较多的可溶性杂质,工业上是利用化学方法除去这些可溶性杂质。
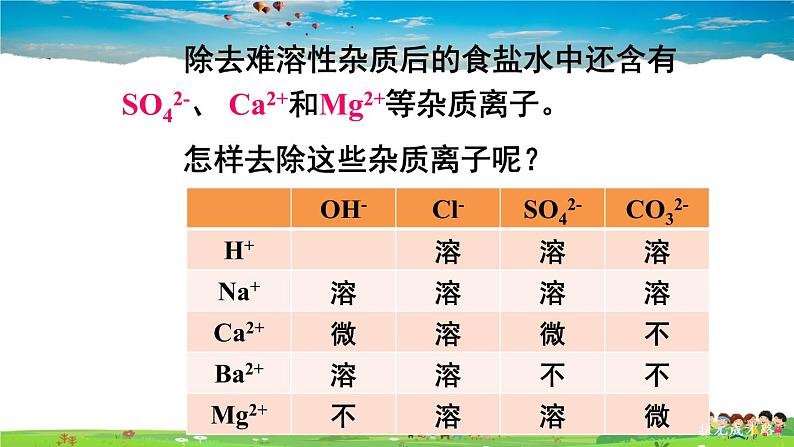
除去难溶性杂质后的食盐水中还含有SO42-、 Ca2+和Mg2+等杂质离子。
怎样去除这些杂质离子呢?
选择试剂时应注意哪些问题?
为了将杂质除尽,所加试剂应该过量
过量的试剂在后续实验中必须除去
一般将杂质离子转换为沉淀、气体或水而除去
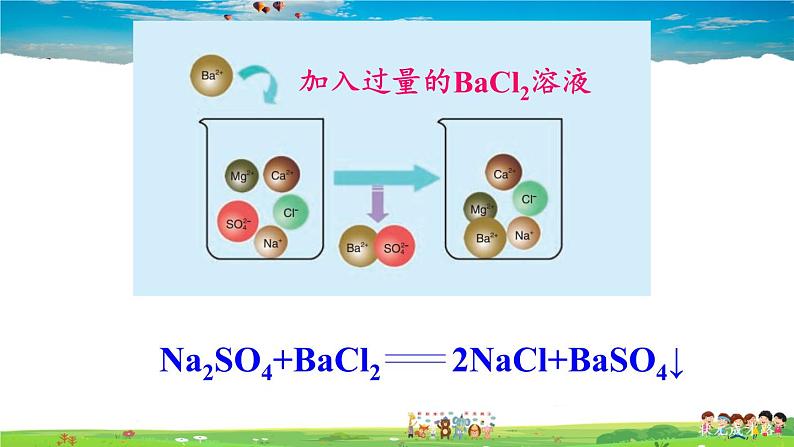
加入过量的BaCl2溶液
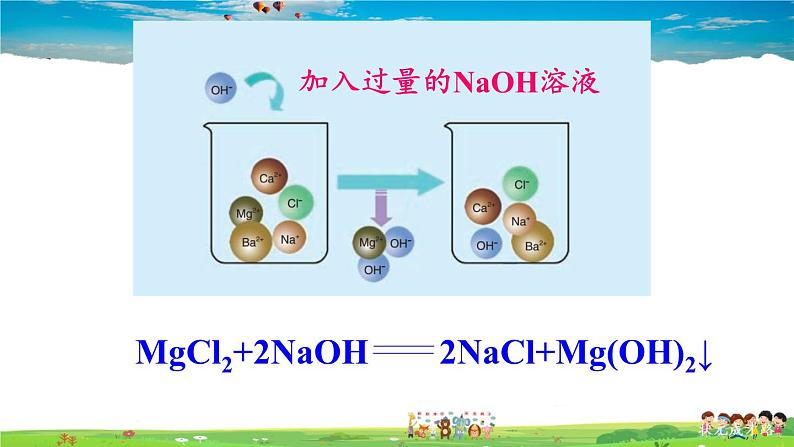
加入过量的NaOH溶液
加入过量的Na2CO3溶液
过滤除沉淀后加入适量的盐酸
Na2CO3 +2HCl 2NaCl+H2O+CO2↑
NaOH +HCl NaCl+H2O
我们所选用的除杂试剂的加入顺序可以变动吗?
Na2CO3 要除去Ca2+和Ba2+,所以Na2CO3要在BaCl2之后加入,盐酸要除去CO32-,最后加入。所以顺序可以是
食盐是人体进行正常新陈代谢的必需品,是重要的调味品和食品添加剂。食盐还是制造烧碱、氯气、盐酸和纯碱等的基本原料。
1.为了除去粗盐中的CaCl2、MgSO4及泥沙,可将粗盐溶于水,然后进行下列5项操作:①过滤;②加过量的NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量的BaCl2溶液.正确的操作顺序是( )
A. ①④②⑤③ B. ④①②⑤③ C. ②⑤④①③ D. ⑤③②④①
2.氯化钠溶液中含有杂质CaCl2、MgCl2、Na2SO4,依次通过下列操作获得纯净的氯化钠:①加过量的NaOH溶液;②加过量的BaCl2溶液;③加过量的Na2CO3溶液;④过滤;⑤加适量的盐酸至溶液呈中性;⑥蒸干溶液中水分得到氯化钠晶体.下列有关分析错误的是( )
A. ①中NaOH溶液用于除去MgCl2B. ③中Na2CO3溶液用于除去CaCl2和BaCl2C. ①②的除杂顺序可以颠倒D. ①②③的除杂顺序可以颠倒
3.通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
(1)除去粗盐中不溶性杂质的操作步骤是____。 (2)第⑥步操作的目的是除去滤液中过量的________。写出反应的方程式:____________________________。 (3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、_______________(填化学式) (4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是_______________________________。 (5)若操作②和操作④的顺序颠倒,则最后所得的精盐中还含有__________(填化学式)
BaCO3、CaCO3
用KOH会有新的杂离子K+产生
粗盐中难溶性杂质的去除
粗盐中可溶性杂质的去除
初中化学鲁教版九年级下册第二节 海水“晒盐“习题ppt课件: 这是一份初中化学鲁教版九年级下册第二节 海水“晒盐“习题ppt课件,共10页。PPT课件主要包含了蒸发结晶,适量的盐酸,沉淀物,碳酸钠,NaOH,Na2CO3等内容,欢迎下载使用。
九年级下册第二节 海水“晒盐“习题ppt课件: 这是一份九年级下册第二节 海水“晒盐“习题ppt课件,共21页。PPT课件主要包含了饱和溶液,蒸发池,结晶池,这种溶剂,KNO3,NaCl,CaOH2,一定压强,一定温度,逐渐增大等内容,欢迎下载使用。
2021学年第二节 海水“晒盐“备课ppt课件: 这是一份2021学年第二节 海水“晒盐“备课ppt课件,共24页。PPT课件主要包含了动动手,海水晒盐,蒸发池,结晶池,--蒸发结晶法,实验过程,粗盐提纯,实验室提纯,玻璃棒,操作要点等内容,欢迎下载使用。













