






所属成套资源:鲁教版化学九年级下册PPT课件
- 鲁教版化学九年级下册 第八单元 海水中的化学 第二节 海水“晒盐” 第2课时 溶解度【课件+素材】 课件 15 次下载
- 鲁教版化学九年级下册 第八单元 海水中的化学 第二节 海水“晒盐” 第3课时 粗盐的提纯【课件+素材】 课件 15 次下载
- 鲁教版化学九年级下册 第八单元 海水中的化学 第三节 海水“制碱” 第2课时 盐的化学性质 复分解反应的实质【课件+素材】 课件 14 次下载
- 鲁教版化学九年级下册 第九单元 金属 第一节 常见的金属材料 第1课时 金属的物理性质 合金【课件+素材】 课件 13 次下载
- 鲁教版化学九年级下册 第九单元 金属 第一节 常见的金属材料 第2课时 金属矿物及其冶炼【课件+素材】 课件 13 次下载
初中鲁教版第八单元 海水中的化学第三节 海水“制碱“课文课件ppt
展开
这是一份初中鲁教版第八单元 海水中的化学第三节 海水“制碱“课文课件ppt,文件包含第八单元海水中的化学第三节海水“制碱”第1课时氨碱法制纯碱纯碱的性质第1课时氨碱法制纯碱纯碱的性质ppt、碳酸钠碳酸氢钠分别与稀盐酸的反应wmv、碳酸钠溶液与澄清石灰水反应wmv等3份课件配套教学资源,其中PPT共38页, 欢迎下载使用。
纯碱或苏打(主要成分为碳酸钠)是以食盐、石灰石为原料,以氨为媒介,采用氨碱法制得的。
由NaCl转变为Na2CO3,物质的元素组成发生了什么变化?用NaCl制Na2CO3,还需要什么原料?
制取物质时要遵循的几条原则 原料来源是否丰富、易得?价格是否低廉?工艺流程及设备是否简单?生产过程是否安全?是否会造成环境污染?
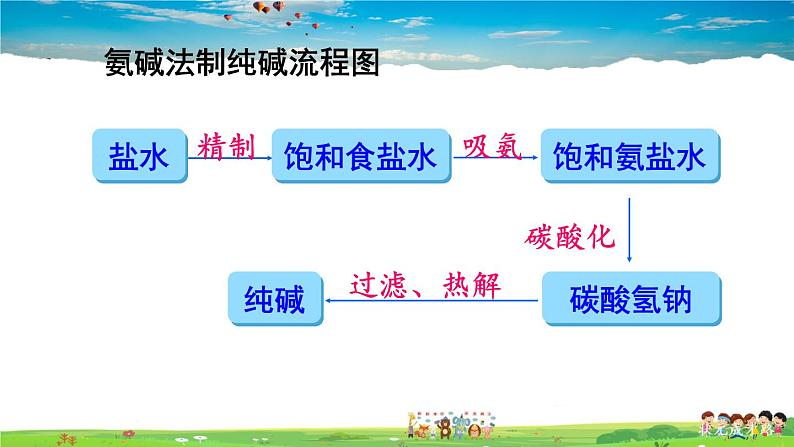
工业上采用氨碱法生产纯碱,是先向饱和食盐水中通入氨气,制成饱和氨盐水,在加压并不断通入二氧化碳的条件下使碳酸氢钠(NaHCO3)结晶析出,过滤后,将碳酸氢钠加热分解即得纯碱。
上述过程的化学反应原理为:
1.在用氨碱法生产纯碱的过程中,为什么要先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通入二氧化碳?
氨溶于水后生成氨水显碱性,促进CO2的吸收。
2. 氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵,哪种物质首先结晶析出?为什么?
相同温度下NaHCO3比NH4Cl溶解度小,所以NaHCO3先析出。
分析氨碱法的优点和不足之处
CO2和NH3可回收利用
回收氨时产生的大量CaCl2用处不大,且污染环境
1926年,我国化学家侯德榜在氨碱法的基础上,创立了更为先进的联合制碱法(侯氏制碱法)。
侯德榜(1890-1974)
向滤出NaHCO3晶体后的NH4Cl溶液中加入食盐,使其中的NH4Cl单独结晶析出,用作氮肥, NaCl溶液则可循环使用。
侯氏制碱法保留了氨碱法的优点,克服了其缺点,打破了当时西方国家对制碱技术的垄断,促进了世界制碱技术的发展。
纯碱在通常情况下为______粉末,____溶于水,水溶液显____性。
纯碱在工业生产中用途极广,如石油精炼、粗盐精制、硬水软化、人造纤维及玻璃生产等均需大量的纯碱。纯碱还广泛应用于冶金、造纸、纺织印染和洗涤剂生产等领域。
碳酸氢钠俗称________,又称酸式碳酸钠,通常是______粉末状晶体,____溶于水,受热____分解。
在灭火器里,它是二氧化碳发生剂;在食品工业上,它是发酵粉的主要成分;在制造饮料时,它是一种常用原料;在医疗上,它是治疗胃酸过多的药剂之一 。
灭火器、制饮料、发酵粉、治疗胃酸
石油精炼、洗涤剂、制造玻璃等。
取少量碳酸钠固体,加入试管中,加少量蒸馏水后振荡,观察其溶解情况。再滴入2~3滴酚酞试液,观察现象。
现象:_____________________
结论:碳酸钠______溶于水,溶液显______性。
取少量碳酸钠固体,加入试管中,然后滴加稀盐酸,观察现象。迅速将燃着的木条伸进试管口,观察现象 。
化学方程式:__________________________
若用稀硫酸代替稀盐酸进行实验,现象是否相同?
碳酸钠、碳酸氢钠与稀盐酸的反应
向盛有少量碳酸钠溶液的试管中滴加澄清石灰水,观察现象。
碳酸钠与氢氧化钙的反应
向盛有少量碳酸钠溶液的试管中滴加氯化钡溶液,观察现象。
1.“侯氏制碱法”的生产过程涉及的主要化学反应如下:
请回答:(1)反应①中X的化学式为________。(2)NH4Cl中N元素的化合价为________。(3)除去混在Na2CO3粉末中少量的NaHCO3的方法是______________________________。
加热Na2CO3和NaHCO3的混合物
2.工业上采用氨碱法生产纯碱的工艺是先向饱和食盐水中通入较多NH3(溶液显碱性),再通入足量的CO2的原因是( ) A.使CO2更易被吸收 B.NH3比CO2更易制取 C.CO2的密度比NH3大 D.为了增大NaHCO3的溶解度
3.下列说法正确的是( ) A.制纯碱需要的原料有食盐和石灰石 B.海水晒得的粗盐可以直接吸氨制成氨盐水 C.向氨盐水中通入CO2可得到纯碱,溶液经结晶后得到纯碱固体 D.因为氯化钠水溶液呈中性,所以氨盐水也呈中性
4.图1是“△△牌发酵粉”的部分信息,课外化学兴趣小组的同学对其进行了如下探究(请你完成相应填空):
△△牌发酵粉【主要成分】NaHCO3、酒石酸【用途】面粉发酵,焙制糕点【用法】取本品适量加水溶解与面团揉和或直接与面团揉和后加热
【查阅资料】(1)酒石酸是一种易溶于水的固 体有机酸;(2)发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致;(3)Na2CO3受热不分解。【提出问题】NaHCO3在发酵粉加水或加热时如何产生CO2?【假设猜想】甲:…… 乙:酒石酸与NaHCO3在溶液中反应产生 CO2。 丙:NaHCO3加热产生CO2。
【实验探究】(1)小明同学取少量NaHCO3粉末于试管中,加入适量水,无气体产生,从而否定了猜想甲,则猜想甲是________________________________。小明又将酒石酸溶液和NaHCO3溶液混合,产生了CO2,从而验证了猜想乙,说明了NaHCO3具有的性质之一是______________________。(2)小英同学为探究猜想丙设计了图2所示的实验装置:小英另取适量NaHCO3粉末加入a试管中,
NaHCO3和水反应产生二氧化碳
NaHCO3能与酸反应
加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊。b试管中反应的化学方程式为___________________________________________。持续加热直至两支试管均不再发生变化时,发现a试管中仍残留有较多白色固体粉末,向该粉末中滴加稀盐酸,有CO2产生,说明该粉末是______。【实验小结】NaHCO3在发酵粉中产生CO2的条件是_______;NaHCO3受热发生变化的化学方程式为__________________________________。
Ca(OH)2+CO2=CaCO3↓+H2O
相关课件
这是一份初中第三节 海水“制碱“习题课件ppt,共23页。PPT课件主要包含了饱和氨盐水,碳酸氢钠,石灰石,碳酸钠,氯化铵,指示剂,小苏打,酸式碳酸钠,粉末状晶,CaCO3等内容,欢迎下载使用。
这是一份化学3 海水“制碱”课文配套课件ppt,共18页。PPT课件主要包含了NaHCO3,小苏打,又称酸式碳酸钠,碳酸氢钠,Na2CO3,与酸碱指示剂作用,纯碱的性质,与酸反应,或碳酸氢根离子,与氯化钡的反应等内容,欢迎下载使用。
这是一份初中化学鲁教版九年级下册第三节 海水“制碱“多媒体教学ppt课件,共40页。PPT课件主要包含了难溶性,CuOH2,NaOH,复分解反应,H2SO4,BaCl2,NH4Cl,∶21,吸收空气中的二氧化碳等内容,欢迎下载使用。










