
人教版 (2019) 选择性必修1 第四章 章末复习方案学案
展开
这是一份人教版 (2019) 选择性必修1 第四章 章末复习方案学案,共7页。
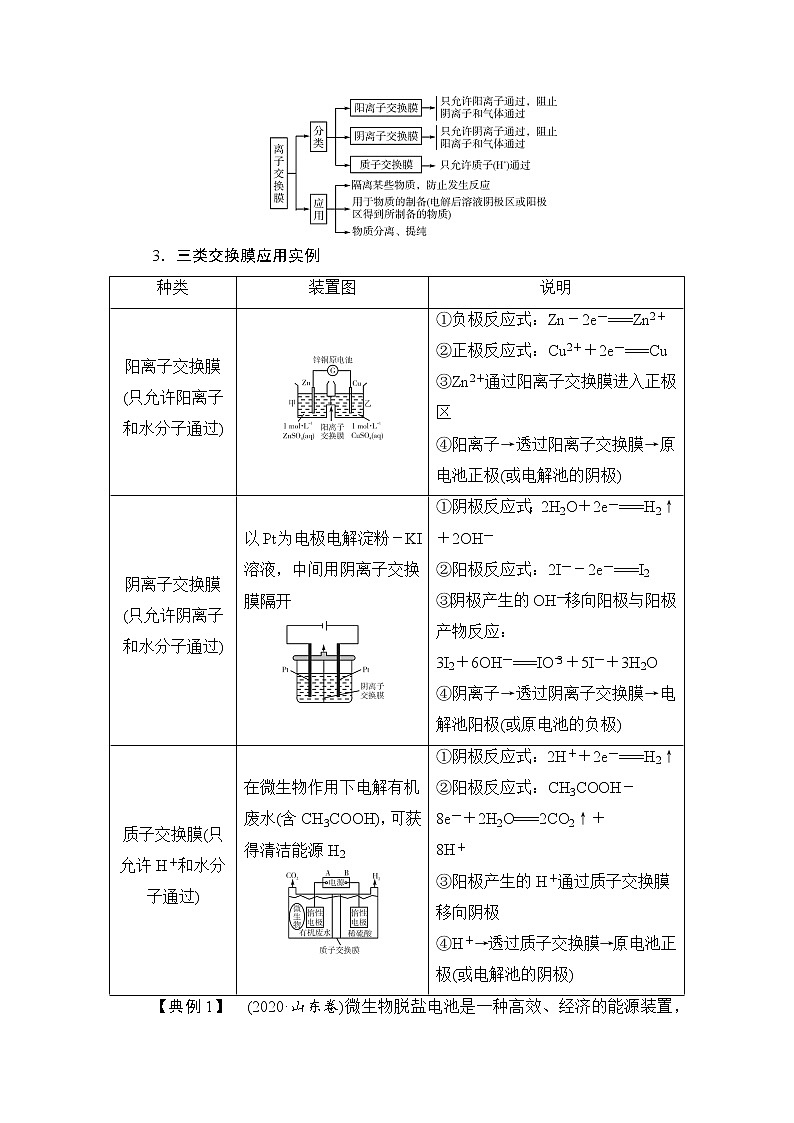
素能提升一 隔膜在电化学中的功能1.含义和作用(1)含义:离子交换膜又叫隔膜,由高分子特殊材料制成。(2)作用:①能将两极区隔离,阻止两极区产生的物质接触,防止发生化学反应;②能选择性地通过离子,起到平衡电荷、形成闭合回路的作用。2.分类和应用3.三类交换膜应用实例种类装置图说明阳离子交换膜(只允许阳离子和水分子通过)①负极反应式:Zn-2e-===Zn2+②正极反应式:Cu2++2e-===Cu③Zn2+通过阳离子交换膜进入正极区④阳离子→透过阳离子交换膜→原电池正极(或电解池的阴极)阴离子交换膜(只允许阴离子和水分子通过)以Pt为电极电解淀粉-KI溶液,中间用阴离子交换膜隔开①阴极反应式:2H2O+2e-===H2↑+2OH-②阳极反应式:2I--2e-===I2③阴极产生的OH-移向阳极与阳极产物反应:3I2+6OH-===IO+5I-+3H2O④阴离子→透过阴离子交换膜→电解池阳极(或原电池的负极)质子交换膜(只允许H+和水分子通过)在微生物作用下电解有机废水(含CH3COOH),可获得清洁能源H2①阴极反应式:2H++2e-===H2↑②阳极反应式:CH3COOH-8e-+2H2O===2CO2↑+8H+③阳极产生的H+通过质子交换膜移向阴极④H+→透过质子交换膜→原电池正极(或电解池的阴极)【典例1】 (2020·山东卷)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是( )A.负极反应为CH3COO-+2H2O-8e-===2CO2↑+7H+B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜C.当电路中转移1 mol电子时,模拟海水理论上除盐58.5 gD.电池工作一段时间后,正、负极产生气体的物质的量之比为2∶1答案 B解析 据图可知a极上CH3COO-转化为CO2和H+,C元素被氧化,所以a极为该原电池的负极,b极为正极。负极CH3COO-失电子被氧化成CO2和H+,结合电荷守恒可得电极反应式为 CH3COO-+2H2O-8e-===2CO2↑+7H+,A项正确;为了实现海水的淡化,模拟海水中的氯离子需要移向负极,即a极,则隔膜1为阴离子交换膜,钠离子需要移向正极,即b极,则隔膜2为阳离子交换膜,B项错误;当电路中转移 1 mol 电子时,根据电荷守恒可知,海水中会有 1 mol Cl-移向负极,同时有 1 mol Na+移向正极,即除去 1 mol NaCl,质量为 58.5 g,C项正确;b极为正极,水溶液为酸性,所以氢离子得电子产生氢气,电极反应式为2H++2e-===H2↑,则当转移 8 mol 电子时,正极产生4 mol气体,根据负极反应式可知负极产生 2 mol 气体,物质的量之比为4∶2=2∶1,D项正确。【变式1】 利用电解法制取Na2FeO4的装置图如图所示,下列说法正确的是(电解过程中温度保持不变,溶液体积变化忽略不计)( )A.Y是外接电源的正极,Fe电极上发生还原反应B.Ni电极上发生的电极反应为2H2O-4e-===O2↑+4H+C.若隔膜为阴离子交换膜,则电解过程中OH-由B室进入A室D.电解后,撤去隔膜,充分混合,电解液的pH比原来小答案 D解析 铁电极为阳极,Y接电源的正极,铁电极上发生失电子的氧化反应Fe+8OH--6e-===FeO+4H2O↑,A项错误;镍电极为阴极,X接电源的负极,镍电极上发生的反应为2H2O+2e-===H2↑+2OH-,B项错误;在电解池装置中,阴离子向阳极移动,OH-由A室进入B室,C项错误;总反应为2Fe+2OH-+2H2O===FeO+3H2↑,由于反应消耗OH-,电解的OH-浓度降低,pH比原来小,D项正确。素能提升二 多池串联的两大模型及原理分析1.有外接电源电池类型的判断方法有外接电源的各电池均为电解池,若电池阳极材料与电解质溶液中的阳离子相同,则该电池为电镀池。如:则甲为电镀池,乙、丙均为电解池。2.无外接电源电池类型的判断方法(1)直接判断非常直观明显的装置,如燃料电池、铅酸蓄电池等在电路中,则其他装置为电解池。如图所示:A为原电池,B为电解池;甲池为原电池,其余为电解池。(2)根据电池中的电极材料和电解质溶液判断原电池一般是两种不同的金属电极或一个金属电极一个碳棒电极;而电解池则一般两个都是惰性电极,如两个铂电极或两个碳棒电极。原电池中的电极材料和电解质溶液之间能发生自发的氧化还原反应,电解池的电极材料一般不能和电解质溶液自发反应。如图所示:B为原电池,A为电解池。(3)根据电极反应现象判断在某些装置中根据电极反应或反应现象可判断电极,并由此判断电池类型。如图所示:若C极溶解,D极上析出Cu,B极附近溶液变红,A极上放出黄绿色气体,则可知乙是原电池,D是正极,C是负极;甲是电解池,A是阳极,B是阴极。B、D极发生还原反应,A、C极发生氧化反应。3.“串联”类装置的解题流程【典例2】 假设图中原电池产生的电压、电流强度均能满足电解、电镀要求,即为理想化。①~⑧为各装置中的电极编号。下列说法错误的是( )A.当K闭合时,甲装置在电路中作电源B.当K断开时,乙装置锌片溶解,有氢气产生C.当K闭合后,整个电路中电子的流动方向为③→②、①→⑧、⑦→⑥、⑤→④D.当K闭合后,甲、乙装置中pH变大,丙、丁装置中pH基本不变答案 A解析 当K闭合时,乙装置构成原电池,在电路中作电源,整个电路中电子的流动方向为③→②、①→⑧、⑦→⑥、⑤→④,A项错误,C项正确;当K断开时,乙装置中锌片与稀硫酸发生置换反应,产生氢气,B项正确;当K闭合后,乙装置中消耗H+,pH变大,甲装置中电解饱和食盐水,pH变大,丙装置中相当于在银上镀铜,pH基本不变,丁装置中相当于铜的电解精炼,pH基本不变,D项正确。【变式2】 某同学组装了如图所示的电化学装置,电极Ⅰ为Al,其他均为Cu,则下列说法正确的是( )A.电流方向:电极Ⅳ→→电极ⅠB.电极Ⅰ发生还原反应C.电极Ⅱ逐渐溶解D.电极Ⅲ的电极反应:Cu2++2e-===Cu答案 A解析 当多个池串联时,根据电池中的电极材料和电解质溶液能否自发反应可知,图示中左边和中间两池组成原电池,右边为电解池。电子移动方向为电极Ⅰ→→电极Ⅳ,电流方向与电子移动方向相反,A项正确;电极Ⅰ为原电池的负极,失去电子,被氧化,发生氧化反应,B项错误;电极Ⅱ为原电池的正极,铜离子在电极Ⅱ上得电子,生成铜单质,该电极质量逐渐增大,C项错误;电极Ⅱ为正极,所以电极Ⅲ为电解池的阳极,其电极反应式为Cu-2e-===Cu2+,D项错误。






