





中考化学总复习专题三物质的检验、鉴别、除杂与提纯课件完美
展开物质的检验、鉴别、除杂及提纯是初中化学的重点知识,也是中考必考的考点,常利用此类试题对物质的性质进行考查。 检验物质时根据物质的性质选择合适的检验方法,尽量以不消耗或少消耗原物质为原则。检验物质的三个原则:(1)看:颜色、状态。(2)嗅:气味。(3)实验:加试剂。
物质的鉴别,就是根据物质的特征反应,选择恰当的试剂和方法,准确观察反应中颜色的改变、沉淀的生成和溶解、气体的生成及气味等实验现象,最终区分出不同物质的实验探究过程。 除杂时根据原物质和杂质的性质选择适当的除杂试剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。 物质提纯的基本原则:1.不引入新的杂质。2.不减少被提纯物质。3.被提纯物质与杂质易分离。4.被提纯物质易复原。
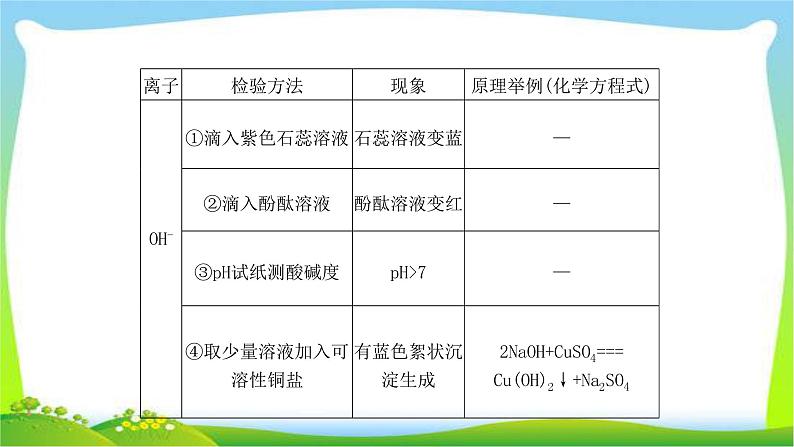
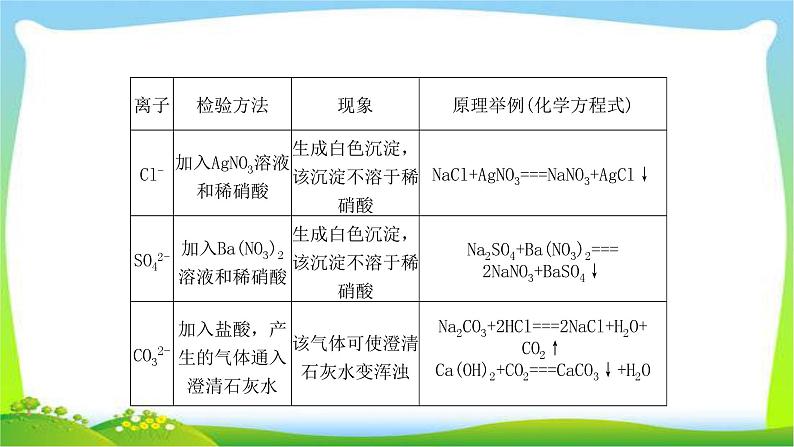
一、物质的检验1.常见离子的检验
二、常见物质的鉴别1.鉴别物质的原理a.利用一些离子间反应时的不同现象,如有气体、沉淀生成,或者变色等;b.利用物质气味、温度、溶解性等的不同。2.鉴别物质的方法(1)物理方法①根据物质颜色的不同a.常见固体的颜色 红色固体:铜、氧化铁;绿色固体:碱式碳酸铜;蓝色固体:氢氧化铜、硫酸铜晶体;紫黑色固体:
高锰酸钾;黑色固体:铁粉、木炭、氧化铜、二氧化锰、四氧化三铁、炭黑、活性炭。b.常见溶液的颜色 蓝色溶液:含Cu2+的溶液;浅绿色溶液:含Fe2+的溶液;黄色溶液:含Fe3+的溶液。②根据气味的不同 常见的具有刺激性气味的气体有:HCl、SO2、NH3。③根据物质的溶解性不同④根据物质溶解时的吸放热现象:NaOH溶于水放出热量,温度升高;NaCl溶于水温度保持不变;NH4NO3溶于水吸收热量,温度降低。
(2)化学方法①根据酸碱性不同,可使用石蕊溶液、酚酞溶液、pH试纸鉴别。②根据发生复分解反应的现象不同进行鉴别。3.常见物质的鉴别(1)纤维的鉴别:将纤维点燃,有________气味且燃烧后残留物是黑色能捏碎的是丝或毛;有烧纸气味的是__________;燃烧产物是黑色硬球且捏不碎的是合成纤维。(2)硬水与软水的鉴别:加入________并搅拌产生泡沫多、浮渣少的是________,反之则是________。
(3)铵态氮肥:加入熟石灰研磨,如果产生刺激性气味且能使湿润的红色石蕊试纸变蓝的气体,则为铵态氮肥。(4)氢氧化钠与氢氧化钙:通入二氧化碳气体,________的是氢氧化钙溶液,无现象的是氢氧化钠溶液。三、物质的分离与提纯 1.原则 (1)不增:不能引入新的杂质;(2)不减:不能使被提纯物质减少;(3)易分:操作简单,易于分离。 2.方法 (1)物理方法
(2)化学方法 a.沉淀法:加入某种试剂将杂质转化为沉淀,过滤除去。如HNO3中混有H2SO4,可加入适量的Ba(NO3)2,发生反应的化学方程式为__________________________________,将H2SO4转化为BaSO4沉淀后,过滤除去。常见的沉淀:
Ba2++SO42-→BaSO4↓ Ba2++CO32-→BaCO3↓ Ca2++CO32-→CaCO3↓ Mg2++2OH-→Mg(OH)2↓ Al3++3OH-→Al(OH)3↓ Fe3++3OH-→Fe(OH)3↓ Cu2++2OH-→Cu(OH)2↓ Ag++Cl-→AgCl↓
Ba(NO3)2+H2SO4===BaSO4↓+ 2HNO3
b.化气法:加入某种试剂将杂质转化为气体而除去。如NaCl溶液中混有少量Na2CO3,可加入适量稀盐酸,发生反应的化学方程式为_____________________________,将Na2CO3转化为二氧化碳气体除去。常见的转化有:
CO32-+2H+→H2O+CO2↑ NH4++OH-→H2O+NH3↑
c.加热法:将杂质通过加热除去或使其转化为被提纯物质。如CaO中混有少量CaCO3,可高温灼烧混合物:CaCO3====CaO+CO2↑,将碳酸钙转化为氧化钙。
Na2CO3+2HCl===2NaCl+CO2↑+H2O
d.置换法:在某些盐溶液中加入某种金属,把盐溶液中的金属置换出来,同时将杂质除去。如ZnSO4中混有CuSO4,可加入过量的Zn:Zn+CuSO4===ZnSO4+Cu,将硫酸铜转化为铜单质而除去。 e.吸收法:适用于气体混合物中杂质气体的除去,选择适当的试剂吸收杂质气体而不能与被提纯气体反应。酸性杂质气体如CO2、SO2、HCl等用碱性溶液吸收;碱性杂质气体如NH3等用酸性溶液吸收。 f.溶解法:将杂质溶解后转化为溶液除去。如Cu里混有少量CuO,可往混合物中加入过量的稀硫酸:CuO+H2SO4===CuSO4+H2O,再过滤,即可将CuO除去。
3.物质分离与提纯的技巧(1)被提纯物质与杂质所含阳离子相同时,选取与杂质中的阴离子不共存的阳离子,再与被提纯物中的阴离子组合出除杂试剂。如:NaNO3(NaCl)可选用AgNO3溶液为除杂试剂。(2)被提纯物质与杂质所含阴离子相同时,选取与杂质中的阳离子不共存的阴离子,再与被提纯物中的阳离子组合出除杂试剂。如:NaCl(BaCl2)可选用Na2SO4溶液为除杂试剂。(3)被提纯物质与杂质所含阴、阳离子都不相同时,选取与杂质中的阴、阳离子都不共存的阴、阳离子组合出除杂试剂。如:KNO3(CuSO4)可选用Ba(OH)2溶液为除杂试剂。
例1[2017甘肃,9]下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)( )
【解析】A.CO中的CO2可以用氢氧化钠溶液吸收并除去,故正确。B.加入稀盐酸将要保留的物质碳酸钾除去了,故错误。C.加入锌粉,把硫酸亚铁和硫酸铜都除去了,故错误。D.Zn和Fe都与稀硫酸反应,故错误。
例2[2017兰州,21]除去下列物质中的杂质,所用试剂和方法均正确的是( )
【解析】A.氮气不可燃不助燃,氮气中的少量氧气不能用燃着的木条除去,不能达到除杂目的,故错误。B.硝酸银和盐酸反应生成硝酸,引入新的杂质,不能达到除杂的目的,故错误。C.氢氧化钡和碳酸钠反应生成碳酸钡沉淀和氢氧化钠,能达到除杂目的,故正确。D.氯酸钾在二氧化锰的作用下分解,反而会把原物质除去,且引入了新的杂质二氧化锰,不能达到除杂目的,故错误。
例3[2017毕节]下列实验操作不能达到实验目的的是( )
【解题妙招】在解答此类问题时,首先要了解需要除去的是哪些物质,明确除杂时不能将原物质除去;然后选择适当的试剂进行除杂,在除杂时,如果杂质和所加试剂的状态一样,就要注意加入量的控制。
【解析】A.分别加少量水时,固体溶于水放热的是氢氧化钠,无明显现象的是氯化钠。B.硫酸钠和硝酸钡反应生成硫酸钡沉淀和硝酸钠,在除去硫酸钠的同时带入新的杂质硝酸钠,故错误。C.将混合气体通过装有浓硫酸的洗气瓶时,氢气中的水蒸气被浓硫酸吸收。D.取样与熟石灰混合研磨,能够产生刺激性气味的是氯化铵,无明显现象的是氯化钾,故正确。
2024河北中考化学复习 板块五 主题3 物质的检验、鉴别与除杂(2~4分) 课件: 这是一份2024河北中考化学复习 板块五 主题3 物质的检验、鉴别与除杂(2~4分) 课件,共41页。PPT课件主要包含了知识清单·理脉络,④化肥的检验,蒸发结晶,硫酸亚铁,硫酸铜溶液或硫酸,一氧化碳,高温煅烧,稀硫酸,降温结晶,常见除杂举例等内容,欢迎下载使用。
中考化学复习高频考点集中练7物质的检验、鉴别与除杂课件: 这是一份中考化学复习高频考点集中练7物质的检验、鉴别与除杂课件,共19页。PPT课件主要包含了CaOH2,复分解反应,溶液由红色变成无色,实验探究一,产生气泡,CaCl2,完全除去Na2CO3,NO-3,AgCl等内容,欢迎下载使用。
中考化学一轮复习考点讲练课件 物质的检验、鉴别与除杂 (含答案): 这是一份中考化学一轮复习考点讲练课件 物质的检验、鉴别与除杂 (含答案),共27页。PPT课件主要包含了变浑浊,出现水雾等内容,欢迎下载使用。












