
化学人教版 (2019)第一节 化学反应与能量变化导学案
展开
这是一份化学人教版 (2019)第一节 化学反应与能量变化导学案,共5页。学案主要包含了化学反应与能量,人类对能源的利用等内容,欢迎下载使用。
1.实验探究:
2.放热反应和吸热反应
(1)含义:
①放热反应:_________的化学反应。
②吸热反应:_________的化学反应。
(2)实例:
①放热反应:
②吸热反应:
冬季生活中常常采用下列方法获得热量:
①烧炭取暖;
②用电暖器取暖;
③天然气壁挂炉取暖;
④空调取暖;
⑤地下水循环取暖等,都属于放热反应吗?
二、化学键与化学反应中能量变化的关系
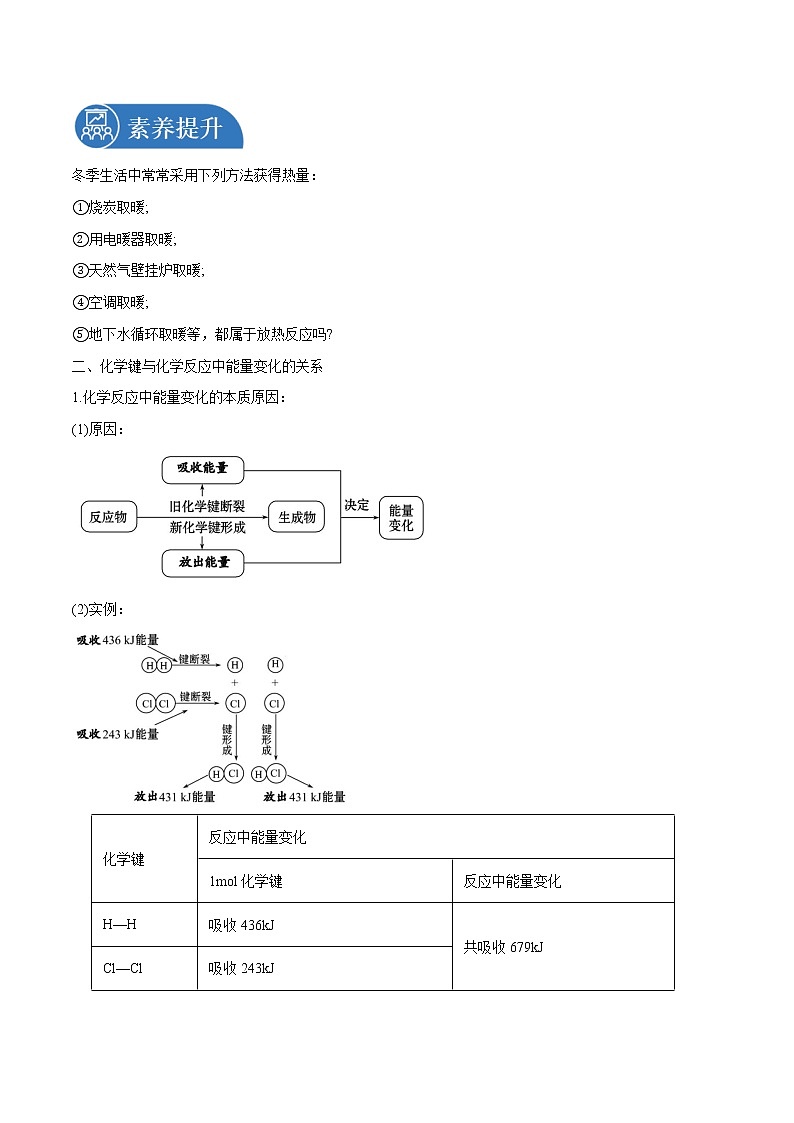
1.化学反应中能量变化的本质原因:
(1)原因:
(2)实例:
2.多角度分析化学反应的能量变化
三、人类对能源的利用
1.利用的三个阶段:
2.化石燃料利用过程中亟待解决的两方面问题
(1) ;(2) 。
3.在燃料利用过程中,节能的主要环节:
(1)燃料燃烧阶段——可通过改进锅炉的炉型和燃料空气比、清理积灰等方法提高燃料的燃烧效率;
(2)能量利用阶段——可通过使用节能灯,改进电动机的材料和结构,以及发电厂、钢铁厂余热与城市供热联产等措施促进能源循环利用,有效提高能量利用率。
4.新能源
(1)特点:资源丰富、______________________。
(2)人们比较关注的新能源:__________能、________能、地热能、海洋能和________能等。
例1.下列说法正确的是( )
A.Fe与S在加热条件下才能发生反应,所以该反应属于吸热反应
B.HNO3、H2SO4分别与NaOH溶液反应都放出热量
C.分解反应都是吸热反应,化合反应都是放热反应
D.合成氨的反应是放热反应,所以N2与其他物质的反应也是放热反应
例2.下列说法正确的是( )
A.任何化学反应都伴随着能量的变化
B.H2O(g)→H2O(l)该过程放出大量的热,所以该过程是化学变化
C.化学反应中能量的变化都表现为热量的变化
D.对于如图所示的过程,是吸收能量的过程
例3.关于吸热反应的说法正确的是( )
A.凡需加热的反应一定是吸热反应
B.只有分解反应才是吸热反应
C.使用催化剂的反应是吸热反应
D.CO2与CaO化合是放热反应,则CaCO3分解是吸热反应
例4.已知断裂1ml共价键所需要吸收的能量分别为H—H:436kJ,I—I:151kJ,H—I:299kJ,下列对H2(g)+I2(g)2HI(g)的反应类型判断错误的是( )
A.放出能量的反应 B.吸收能量的反应
C.氧化还原反应D.可逆反应
例5.化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或断开)1ml化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如图所示,现提供断裂(或形成)1ml以下化学键的吸收(或放出)的能量(kJ):P—P:198,P—O:360,O=O:498,则反应P4(白磷)+3O2==P4O6生成1mlP4O6( )
A.放出1638kJ热量 B.吸收1638kJ热量
C.放出126kJ热量D.吸收126kJ热量
课堂小结
实
验
操
作
【实验6-1】试管中加入2mL2ml·L-1盐酸,并用温度计测量其温度,再向试管中放入打磨过的镁条
【实验6-2】将20gBa(OH)2·8H2O晶体研细后与10gNH4Cl晶体一起放入烧杯中,并将烧杯放在滴有几滴水的木片上。用玻璃棒快速搅拌,玻璃片盖上烧杯
实
验
装
置
【实验6-1】
【实验6-2】
实
验
现
象
___________________________________
___________________________________
有刺激性气味气体产生,用手触摸杯壁下部,烧杯壁_______,试着用手拿起烧杯,________________。
实验
结论
该反应___________________________
该反应___________________________
化学反应发生时伴有____________________________________________________
化学键
反应中能量变化
1ml化学键
反应中能量变化
H—H
吸收436kJ
共吸收679kJ
Cl—Cl
吸收243kJ
H—Cl
放出431kJ
共放出862kJ
结论
679kJ--862kJ==-183kJ,即反应放出183kJ热量
分析角度
放热反应
吸热反应
微观
断键吸收的热量_____成键放出的热量
断键吸收的热量_____成键放出的热量
宏观
反应物的总能量_____生成物的总能量
反应物的总能量_____生成物的总能量
相关学案
这是一份化学必修 第二册第六章 化学反应与能量第二节 化学反应的速率与限度导学案,共6页。学案主要包含了化学反应速率,影响化学反应速率的因素等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第二册第六章 化学反应与能量第一节 化学反应与能量变化导学案,文件包含思维导图人教版高中化学必修二《611化学反应与热能》同步学习思维导图+学练解析版docx、思维导图人教版高中化学必修二《611化学反应与热能》同步学习思维导图+学练学生版docx等2份学案配套教学资源,其中学案共30页, 欢迎下载使用。
这是一份人教版 (2019)必修 第二册第一节 化学反应与能量变化导学案,共20页。学案主要包含了新知学习,知识进阶,问题探究,知识归纳总结,效果检测等内容,欢迎下载使用。










