





所属成套资源:菏泽专版中考化学总复习课件新人教版专题
菏泽专版中考化学总复习第一部分第三单元物质构成的奥秘第1课时微粒构成物质课件新人教版
展开这是一份菏泽专版中考化学总复习第一部分第三单元物质构成的奥秘第1课时微粒构成物质课件新人教版,共35页。PPT课件主要包含了考点梳理过关,辨一辨►,原子的构成与结构,核外电子排布,想一想►,典型例题运用,实验聚焦突破,典例分析,六年真题全练等内容,欢迎下载使用。
第三单元 物质构成的奥秘第1课时 微粒构成物质
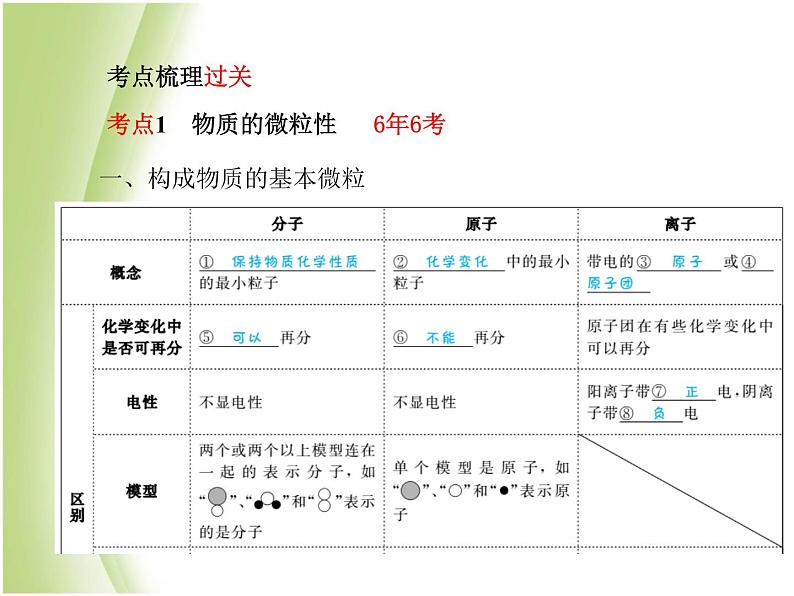
考点1 物质的微粒性 6年6考
一、构成物质的基本微粒
二、用分子、原子观点解释物质的变化
1.分子都比原子大。 ( × )2.同种原子可能构成不同分子。 ( √ )3.尘土飞扬是分子不断运动的结果。 ( × )4.分子是保持物质化学性质的唯一粒子。 ( × )5.由同种分子构成的物质是纯净物,所以由同种原子构成的物质也一定是纯净物。 ( × )6.分子能再分,原子不能再分。 ( × )7.混合物是由不同种分子构成的,纯净物是由同种分子构成的。 ( × )
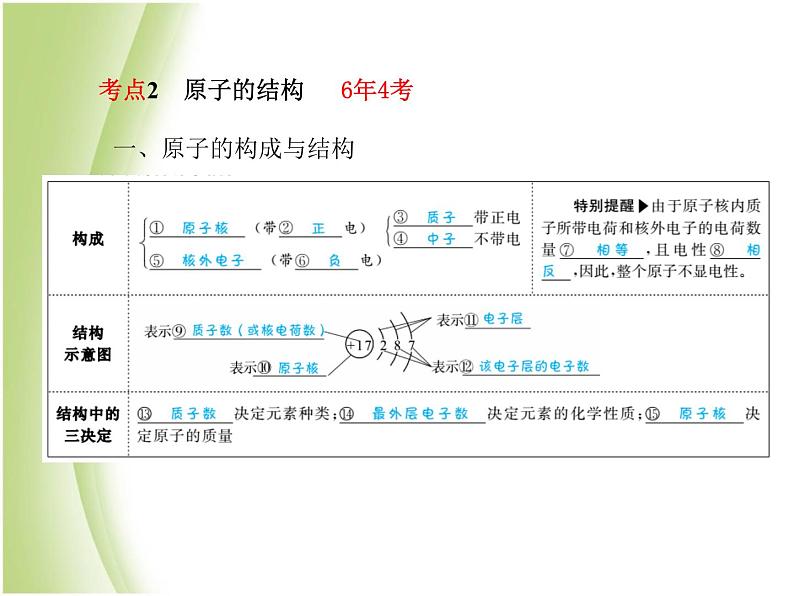
考点2 原子的结构 6年4考
三、相对原子质量及其近似计算
1.最外层电子数小于4的原子一定是金属原子。 ( × )2.在原子中质子数一定等于中子数。 ( × )3.原子中最外层电子数决定了原子在化学变化中是否容易得失电子。 ( √ )4.不同原子的原子核内中子数可能相等。 ( √ )5.所有原子的原子核都是由质子与中子构成的。 ( × )6.最外层电子数相同,化学性质一定相似。 ( × )7.具有相对稳定结构的原子,最外层都有8个电子。 ( × )
考点3 离子 6年6考
原子变成离子时,质子数是否发生改变?化学性质是否发生了改变?原子通过得失最外层电子形成离子,质子数不变,但化学性质发生了改变,如钠原子容易失去最外层的电子,失去电子变为钠离子后就不容易失去电子。
解析:分子是保持物质化学性质的最小粒子,分子不能保持物质的物理性质,A错误;原子可以分为原子核和核外电子,B错误;原子得到电子形成阴离子,失去电子变成阳离子,C正确;分子比构成它的原子的质量大,但不同的分子、原子无法比较大小,D错误。
类型1 有关原子、分子、离子的认识
【例1】[2017·怀化中考]下列关于分子、原子、离子的说法正确的是( C )A.分子是保持物质性质的最小粒子 B.原子是最小的粒子 C.原子得到电子或失去电子变成离子 D.分子一定比原子大
解题方法►在物质构成的相关知识中,同学们要弄清构成物质的三种微粒,关于构成的三个层次以及构成原子的各微粒之间的关系,才能真正掌握“三子”的相关联系,形成完备而有序的知识网络。其关系如下图所示:
注意事项►分子和原子的本质区别,不能认为分子可分而原子不可分,只有在“化学变化”的前提条件下,才是正确的。没有“化学变化”这个前提,原子仍是可分的。也不能简单地认为分子比原子大,不同种物质的分子和原子不能比较其大小。
变式训练►1.下列关于微粒的说法正确的是( )A.物质都是由分子构成的 B.热胀冷缩是由于微粒大小发生了变化 C.原子和离子不能相互转化 D.构成物质的微粒是在不停地运动的
D 物质是由分子、原子或离子构成的,A项错误;热胀冷缩是由于微粒间隔发生了变化,微粒大小没有变化,B项错误;离子是带电的原子或原子团,原子得失电子后会变成离子,离子再失得电子后就可能变成原子,C项错误;构成物质的微粒是在不断运动的,D项正确。
2.[2016·聊城中考]下列对分子、原子、离子的认识,不正确的是( )A.分子、原子、离子都能构成物质 B.气体压缩为液体,分子体积变小 C.温度越高,分子运动越快 D.钠原子和钠离子的化学性质不同
B 构成物质的微粒有分子、原子、离子,A正确;气体压缩为液体,分子间隔变小,分子体积不变,B错误;温度越高,分子运动越快,C正确;钠原子失去1个电子形成钠离子,钠原子和钠离子化学性质不同是由于其最外层电子数不同,D正确。
【例2】[2017·烟台中考]如图是四种粒子的结构示意图,下列说法正确的是( D )
解析:同种元素的粒子质子数相同,②③的核内质子数不同,不属于同种元素,A错误;决定元素化学性质的是最外层电子数,②④的最外层电子数不同,则化学性质不同,B错误;②的质子数为13,核外电子数为10,质子数>核外电子数,为带3个单位正电荷的铝离子,其离子符号为Al3+,C错误;镁原子的最外层电子数为2,该元素在化合物中显+2价;氟原子的最外层电子数为7,则该元素在化合物中显-1价,故组成化合物的化学式为MgF2,D正确。
类型2 原子的结构、微粒的结构示意图
A.②③属于同种元素 B.②④的化学性质相同C.②的符号为Al+3 D.①③形成的化合物是MgF2
解题方法►由结构示意图判断粒子是原子还是离子的关键是看核内质子数与核外电子总数的关系。当质子数=核外电子数时,表示原子;当质子数>核外电子数时,表示阳离子;当质子数 < 核外电子数时,表示阴离子。
易错分析►对原子结构及示意图所表示的意义不清楚而导致错误。不清楚不同元素之间的本质区别及最外层电子在化学反应中的作用是本题出错的主要原因。
变式训练►3.[2016·连云港中考]目前世界上最精准的钟是以锶做钟摆的钟。锶的原子结构示意图及在元素周期表中某些信息如下图所示,下列说法正确的是( )
D 原子中,质子数=核外电子数,故x=38-2-8-8-2=18,A错误;锶的偏旁部首是“钅”,属于金属元素,B错误;相对原子质量是一个比值,单位是“l”,不是“g”,C错误;锶原子的最外层电子数为2,小于4,故在化学反应中易失去电子,D正确。
A.x的值为8B.锶属于非金属元素C.锶的相对原子质量为87.62gD.锶原子在化学反应中易失去电子
4.[2016·泰安中考]下列关于四种粒子的结构示意图的说法中正确的是( )
B 同种元素质子数一定相同,①③的质子数都是17,两者属于同种元素,A项错误;②所示原子最外层电子数是1,在化学反应中易失掉1个电子带一个单位正电荷,所以②表示的元素在化合物中通常显+1价,B项正确;元素的化学性质和最外层电子数关系密切,一般情况下最外层电子数相同则化学性质相似,②③的最外层电子数分别是1、7,故化学性质不会相似,C项错误;④中质子数等于核外电子数,是原子,D项错误。
A.①③是不同种元素 B.②表示的元素在化合物中通常显+1价C.②③的化学性质相似 D.①④表示的是离子
实验2:分子运动现象的实验探究
【例】[2015·武汉中考]小明同学对探究分子性质的实验(图1)进行了改进。如图2所示,试管丁、戊中各有一张每隔2厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的小药瓶固定在橡皮塞上,试管丁中小药瓶上的瓶塞已塞紧,试管戊中的小药瓶上无瓶塞。关于图1、图2中的实验有以下说法:
①图2比图1的实验更环保、更节约;②图1和图2的实验均能证明分子在不断运动;③浓盐酸有挥发性,仅将浓氨水换成浓盐酸也可达到实验目的;④如果丁中没有小药瓶,图2的实验也可达到实验目的;⑤若将戊浸入冰水中,滤纸条不会变红。以上说法中错误的是( C )A.①② B.③④ C.③⑤ D.④⑤
分析►①图2实验是在密封的小容器内进行的,与图1比较更环保、更节约,正确;②图1中乙烧杯中的酚酞溶液变红色,丙烧杯中的酚酞不变色;图2中丁试管中的滤纸不变色,戊试管中滤纸条上的酚酞变红色,二者均说明分子在不断地运动,正确;③盐酸不能使无色酚酞溶液变色,错误;④如果丁中没有小药瓶,根据戊中滤纸条的酚酞点由外向里依次变红也可达到实验目的,正确;⑤分子在不同温度下都是在不断运动的,错误;故选C。
命题挖掘►如图所示的实验不能说明的是( )
A.分子在不停地运动 B.盐酸能使紫色石蕊溶液变红 C.构成物质的微粒不同,性质不同 D.化学反应的实质是分子分裂为原子,原子重新结合成新分子
D 浓盐酸和紫色石蕊溶液没有接触,但是石蕊溶液变红了,说明分子在不断地运动,A正确;盐酸挥发出的氯化氢气体进入石蕊溶液中,石蕊溶液变红,说明盐酸能使紫色石蕊溶液变红,B正确;该实验中紫色石蕊溶液变红,是因为氯化氢分子运动到紫色石蕊溶液烧杯中溶于水使溶液变红,说明构成物质的微粒不同,性质不同,C正确;此实验不能证明化学反应的实质是分子分裂为原子,原子重新结合成新分子,D错误。
命题点1 物质的微粒性
用微观粒子的性质解释生活中的常见现象主要以识别与选择的形式考查,有时也会在理解与应用中涉及。命题内容包括:微观粒子是在不断运动的;微粒之间有间隔;物质的化学性质不同与粒子的种类不同有关。
B 同一原子中,质子数=核外电子数=核电荷数=原子序数;在阳离子中,质子数>核外电子数;在阴离子中,质子数<核外电子数,该图为氧原子的结构示意图。H2O和H2O2中氢元素的化合价相同,都是+1价,水中氧元素为-2价,过氧化氢中氧元素的化合价为-1价。由两种或两种以上物质组成的物质叫混合物;由一种物质组成的物质叫纯净物;水和冰块是同种物质,混合形成纯净物。水沸腾时可冲起壶盖,原因是液态水受热变成水蒸气时,水分子之间的间隔变大,水分子本身的大小不变。
1.[2017·菏泽5题2分]水是由氢元素和氧元素组成的,下列有关说法正确的是( )A.氧离子的结构示意图为B.H2O和H2O2中氢元素的化合价相同C.水和冰块混合形成混合物D.水沸腾时可冲起壶盖,说明温度升高水分子变大
B 水是由水分子构成的,水分子保持水的化学性质,A项错误;化学反应的实质就是构成物质的分子先分裂成原子,原子再重新组合成其他物质的分子,B项正确;水变成水蒸气发生的是物理变化,变化过程中仅是水分子间的间隔变大,水分子本身并没有发生变化,C项错误;花香四溢是因为构成花香物质的分子在不停地运动,D项错误。
2.[2015·菏泽5题2分]对于下列说法,有关微观解释正确的是( )A.水分子是由氢原子和氧原子构成的,氢原子和氧原子能保持水的化学性质B.化学反应过程的实质是分子破裂原子重新组合C.将水加热变成水蒸气,体积变大,是因为水分子体积变大D.花香四溢主要是因为分子间有间隔
押题预测►1.用分子、原子的观点解释下列现象,其中不合理的是( )A.品红在水中扩散——分子在不断运动B.水结成冰——分子停止运动C.1滴水中大约有1.67×1021个水分子——分子很小D.气体可以压缩储存在钢瓶中——分子间有间隔
B 品红在水中扩散,是因为品红分子在不断地运动,运动到水分子中间去了,A合理;分子总是在不断地运动着,冰中的分子仍是在不断地运动,B不合理;一滴水中大约有1.67×1021个水分子,说明水分子很小,C合理;由于分子之间有间隔,在受压时间隔变小,所以气体可以压缩储存在钢瓶中,D合理。
原子的结构在考查时常结合热点信息或实际应用进行考查,主要考查点为原子结构、原子结构示意图。
命题点2 原子的结构
3.[2014·菏泽3题2分]下列是几种微粒的结构示意图,有关说法错误的是( )
B 微粒①最外层电子数为7,大于4,易得到1个电子,所以A项正确;微粒②和④核内质子数不相等,不属于同种元素,所以B项错误;微粒③最外层电子数为1,小于4,易失去1个电子而形成+1价的金属阳离子,所以C项正确;微粒④是失去2个电子后形成的阳离子,所以D项正确。
A.微粒①易得到电子B.微粒②和④核外电子排布相同,属于同种元素C.微粒③易形成+1价金属阳离子D.微粒④带两个单位正电荷
B 原子结构示意图中圆圈里面的数字表示质子数,所以氯原子核内有17个质子,故选项B正确;第一电子层有2个电子,故选项A错误;最外层有7个电子,易得到1个电子达到8电子的稳定结构,故选项C错误;氯化铝的化学式为AlCl3,故选项D错误。
4.[2013·菏泽6题2分]如图是氯元素的原子结构示意图,下列叙述正确的是( )A.氯原子第一电子层有7个电子B.氯原子核内有17个质子C.氯原子在化学反应中容易失去电子D.氯与铝形成物质的化学式为AlCl2
押题预测►2.根据如图提供的信息进行判断,下列说法中,错误的是( )A. 该粒子原子核内有11个质子B. 该粒子属于金属元素C. 该粒子易形成阴离子D. 该粒子呈电中性
C 由粒子结构示意图可看出,该粒子核内有11个质子,A正确;该粒子是钠原子,最外层电子数为1(小于4),属于金属元素,B正确;该粒子易失去最外层的1个电子,形成阳离子,C错误;该粒子核内质子数为11,核外电子数也为11,呈电中性,D正确。
有关原子、分子、离子的认识是中考的常考考点,主要以选择题和填空题形式出现,结合构成物质的微粒,分子、原子在化学反应中的变化,对分子、原子、离子的说法正误进行分析判断。
命题点3 有关原子、分子、离子的认识
5.[2013·菏泽3题2分]下列有关物质变化的说法错误的是( )A.粉笔写字的过程是物理变化B.在化学变化中,分子可以变成其他分子C.在化学变化中,原子可以变成其他原子D.在化学变化中伴随着能量变化
C 粉笔写字的过程中没有其他物质生成,属于物理变化,A正确;在化学变化中分子可以分成原子,原子再重新组合成其他的分子,所以在化学变化中,分子可以变成其他分子,B正确;原子是化学变化中的最小粒子,不会改变,C错误;在化学变化中伴随着能量变化,有的反应放热,有的反应吸热,D正确。
押题预测►3.下列关于原子、分子的说法错误的是( )A.分子可以构成物质,而原子只能构成分子B.在化学变化中,分子可以分成原子,而原子不能再分C.在原子中,质子数等于核外电子数D.分子是保持物质化学性质的最小粒子
A 分子是构成物质的一种粒子,原子、离子也能构成物质,A错误。
4.下面是4位同学对分子、原子、离子的描述,其中正确的是( )
B 分子和原子不带电荷,A错误;分子、原子、离子都可以直接构成物质,B正确;分子在化学变化中可以再分,C错误;由分子构成的物质,其化学性质由分子保持,而物理性质不由分子保持,D错误。
相关课件
这是一份福建省中考化学复习专题一物质构成的奥秘第1课时微粒构成物质认识化学元素课件,共16页。PPT课件主要包含了保持物质化学性质,化学变化中,微粒的质量大小,做无规则运动,氯化钠,二氧化碳,针对训练,图1-1,考点2原子的构成,原子核等内容,欢迎下载使用。
这是一份北京专版中考化学基础复习一物质构成的奥秘第1课时构成物质的微粒课件,共16页。PPT课件主要包含了氧分子,铁原子,钠离子和氯离子,水分子,铜原子,分子在不断运动,分子之间有间隔,氢原子,氧原子,两个氢原子等内容,欢迎下载使用。
这是一份菏泽专版中考化学总复习第一部分第三单元物质构成的奥秘第2课时物质的组成和分类课件新人教版,共32页。PPT课件主要包含了考点梳理过关,元素的分类,元素符号,想一想►,物质的总体分类,酸碱盐的比较,有机化合物,辨一辨►,典型例题运用,六年真题全练等内容,欢迎下载使用。












