


湖南省中考化学复习突破专题五流程图题课件
展开
这是一份湖南省中考化学复习突破专题五流程图题课件,共29页。PPT课件主要包含了Cl2,HCl,蒸发池,饱和溶液,玻璃棒,复分解反应,作氮肥,CaCO3,H2O,氯化钠等内容,欢迎下载使用。
1. 流程图题型的结构题头(引入信息)→题干(提取信息,应用解题)→题尾(得出结论或产品)。2. 解题方法和思路
3. 具体操作(1)关注“箭头”:箭头进入的是投料(即反应物),出去的是生成物(包括主产物和副产物)。
(2)关注方框内所指。
(3)关注流程“三线”和“核心”(如图)。三线:出线和进线方向表示物料流向或操作流程,可逆线表示物质循环使用。
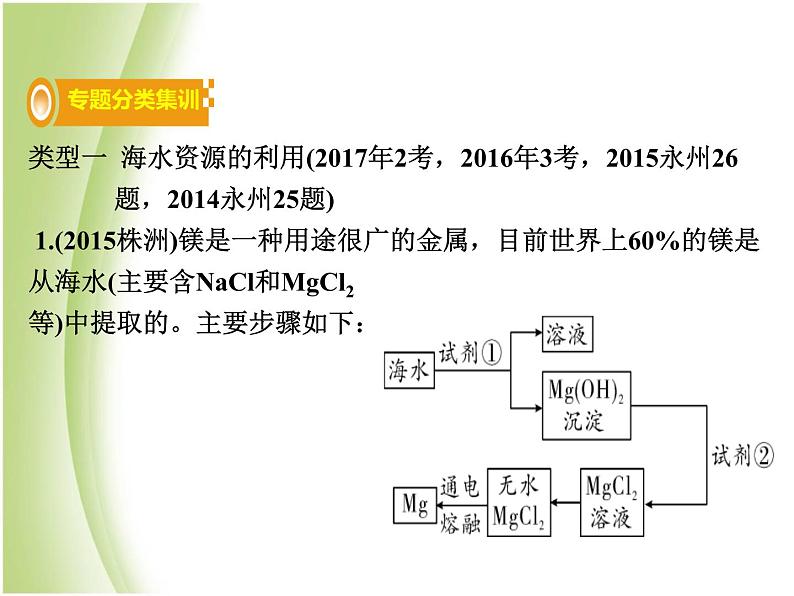
类型一 海水资源的利用(2017年2考,2016年3考,2015永州26 题,2014永州25题) 1.(2015株洲)镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含NaCl和MgCl2等)中提取的。主要步骤如下:
(1)上述步骤中试剂①应过量,理由是__________________________。(2)请写出Mg(OH)2沉淀与试剂②发生中和反应的化学方程式______________________________________。(3)无水MgCl2在熔融状态下通电得到金属镁和物质A,氢气在物质A中燃烧生成物质B,则物质A和B的化学式分别为:A________,B________。
使海水中的氯化镁充分反应
【解析】(1)MgCl2+2NaOH Mg(OH)2↓+2NaCl,试剂①为NaOH,若氢氧化钠量少,海水中的氯化镁反应不完,氢氧化钠过量能把海水中的氯化镁反应完。(2)根据提示,氢氧化镁与试剂②发生的是中和反应,故试剂②是酸,反应生成了氯化镁,所以试剂②是盐酸,发生反应的化学方程式为Mg(OH)2+2HCl MgCl2+2H2O。(3)MgCl2 Mg+Cl2 ↑,H2+ Cl2 2HCl,故A为Cl2,B为HCl。
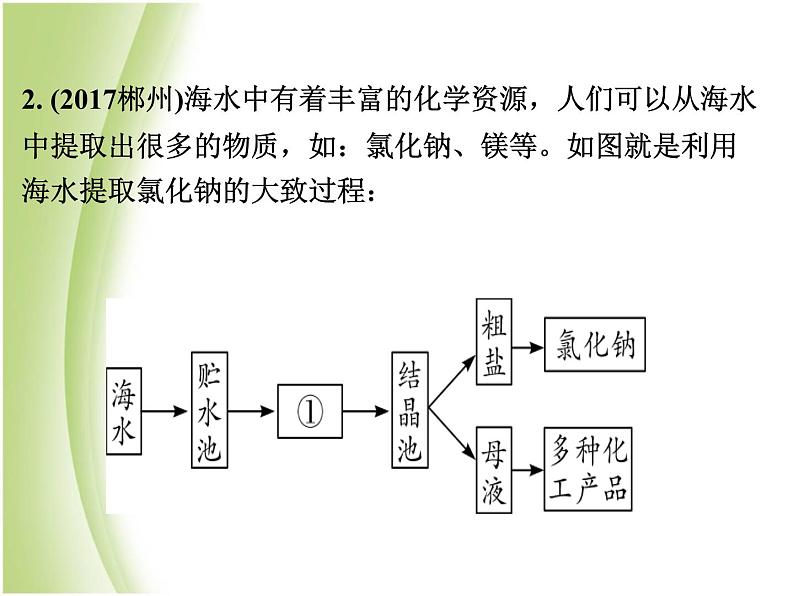
2. (2017郴州)海水中有着丰富的化学资源,人们可以从海水中提取出很多的物质,如:氯化钠、镁等。如图就是利用海水提取氯化钠的大致过程:
(1)图中①是________(填“蒸发池”或“冷却池”);(2)析出晶体后的母液是氯化钠的___________(填“饱和 溶液”或“不饱和溶液”);(3)实验室除去粗盐中难溶性杂质的主要实验步骤有: Ⅰ溶解 Ⅱ________(填操作名称) Ⅲ蒸发上述三个步骤中,用到的同一种玻璃仪器的名称是________,该玻璃仪器在步骤Ⅱ中的作用是________;
(4)提取粗盐后的母液中含有较多氯化镁,从母液中提取金属镁的过程大致如下:该过程中反应Ⅰ的基本反应类型是_________________;写出反应Ⅱ的化学方程式为____________________________。
【解析】(2)析出晶体后的母液不能继续溶解氯化钠固体,因此,该母液是氯化钠的饱和溶液。(3)实验室除去粗盐中难溶性杂质的主要操作步骤是:溶解、过滤、蒸发。三个步骤中都要用到玻璃棒,过滤时玻璃棒的作用是引流。(4)反应Ⅰ是氯化镁与氢氧化钙的反应,是由两种化合物相互交换成分,生成另外两种化合物的反应,它属于复分解反应。反应Ⅱ的一种反应物是氢氧化镁,生成物是氯化镁,则试剂X为HCl,其化学方程式为Mg(OH)2+2HCl MgCl2+2H2O。
类型二 矿产资源的利用(2017娄底43题,2016株洲28题,2015常德29题)(2017娄底)碳酸亚铁(FeCO3)可用于制作补铁药物,以下是用硫铁矿烧渣(主要成分为Fe2O3、SiO2等)为原料制备碳酸亚铁的生产流程示意图:【资料】40 ℃以上时,(NH4)2CO3易分解。
(1)操作Ⅰ的名称为________。(2)写出向固体A中加入稀硫酸后发生反应的化学方程式:________________________________。(3)加入(NH4)2CO3后,该反应必须控制的条件是_____________________。(4)从溶液C中可回收一种化工产品,请写出它的一种用途______________。
温度在40 ℃以下
Fe+H2SO4 FeSO4+H2↑
【解析】(1)过滤的方法可以将不溶物和液体分离,SiO2固体不溶于水,要将它与溶液B分开,可以使用过滤的方法,所以操作Ⅰ的名称为过滤。(2)硫铁矿烧渣与足量CO在高温下反应,得到的固体A中含有铁与二氧化硅。向固体A中加入过量稀硫酸,铁可以与稀硫酸反应生成硫酸亚铁和氢气,而二氧化硅不能与稀硫酸发生反应,其化学反应方程式为Fe+H2SO4 FeSO4+H2↑。(3)40 ℃以上时,(NH4)2CO3易分解,因此加入(NH4)2CO3后,温度必须控制在40 ℃以下。(4)溶液C中可回收的化工产品中含有硫酸铵,由于它组成中含有氮元素,故可用作氮肥。
类型三 “三废”的利用(2016湘潭27题) 1.(2016湘潭)某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题。
(1)固体A中含有____和___,无色气体X为____(均填化学式)。(2)步骤①中反应的化学方程式为________________________, 该反应属于四种基本类型中的________反应。(3)操作a的名称为________,在该操作中用到了玻璃棒其作用 为________。(4)理论上所得硫酸亚铁晶体的质量____(填“>”“
相关课件
这是一份鲁教版中考化学复习题型突破五流程图题课件,共40页。PPT课件主要包含了酒精灯,蒸发皿,富集氯化镁,等合理即可,Fe2+,FeSO4,Fe或铁,更充分,除去废料中的铁,CO2等内容,欢迎下载使用。
这是一份人教版中考化学复习题型突破六流程图题练习课件,共47页。PPT课件主要包含了富集氯化镁,除去氢氧化钠和碳酸钠,氯化钠或NaCl,潮汐能合理即可,有机化合物,氩气的化学性质不活泼,CrOH3,催化作用,NH3•H2O,CuNO32等内容,欢迎下载使用。
这是一份人教版中考化学复习题型突破六流程图题课件,共37页。PPT课件主要包含了富集氯化镁,复分解反应,HCl,Mg2+,FeOH3,作氮肥,CuNO32,CuAg,混合物,H2SO4等内容,欢迎下载使用。








