
化学九年级第一学期3.2 溶液测试题
展开最新人教版九年级化学下册第九单元溶液同步训练试卷【精编】
(考试时间:90分钟,总分100分)
班级:__________ 姓名:__________ 分数:__________
一、单选题(每小题3分,共计24分)
1、属于溶液的是
A.八宝粥 B.汽水 C.珍珠奶茶 D.蒸馏水
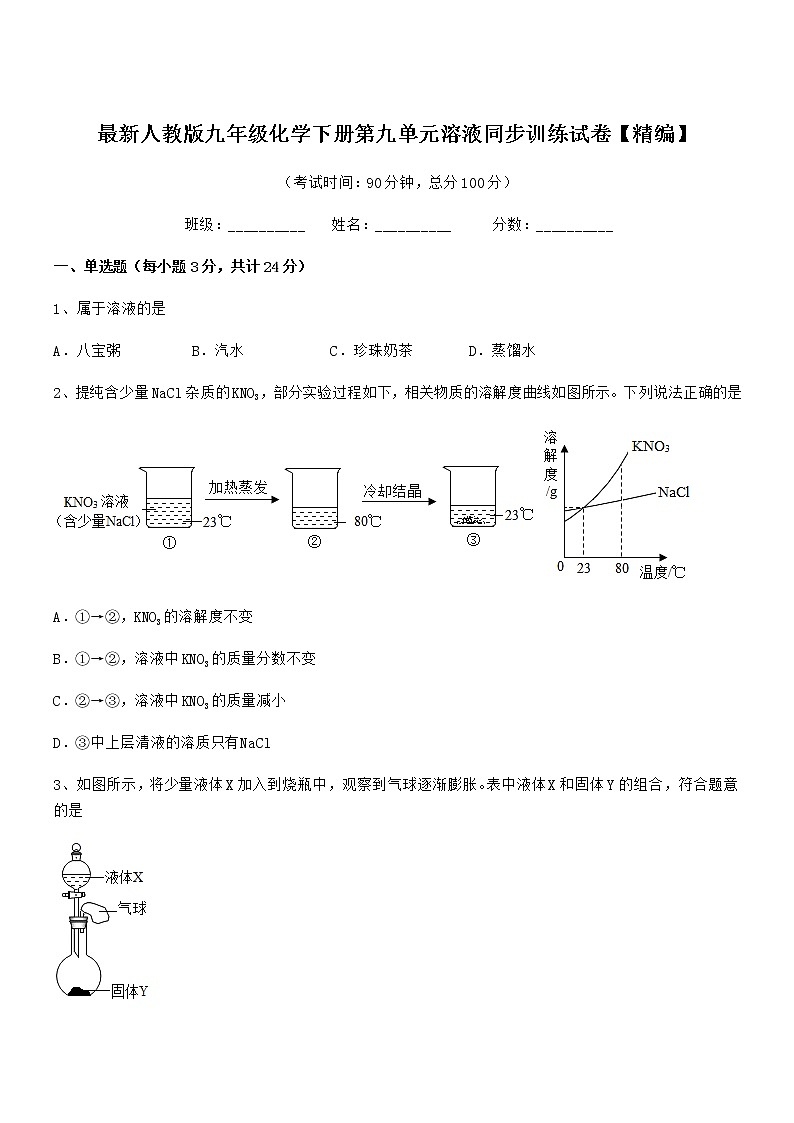
2、提纯含少量NaCl杂质的KNO3,部分实验过程如下,相关物质的溶解度曲线如图所示。下列说法正确的是
A.①→②,KNO3的溶解度不变
B.①→②,溶液中KNO3的质量分数不变
C.②→③,溶液中KNO3的质量减小
D.③中上层清液的溶质只有NaCl
3、如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀。表中液体X和固体Y的组合,符合题意的是
| ① | ② | ③ | ④ |
X | 稀盐酸 | 水 | 水 | 水 |
Y | 锌粒 | 氯化钠 | 氢氧化钠 | 硝酸铵 |
A.①② B.①③ C.①③④ D.②③④
4、下列有关溶液的说法不正确的是
A.氯化钠溶于水就是钠离子和氯离子在水分子作用下均匀扩散到水中的过程
B.溶液加水稀释前后溶质的质量不变
C.同种溶质的饱和溶液与不饱和溶液通过改变条件可以相互转化
D.均一、稳定的液体一定是溶液
5、如图是a、b、c三种固体物质的溶解度曲线,下列分析正确的是
A.若b中混有少量的a,可采用降温结晶的方法提纯b
B.t2℃时,物质a的100g饱和溶液中含有25g物质a
C.t3℃时,分别将a、b、c的饱和溶液降温至t1℃,溶质质量分数关系是b>a=c
D.t2℃时向50g水中加入15g物质b充分搅拌,所得溶液质量一定小于65g
6、配制50g溶质质量分数20%的硝酸钾溶液,下列图示错误的是
A.称固体 B.量液体
C.溶解 D.装瓶贴标签
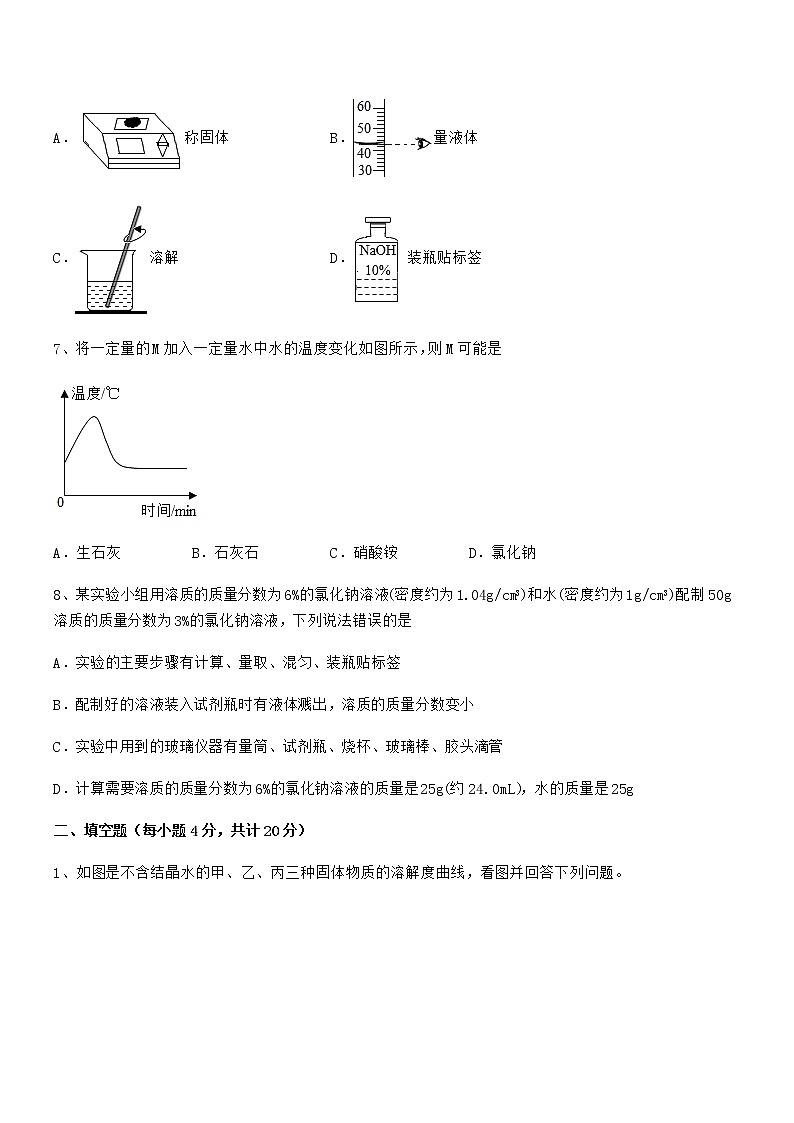
7、将一定量的M加入一定量水中水的温度变化如图所示,则M可能是
A.生石灰 B.石灰石 C.硝酸铵 D.氯化钠
8、某实验小组用溶质的质量分数为6%的氯化钠溶液(密度约为1.04g/cm3)和水(密度约为1g/cm3)配制50g溶质的质量分数为3%的氯化钠溶液,下列说法错误的是
A.实验的主要步骤有计算、量取、混匀、装瓶贴标签
B.配制好的溶液装入试剂瓶时有液体溅出,溶质的质量分数变小
C.实验中用到的玻璃仪器有量筒、试剂瓶、烧杯、玻璃棒、胶头滴管
D.计算需要溶质的质量分数为6%的氯化钠溶液的质量是25g(约24.0mL),水的质量是25g
二、填空题(每小题4分,共计20分)
1、如图是不含结晶水的甲、乙、丙三种固体物质的溶解度曲线,看图并回答下列问题。
(1)M点表示的含义是___________。
(2)t2℃时,将20g甲物质加入到50g水中,充分溶解后所得溶液的质量是___________g。
(3)t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温至t2℃,所得溶液中溶质质量分数由大到小的顺序是___________。
(4)若甲物质中混有少量乙物质,最好采用___________的方法提纯甲。
2、如图是a、b、c三种物质的溶解度曲线,请据图回答:
(1)P点的含义是______;
(2)t2℃时30g a物质加入到50g水中不断搅拌,充分溶解后形成溶液的质量是______g,此时a的溶质质量分数为______;
(3)将t1℃的a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数的大小关系是______;
(4)t2℃时,将c的饱和溶液变成不饱和溶液,可采取的方法是______(填一种方法),变为不饱和溶液后,溶液的质量分数一定会______(填“变大”、“变小”、“不变”或 “不确定”)。
3、A、B、C三种固体物质的溶解度曲线如图所示。回答下列问题。
(1)P点的意义为_____。
(2)t2℃时分别把10gA、B、C加入50g水中,能形成饱和溶液的是_____。
(3)将t1℃的A、B、C的饱和溶液分别升温到t2℃,所得溶液的溶质质量分数由大到小的顺序为_____。
4、如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)A点的含义是______。
(2)在30 ℃时,向30克甲物质中加入50克水,充分溶解后所得溶液是______溶液(填“饱和”或“不饱和”)。
(3)若乙中混有少量甲,最好采用______的方法提纯乙。
(4)将30 ℃时甲、乙、丙三种物质的饱和溶液降温到10 ℃,则其溶质质量分数不变的物质是______。
(5)20℃时甲、乙、丙三种物质的溶解度由大到小的顺序是______。
5、2021年世界水日的主题是“珍惜水,爱护水”,请回答下列与水有关的问题:
(1)向某自来水样品中加入一定量的肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该自来水属于_________(填“硬水”或“软水”);
(2)生活中常用_________的方法降低水的硬度;
(3)电解水实验证明了水是由_________组成的;
(4)用洗洁精清洗餐具上的油污,利用了洗洁精对油污的_________作用;
(5)珍惜水资源是每个公民应尽的责任和义务,请写出节约用水的一种具体做法__________。
三、计算题(每小题4分,共计36分)
1、某化学兴趣小组取部分变质的 Ca(OH)2(含杂质 CaCO3)样品8.0g投入200.0g水中,充分搅拌,通入足量CO2,溶质质量与反应的 CO2质量的关系如图所示。[提示:CaCO3+H2O+CO2=Ca(HCO3)2,Ca(HCO3)2能溶于水]
(1)Ca(OH)2全部转化为CaCO3时消耗的CO2 质量为______g。
(2)8.0g样品中杂质CaCO3 的质量为多少?
(3)通入 m3g CO2时,溶液中溶质的质量为多少?
2、中华文化源远流长,早在西汉时期《淮南万毕术》一书中就有“曾青得铁则化为铜”的记载,这是我国现代“湿法炼铜”的先驱。利用此原理,向160kg含硫酸铜的废液中加入足量的铁粉,得到金属铜6.4kg。请计算废液中硫酸铜的溶质质量分数。
3、为测定实验室中某过氧化氢溶液的溶质质量分数,小明取34.0g过氧化氢溶液放入烧杯中,然后进行如图所示的实验。请计算:
(1)反应后产生气体的质量为_________g。
(2)此过氧化氢溶液中溶质的质量分数。(写出计算过程)
4、现有14.9克纯碱样品(含Na2CO3和NaCl的混合物),将其放入干净的烧杯中,加入水使其完全溶解,向所得溶液中缓慢加入一定质量分数的稀盐酸(反应方程式为:)。产生气体的质量与加入稀盐酸的质量关系如图所示,
回答下列问题:
(1)产生CO2的质量为_________克。
(2)所用稀盐酸中氯化氢的质量分数是_____?
5、有效预防登革热的方法之一就是用杀虫剂对室外水沟、垃圾池周围以及有杂草的地方进行喷洒灭蚊。某街道决定采用高效氯氰菊酯杀虫剂进行喷杀,瓶上的标签如下表所示。求:
氯氰菊酯杀虫剂1000mL | |
溶质的质量分数 | 80% |
密度 | 1.2g/cm3 |
具有强毒性,阴冷,密封储藏 | |
(1)1000mL氯氰菊酯杀虫剂的质量是___________g,其中含溶质氯氰菊酯___________g。
(2)欲配制30kg溶质质量分数为20%的氯氰菊酯杀虫剂来消毒,需要这种氯氰菊酯杀虫剂的质量是多少?
6、某同学为定量研究氢氧化钠溶液与稀盐酸反应,做了如下实验:取适量的溶质质量分数为10%的氢氧化钠溶液,加入到50克溶质质量分数为7.3%的稀盐酸中,恰好完全反应。求:(写计算过程)
(1)加入的氢氧化钠溶液的质量。
(2)反应后所得溶液中溶质的质量分数。
7、69中学化学兴趣小组的同学,将用石灰石与稀盐酸制取8.8gCO2后的固液混合物206.3g,倒入废液缸中进行如下探究和处理:
已知在(1)中盐酸反应一半,(2)中盐酸恰好完全反应。
(1)实验过程中发生反应的化学方程式______;
(2)与氧化钙反应的物质质量(X)的比例式______;
(3)所用石灰石的纯度______;
(4)最后所得溶液中溶质的质量分数______;
(5)用36.5%的盐酸配置实验所需的稀盐酸400g,加水的质量为______。
8、计算题
为测定某过氧化氢溶液的溶质质量分数,取68g过氧化氢溶液和2g二氧化锰与烧杯中,充分反应后烧杯中物质的总质量为66.8g。
(1)氧气的质量为____________。
(2)求过氧化氢溶液的溶质质量分数_____。
9、为测定某氯化钠溶液中溶质的质量分数,做如下实验:向烧杯中加入10 g该氯化钠溶液,然后向其中滴加硝酸银溶液,发生反应生成氯化银沉淀。滴加硝酸银溶液质量与产生沉淀质量关系如图所示。根据实验计算:
(1)该反应生成沉淀的质量为______克。
(2)该氯化钠溶液中溶质的质量分数为多少?(提示:化学反应方程式为 NaCl+AgNO3=NaNO3+AgCl↓)
四、实验探究(每小题5分,共计20分)
1、据报道:一辆满载20t电石的挂车,在浙江滨江区江南大道信诚路口燃起熊熊大火。在事故路面上,沿路洒满了五六百米燃着的石头,这辆货车在雨中整整烧了一天,消防官兵对大火也束手无策,场面令人震撼。
长岭中心中学九(1)班化学兴趣小组对上述报道产生浓厚兴趣,为此进行探究,请你一起参入。
(查阅资料)电石[CaC2]是一种重要的化工原料,遇水即发生剧烈反应并放出大量的热,生成一种可燃气体[C2H2]和一种白色固体。
(提出问题)白色固体是什么物质?
(进行猜想)小明猜想白色固体可能是CaO、Ca(OH)2、Ca(HCO3)2或CaCO3中的一种。
(1)你认为小明猜想的依据是_____。
(2)小雨上网查阅后得知,白色固体不是Ca(HCO3)2,同时提出猜想中的CaO也不存在,你认为白色固体不是CaO的理由是(用化学方程式表示)_____。
(实验探究)小浩对白色固体讲行探究,请你帮忙完成。
实验方案 | 实验操作 | 实验现象 | 实验结论 |
小浩的方案 | 取少量白色固体于试管中,向其中加入稀盐酸 | 固体溶解,无气泡冒出 | _____ |
我的方案 | _____ | _____ | 白色固体是Ca(OH)2 |
(综合应用)结合上述事例,请你就易燃易爆物在贮存和运输时应注意的事项,提出一条合理建议: _____。
(拓展创新)氢氧化钙在空气中易变质,若变质后的固体中只含有碳酸钙和氢氧化钙,取变质后的固体17.4g加入到150g稀盐酸中恰好完全反应,生成二氧化碳的质量为4.4g。则变质后的固体中碳酸钙的质量分数为_____,反应后所得溶液中溶质的质量分数为_____(只写计算式)
2、探究“烧不坏的滤纸”实验。
(实验过程)将浸泡于适宜浓度的酒精溶液中的滤纸取出后点燃,发现酒精发生燃烧, 而滤纸不燃烧且完好无损。
(1)酒精(C2H6O)完全燃烧的化学方程式为____。
(2)从燃烧条件分析,滤纸未燃烧的原因是____。
(提出问题)该实验中,适合的酒精溶液溶质质量分数范围是多少?
(探究步骤)Ⅰ.按下表配制不同浓度的酒精溶液(已知:无水酒精的密度为 0.8 g/mL,水的密度为 1.0 g/mL)
实验编号 | 无水酒精体积/mL | 水体积/mL |
① | 10 | 5 |
② | 10 | 10 |
③ | 10 | 15 |
④ | 10 | 20 |
⑤ | 10 | 30 |
Ⅱ.用不同浓度的酒精溶液浸泡滤纸。
Ⅲ.用温度传感仪测定酒精燃烧时滤纸的温度数据,绘成图像如图。
(3)曲线①在接近 20 s 时,温度突然上升的主要原因是____。
(4)实验③大约在____s 时酒精燃尽,火焰熄灭。
(5)没有继续进行“无水酒精与水的体积比为 10:35” 实验的原因是____。
(实验结论)(6)根据图中信息分析:为确保实验成功,所用酒精溶液的溶质质量分数(ω)合理的范围是____(计算结果保留至小数点后 1 位)。
3、对比归纳是学习化学的重要方法。请你根据下列实验装置完成有关问题
(1)图1是探究燃烧的条件。由“①处的白磷不燃烧、②处的白磷燃烧”的现象,说明可燃物燃烧需满足的条件是_______________________。
(2)图2是探究铁生锈的条件。一周后试管A中铁钉生锈,试管B、C中铁钉无明显变化。对比试管______(选填字母序号,下同)中的实验现象,说明铁生锈一定要有水参加;对比试管__________中的现象,说明铁生锈必需水和氧气同时参加。
(3)图3是探究影响物质溶解性的因素。对比A试管和B试管,发现B试管中固体可溶, A试管中固体几乎不溶。该对比实验说明了影响物质溶解性的因素是__________________。某同学又补充了C试管所示实验,他想探究的影响因素是__________________。
(4)图4探究常温下镁与铁的金属活动性。分别向盛有等质量镁条与铁粉的两只试管中同时加入等质量等质量分数的稀盐酸,观察试管中金属表面产生气泡的快慢。请你指出其中的不合理之处:______________。
4、某校兴趣小组的同学,利用家庭常用的调味品味精做了以下实验。
查阅资料:味精能溶于水,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是,易溶于水,与硝酸银溶液不反应),另外还含有氯化钠,其它成分不考虑。
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是______(填字母)。
A 5mL B 10mL C 50mL D 100mL
(2)下图是配制过程,正确的操作顺序为______(填编号)。
(3)为测定味精中氯化钠的质量分数,进行如下实验:
①向所配制的50g溶液中加入硝酸银溶液充分反应,然后精确测定氯化银沉淀质量,从而计算该味精中氯化钠的质量分数。检验沉淀是否完全的方法是:静置后,在上层清液中加入______(填化学式)溶液,观察是否有沉淀生成。
②在其它操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制的溶液中,谷氨酸钠的质量分数______(填“偏大”、“偏小”或“无影响”),所测定的味精中氯化钠的质量分数______(填“偏大”、“偏小”或“无影响”)。
初中化学沪教版 (上海)九年级第一学期3.2 溶液课后测评: 这是一份初中化学沪教版 (上海)九年级第一学期3.2 溶液课后测评,共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
初中化学沪教版 (上海)九年级第一学期3.2 溶液同步训练题: 这是一份初中化学沪教版 (上海)九年级第一学期3.2 溶液同步训练题,共16页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
初中沪教版 (上海)3.2 溶液同步训练题: 这是一份初中沪教版 (上海)3.2 溶液同步训练题,共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。













