

2021-2022年度最新人教版九年级化学下册第九单元溶液期中复习试卷【完整版】
展开最新人教版九年级化学下册第九单元溶液期中复习试卷【完整版】
(考试时间:90分钟,总分100分)
班级:__________ 姓名:__________ 分数:__________
一、单选题(每小题3分,共计24分)
1、某温度下有一杯饱和的硝酸钾溶液,欲使其溶质的质量分数发生改变,下列操作可行的是
A.加入一定质量的硝酸钾晶体 B.升高温度
C.降低温度 D.恒温蒸发溶剂
2、根据下列实验方案进行实验,能达到实验目的的是
实验 方案 | ||||
实验 目的 | A.探究影响物质溶解性的因素 | B.探究可燃物燃烧的条件 | C.探究铁钉生锈是否有氧气参与 | D.验证质量守恒定律 |
A.A B.B C.C D.D
3、现有镁和氧化镁的混合物3.2g与100g一定溶质质量分数的稀硫酸恰好完全反应,反应后得到103.1g溶液,则该混合物中镁和氧化镁的质量比为
A.3:5 B.6:6 C.1:1 D.5:4
4、下列物质不能溶于水形成溶液的是
A.花生油 B.蔗糖 C.食盐 D.味精
5、如图所示,向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是
A.氢氧化钠 B.碳酸钙
C.硝酸铵和氢氧化钙 D.氯化钠
6、下列实验方案不能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 除去水中的异味和色素 | 用活性炭吸附 |
B | 鉴别硬水和软水 | 取样,分别加入肥皂水,振荡 |
C | 除去粗盐中的难溶性杂质 | 溶解,蒸发,结晶 |
D | 探究分子之间有空隙 | 将水、酒精各50mL倒入100mL量筒中 |
A.A B.B C.C D.D
7、将一定量的M加入一定量水中水的温度变化如图所示,则M可能是
A.生石灰 B.石灰石 C.硝酸铵 D.氯化钠
8、下列关于溶液的有关说法正确的是
A.利用洗洁精的溶解作用洗去碗上的油污 B.饱和溶液降温都能析出晶体
C.浓溶液都是饱和溶液 D.溶液都是均一、稳定的混合物
二、填空题(每小题4分,共计20分)
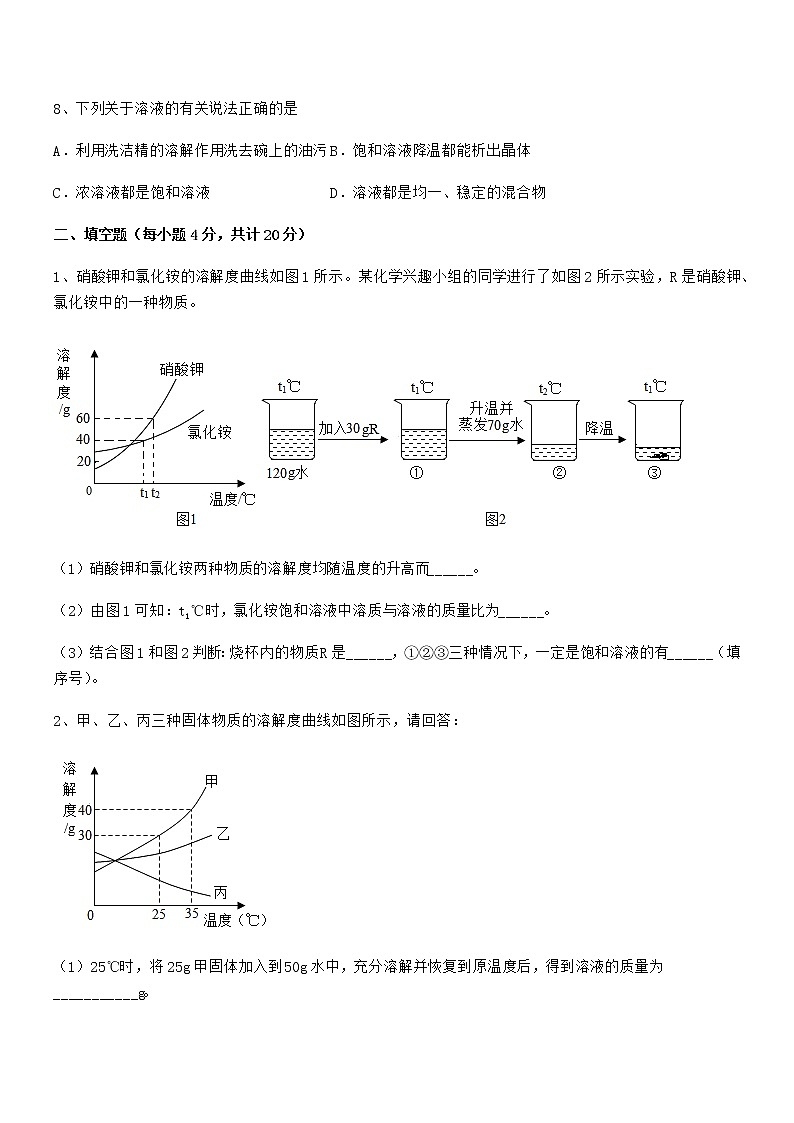
1、硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验,R是硝酸钾、氯化铵中的一种物质。
(1)硝酸钾和氯化铵两种物质的溶解度均随温度的升高而______。
(2)由图1可知:t1℃时,氯化铵饱和溶液中溶质与溶液的质量比为______。
(3)结合图1和图2判断:烧杯内的物质R是______,①②③三种情况下,一定是饱和溶液的有______(填序号)。
2、甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为___________g。
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是___________。
(3)现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是___________。(填字母序号)
(4)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数___________(填“变大”“变小”或“不变”)
3、生活与化学密切相关,请用你学到的知识回答:
(1)日前使用的煤、石油、天然气均为___________(填“可再生”或“不可再生”)能源。
(2)石油的综合利用是利用石油中各成分的___________不同,将它们分离,得到不同的产品。
(3)通常所说的煤气中毒是指____________(填化学式)引起的中毒。
(4)为保证安全,凡是可燃性气体,点燃前都要检验气体的________。
(5)煤发电时,将煤块粉碎成煤粉,其目的是_______。
(6)炭雕以活性炭为原料,对甲醛等有害气体有很强的__________作用,能净化室内空气。
(7)洗涤灵能洗去盘子上的油渍,原理是洗涤灵对食用油有____作用,它能增强乳浊液的___性。
4、用下图装置完成“粗盐中难溶性杂质的去除”实验请回答下列问题:
(1)粗盐提纯实验中的操作顺序为______(填序号),以及称量精盐并计算产率。
(2)操作③中玻璃棒搅拌的作用是______。
(3)操作③中,当观察到蒸发皿内出现______时,停止加热,让余热蒸干剩余液体。
5、如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)10℃,甲、乙、丙三种物质的溶解度由小到大的顺序______。
(2)在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液质量是______。
(3)若乙中混有少量甲,最好采用______的方法提纯乙(填“降温结晶”或“蒸发结晶”)。
(4)30℃时,把等质量的甲、乙、丙三种物质配成各自的饱和溶液,需水最多的是______。
(5)30℃时,甲乙丙三种物质的饱和溶液将其温度降到10℃时所得溶液的溶质质量分数由大到小的是______。
三、计算题(每小题4分,共计36分)
1、将13克的锌粒放入87.4克的稀盐酸中,当锌粒完全反应后:
(1)最多可以放出多少克的氢气?
(2)盐酸溶液中溶质的质量分数是多少?
2、配制500mL质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),需要氢氧化钠和水的质量各是多少?
3、实验室常用过氧化氢溶液与二氧化锰混合制取氧气.现将2.5g二氧化锰放入盛有50g过氧化氢溶液的锥形瓶中,完全反应后,放出气体的质量与反应时间的关系如图所示.
试求
(1)完全反应后生成的氧气的质量为______g.
(2)求过氧化氢溶液中过氧化氢的质量分数。
4、从一瓶氯化钾溶液中取出20克溶液,蒸干后得到2.8克的氯化钾固体。则这瓶溶液中溶质的质量分数为多少?(要求写出计算过程)
5、兴趣小组的同学取10克石灰石于烧杯中并慢慢加入盐酸,测得反应过程剩余固体质量与加入盐酸的质量关系如图所示(石灰石中的杂质不与盐酸反应也不溶于水)。请回答下列问题:
(1)石灰石中所含杂质的质量是 g。
(2)实验结束时生成二氧化碳的质量是多少?(写出计算过程,注意格式)
(3)当加入 g盐酸时,反应恰好停止。
6、向 100 克 16%的氢氧化钠溶液中,加入 100 克稀硫酸恰好完全反应,请计算:
(1)稀硫酸的溶质质量分数?
(2)反应结束后所得溶液的溶质质量分数?
7、为测定某石灰石样品中碳酸钙的质量分数,取25g该样品(杂质不参加反应也不溶于水),加入盛有146g稀盐酸的烧杯中,恰好完全反应,气体全部逸出,反应后烧杯内物质的总质量为162.2g.试回答:
(1)生成气体的总质量为___________g。
(2)该石灰石样品中碳酸钙的质量分数为___________(精确到0.1%)。
(3)所用稀盐酸的溶质质量分数为多少。
8、小樱同学在实验室进行有关浓硫酸溶液的实验,试剂瓶上的标签如下表所示。她从瓶中倒出20mL用于配制稀硫酸溶液。请计算:
浓硫酸溶液(H2SO4)500mL | |
溶质的质量分数 | 98% |
密度 | 1. 84 g/cm3 |
强腐蚀性,阴冷,密封储藏 | |
(1)这20mL浓硫酸溶液的质量为___________g。
(2)她将这20mL浓硫酸溶液与100mL水均匀混合,水的密度为1g/cm3所得稀硫酸溶液中溶质的质量分数是多少?(结果保留到小数点后一位)
9、新型冠状病毒是2019年底首次出现在人群中的一种全新病原体,目前对其所知仍然十分有限,通过对现有的流行病学资料研究分析,灭活新型冠状病毒的方法如下,该病毒对紫外线和热很敏感,56℃持续加热30分钟,以及使用紫外线灯照射30分钟以上,都可以有效的灭活病毒。另外,乙醚、75%的乙醇、含氯消毒液、过氧乙酸和氯仿等脂溶液也可有效的灭活病毒,不过氯己定不能灭活该病毒。现嘉祥县第四中学每天需要喷洒一定质量分数的过氧乙酸的消毒液,以许光皓,高晗,张明宇,晁子昂,李广杰,岳腾飞,孔凡泰,山耀凯,张潇益,朱振瀚组成的兴趣小组圆满完成任务。请你完成下面的计算,写出计算过程:
(1)100kg质量分数为0.5%的过氧乙酸消毒液中,过氧乙酸的质量为______kg。
(2)要配制100kg质量分数为0.5%的过氧乙酸消毒液,需要质量分数为10%的过氧乙酸溶液的质量是多少?
四、实验探究(每小题5分,共计20分)
1、在20℃环境中,制取干燥的二氧化碳气体,并验证二氧化碳气体与氢氧化钠溶液可以发生化学反应,设计如下探究实验。
(查阅资料)
(1)碳酸钠、水、二氧化碳可以化合生成碳酸氢钠(NaHCO3)。
(2)20℃,氢氧化钠、碳酸钠和碳酸氢钠的溶解度如下表所示:
物质 | 氢氧化钠 | 碳酸钠 | 碳酸氢钠 |
溶解度/g | 110 | 21.8 | 9.6 |
(定性探究)
(1)装置F中除导管外的玻璃仪器名称是____________。
(2)装置B中盛有碳酸氢钠溶液,目的是吸收装置A中挥发出的氯化氢气体。
(3)装置C的作用是_________,选择______(选填E、F)装置达到实验目的。
(4)在实验过程中装置D中观察到_______,说明二氧化碳和氢氧化钠溶液能发生化学反应。
(定量计算)
(5)装置D中氢氧化钠全部转化成碳酸钠时,理论上最多可以生成碳酸钠多少克________?
(6)当向装置D中通入足量的CO2时,可以将氢氧化钠全部转化为碳酸氢钠,实验过程中会析出的碳酸氢钠质量_________g(不考虑结晶水)。
2、某小组同学向盛有MnO2的试管中加入H2O2溶液,发现有大量气泡和水雾生成。小组同学对H2O2分解反应进行了深入的研究。
Ⅰ.探究水雾产生的原因
(进行实验)分别向三只试管中依次加入0.5gMnO2和30mL溶质质量分数不同的H2O2溶液,用温度传感器测定反应过程中溶液温度的变化,现象如下。
溶液 | 5%H2O2溶液 | 10%H2O2溶液 | 30%H2O2溶液 |
温度变化 | |||
水雾 | 有少量水雾 | 有较多水雾 | 有大量水雾 |
(解释与结论)
(1)在MnO2作催化剂的条件下,H2O2发生分解反应的化学方程式为_______,该反应_______热量(填“吸收”或“放出”)。
(2)H2O2溶液的溶质质量分数与反应中溶液温度变化的关系是_______。
(3)根据以上实验,可得出的结论是_______。
Ⅱ.探究影响H2O2分解反应速率的因素。
(实验方案)
试验编号 | H2O2溶液 | 蒸馏水 | 催化剂 | 温度/°C | |
溶质质量分数 | I'/ mL | I'/ mL | |||
① | 10% | 10 | 20 | 无催化剂 | 20 |
② | 10% | 10 | 20 | 0.5gMnO2 | 20 |
③ | 10% | 15 | x | 0.5gMnO2 | 20 |
(4)对比实验①②,目的是探究_______与H2O2分解反应速率是否有关。
(5)实验②③,目的是探究溶质质量分数与H2O2分解反应速率是否有关,则实验③中x是_______(填字母序号)。
a 15 b 30
(实验过程及分析)
在恒温恒容的密闭容器中完成以上实验,用压强传感器测量反应过程中容器内的气体压强随时间的变化,实验数据如下图所示。
(6)能证明溶质质量分数对H2O2分解反应速率有影响的证据是_______。
3、同学们在实验室用下图装置制取氧气。
(1)加热高锰酸钾时,试管口略向下倾斜的原因是 ______ 。
实验后,同学们发现沾有高锰酸钾的白抹布洗完晾干后变为棕褐色。
(查阅资料)
草酸溶液能将棕褐色物质除去。
(提出问题)
哪些因素能加快草酸除去棕褐色物质的速率?
(进行实验)
将均匀染有棕褐色的抹布剪成大小相同的小布条进行实验
实验 编号
| 实验1 20℃ 水
| 实验2 20℃ 0.5%草酸溶液 | 实验3 20℃ 0.25%草酸溶液 | 实验4 20℃ 0.125%草酸溶液 | 实验5 30℃ 0.25%草酸溶液 | 实验6 40℃ 0.25%草酸溶液 |
现象 | 颜色 没有褪去 | 70秒后 颜色褪去 | 98秒后 颜色褪去 | 150秒后 颜色褪去 | 51秒后 颜色褪去 | 40秒后 颜色褪去 |
(解释与结论)
(2)配制200g溶质质量分数为 0.5%的草酸溶液,需要草酸的质量为 ______ 。
(3)实验1的目的是 ______ 。
(4)证明升高温度能加快草酸除去棕褐色物质的速率,需要对比 ______ (填实验序号)。
(5)由实验2、3、4可以得出的结论是 ______ 。
(反思与评价)
(6)实验后,同学们查资料得知抹布上的棕褐色物质为二氧化锰,请你设计实验方案进行验证 ______ 。
4、2019 年 9 月 29 日,我省于山西省农产品国际交易中心举办了中国(山西)特色农产 品交易博览会。某校化学兴趣小组的同学们参观博览会时,对农药波尔多液产生了浓厚的兴趣,于是同学们对其中的硫酸铜溶液开展了实践活动。
探究过程:
(1)甲组用无水硫酸铜固体配制 100g质量分数为 8%的 CuSO4 溶液
①需硫酸铜固体的质量为______。
②某同学按如图所示步骤依次操作,其中操作错误的步骤是______(填字母序号), 会导致配得的硫酸铜溶液溶质质量分数______(选填“偏大”、“偏小”、“不变”)。
③操作 E 中用玻璃棒搅拌,其目的是______。
(2) 为比较相同浓度的 CuSO4 溶液和 FeCl3 溶液对过 氧化氢分解的催化效果,乙组同学设计了如图所示的创新实验。
实验序号 | 5%H2O2 溶液体积/ml | 分液漏斗中所加物质 | 实验现象 |
实验一 | 50 | 无 | 无明显现象 |
实验二 | 50 | 5ml 8%CuSO4 溶液 | 注射器活塞向右移动 |
实验三 | 50 | 5ml 8%FeCl3 溶液 | 注射器活塞向右移动 |
设计实验
①实验前,应该先______ 。
②在乙组的探究实验中,“实验一”起的作用是______ 。
③为定量比较两者的催化效果,可测量生成等体积气体所需的______。
深入探究
④为了证明 CuSO4 溶液是该反应的催化剂,还需:a.验证______; b.验证______。
总结与提升:
同一物质可以有很多用途。当我们徜徉于化学的海洋时,会发现诸多的奇珍异宝 ,让 我们一起来探究物质更多的用途吧。
2022年度最新人教版九年级化学下册第九单元溶液期末复习试卷(完整版): 这是一份2022年度最新人教版九年级化学下册第九单元溶液期末复习试卷(完整版),共15页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2022年最新人教版九年级化学下册第九单元溶液期中复习试卷【完整版】: 这是一份2022年最新人教版九年级化学下册第九单元溶液期中复习试卷【完整版】,共13页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2022年度最新人教版九年级化学下册第九单元溶液期中复习试卷最新: 这是一份2022年度最新人教版九年级化学下册第九单元溶液期中复习试卷最新,共16页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。












