
2021-2022年度最新人教版九年级化学下册第九单元溶液期中试卷(汇总)
展开这是一份2021-2022年度最新人教版九年级化学下册第九单元溶液期中试卷(汇总),共12页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
最新人教版九年级化学下册第九单元溶液期中试卷(汇总)
(考试时间:90分钟,总分100分)
班级:__________ 姓名:__________ 分数:__________
一、单选题(每小题3分,共计24分)
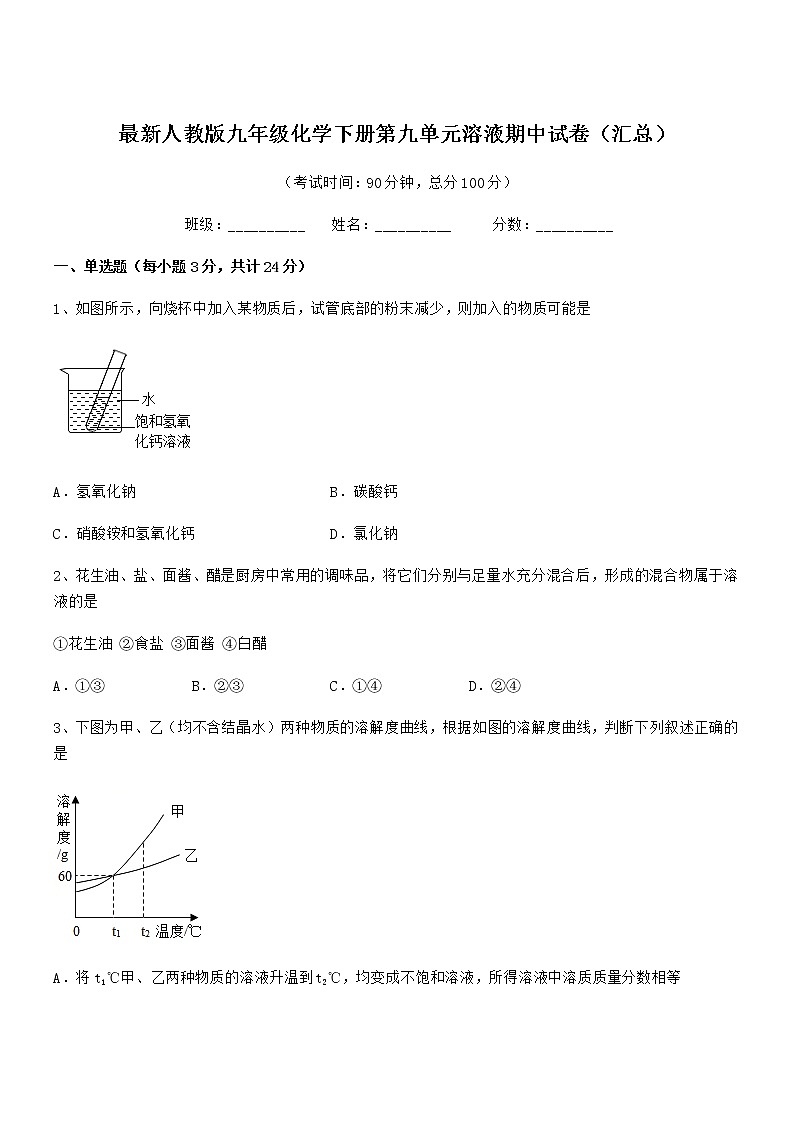
1、如图所示,向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是
A.氢氧化钠 B.碳酸钙
C.硝酸铵和氢氧化钙 D.氯化钠
2、花生油、盐、面酱、醋是厨房中常用的调味品,将它们分别与足量水充分混合后,形成的混合物属于溶液的是
①花生油 ②食盐 ③面酱 ④白醋
A.①③ B.②③ C.①④ D.②④
3、下图为甲、乙(均不含结晶水)两种物质的溶解度曲线,根据如图的溶解度曲线,判断下列叙述正确的是
A.将t1℃甲、乙两种物质的溶液升温到t2℃,均变成不饱和溶液,所得溶液中溶质质量分数相等
B.t1℃等质量的甲、乙溶液蒸发等质量的水,甲析出的晶体比乙多
C.甲中混有少量乙时,可以用蒸发溶剂的方法获得较纯净的甲
D.t2℃等质量的甲、乙的溶液降低温度到t1℃后,所得溶液的质量可能相等
4、下列说法正确的是
A.100g水溶解了30g某物质,则该物质的溶解度为30g
B.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
C.温度相同条件下,同一种物质的饱和溶液比不饱和溶液溶质的质量分数大
D.20℃,某物质的溶解度为20克,此时它的饱和溶液的溶质在整个溶液中的质量分数是20%
5、属于溶液的是
A.蒸馏水 B.矿泉水 C.泥沙水 D.油水
6、下列有关溶液的说法不正确的是
A.氯化钠溶于水就是钠离子和氯离子在水分子作用下均匀扩散到水中的过程
B.溶液加水稀释前后溶质的质量不变
C.同种溶质的饱和溶液与不饱和溶液通过改变条件可以相互转化
D.均一、稳定的液体一定是溶液
7、下列四个图像分别对应不同实验过程,其中不正确的是
A. 分别向等质量且足量的Mg片和Zn片中加入等质量、等浓度的稀硫酸
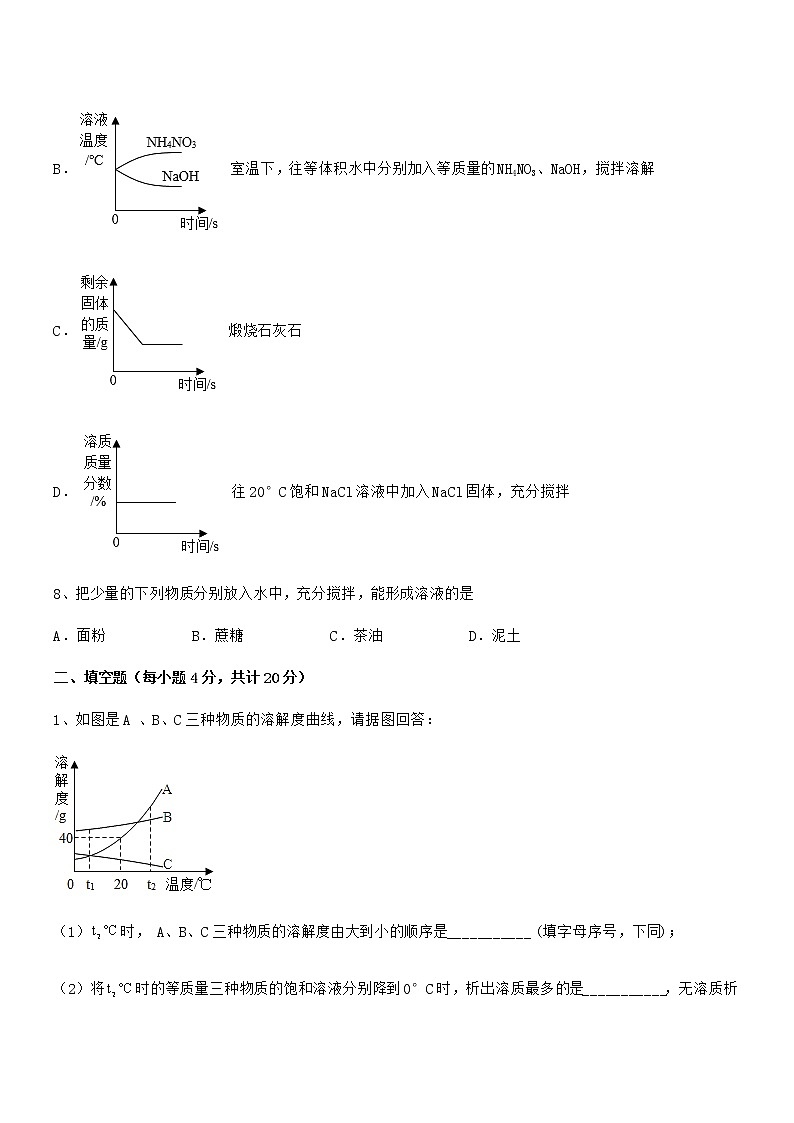
B. 室温下,往等体积水中分别加入等质量的NH4NO3、NaOH,搅拌溶解
C. 煅烧石灰石
D. 往20°C饱和NaCl溶液中加入NaCl固体,充分搅拌
8、把少量的下列物质分别放入水中,充分搅拌,能形成溶液的是
A.面粉 B.蔗糖 C.茶油 D.泥土
二、填空题(每小题4分,共计20分)
1、如图是A 、B、C三种物质的溶解度曲线,请据图回答:
(1)时, A、B、C三种物质的溶解度由大到小的顺序是___________ (填字母序号,下同);
(2)将时的等质量三种物质的饱和溶液分别降到0°C时,析出溶质最多的是___________,无溶质析出的是___________。
(3)20°C时,将30gA物质加入到50g水中并充分搅拌,形成溶液的质量为___________g;
(4)当A中含有少量B,为了得到纯净的A,可采用___________的方法。
(5)时,将等质量的A 、B、C三种物质配制成饱和溶液,所需水的质量由多到少的顺序是___________。
(6)将时A 、B、C三种物质的饱和溶液降低温度到时,这三种溶液中溶质质量分数由大到小的顺序是___________。
2、水与溶液在生产生活中有广泛的用途。
(1)如图为A、B两种物质的溶解度曲线如图所示,请根据图回答下列问题:
①甲的溶解度受温度的影响比乙的溶解度受温度影响______(填“大”或“小”);若甲中含有少量的乙,提纯甲应采用的结晶方法是______。
②t2℃时,将60g的甲、乙分别加入到100g水中,充分溶解,能形成的饱和溶液是______物质。
③将t1oC时甲、乙的饱和溶液升温到t2oC,所得溶液的溶质质量分数的关系是甲______(填“﹥”“﹤”“=”)乙。
(2)欲配制50 g溶质质量分数为0.9%的氯化钠溶液,需溶质质量分数为11%的氯化钠溶液的质量为______(列式即可)。
3、根据NaCl和KNO3的溶解度数据表,回答下列问题:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | |
(1)60℃时,KNO3的溶解度是_________g;
(2)10℃时,溶解度较大的是_________(选填“NaCl”或“KNO3”);
(3)下列分析正确的是_________(填字母)。
A.10℃时,不能够配制出溶质的质量分数为20.9%的KNO3溶液
B.20℃时,20g NaCl固体加入100g水,充分溶解后得到NaCl的不饱和溶液
C.20℃到30℃之间,能配制出溶质质量分数相等的NaCl饱和溶液和KNO3饱和溶液
D.将KNO3溶液经过某种操作后,析出KNO3晶体,过滤后所得溶液溶质的质量分数一定比原溶液小
4、甲、乙两种固体物质的溶解度曲线如下图所示。
(1)t1℃时,甲、乙饱和溶液中溶质的质量分数:甲______乙(填“>”“<”或“=”)。
(2)t2℃时,将60g乙物质放入100g水中,所得溶液中,溶质与溶剂的质量比为______(填最简整数比)。
(3)现有t2℃时,甲、乙两种物质的饱和溶液各100,将这两种溶液分别降温到t1℃,所得溶液中溶质的质量分数甲______乙(填“>”、“<”或“=”)。
(4)小明同学进行了如下图所示的实验:
上述实验过程中所得的溶液,属于不饱和溶液的是______(填序号),溶液中溶质的质量分数相同的是______(填序号)。
(5)喝了汽水以后,常常会打嗝。这说明随温度升高气体的溶解度______。
5、影响气体溶解度的外界因素有___________。
三、计算题(每小题4分,共计36分)
1、在生活中我经常食用食醋,根据所学知识回答下列问题。
(1)食醋中溶质醋酸的化学式___________。
(2)醋酸这种物质由___________构成。
(3)醋酸中碳元素的质量分数是___________。
(4)200 克溶质质量分数为 3%的醋酸溶液中碳元素的质量为___________。
2、现有80g 10%的硝酸钠溶液,若向上述溶液中加入20g水,则所得溶液中溶质的质量分数是多少?(写出计算过程)
3、将一定质量的大理石投入50g稀盐酸中,恰好完全发应,放出气体的质量与反应时间的关系如图所示,请回答下列问题:
(1)完全反应后生成二氧化碳气体的质量为___________g;
(2)所用盐酸溶液中溶质的质量分数?(写出计算过程,结果精确到0.1%)
4、新型冠状病毒是2019年底首次出现在人群中的一种全新病原体,目前对其所知仍然十分有限,通过对现有的流行病学资料研究分析,灭活新型冠状病毒的方法如下,该病毒对紫外线和热很敏感,56℃持续加热30分钟,以及使用紫外线灯照射30分钟以上,都可以有效的灭活病毒。另外,乙醚、75%的乙醇、含氯消毒液、过氧乙酸和氯仿等脂溶液也可有效的灭活病毒,不过氯己定不能灭活该病毒。现嘉祥县第四中学每天需要喷洒一定质量分数的过氧乙酸的消毒液,以许光皓,高晗,张明宇,晁子昂,李广杰,岳腾飞,孔凡泰,山耀凯,张潇益,朱振瀚组成的兴趣小组圆满完成任务。请你完成下面的计算,写出计算过程:
(1)100kg质量分数为0.5%的过氧乙酸消毒液中,过氧乙酸的质量为______kg。
(2)要配制100kg质量分数为0.5%的过氧乙酸消毒液,需要质量分数为10%的过氧乙酸溶液的质量是多少?
5、 “石头纸”是用沿海水产养殖中大量废弃贝壳制得的。为测定其中碳酸钙(杂质不溶于水也不与水反应)的含量,某同学进行了如下实验。取25.0 g样品粉碎放入烧杯中,加入一定质量分数的稀盐酸,所加稀盐酸的质量与生成气体的质量关系如图所示。
(1)根据图示观察,生成气体的质量是______克。
(2)计算“石头纸”中碳酸钙的质量分数。
(3)此稀盐酸的溶质质量分数?
(4)完全反应后烧杯内溶液的溶质质量分数是多少?(结果精确到0.1%)
6、某化学小组的同学进行硫酸铜溶液和氢氧化钠溶液相混合的实验。实验过程及数据如图所示:
(1)判断a为 。
(2)计算氢氧化钠溶液中溶质的质量分数为多少?
7、在农业生产上,常需要用质量分数为16%的氯化钠溶液选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?
8、中华文化源远流长,早在西汉时期《淮南万毕术》一书中就有“曾青得铁则化为铜”的记载,这是我国现代“湿法炼铜”的先驱。利用此原理,向160kg含硫酸铜的废液中加入足量的铁粉,得到金属铜6.4kg。请计算废液中硫酸铜的溶质质量分数。
9、某浓盐酸瓶上的标签如表所示,则:
浓盐酸(HCI)500mL | |
浓度(质量分数) | 36% |
密度 | 1.2g/cm3 |
(1)该瓶浓盐酸的质量为______克。
(2)取100mL 该浓盐酸与500 mL水均匀混合,所得稀盐酸的质量分数是多少?(结果精确到0.01%)
(3)欲配制100g质量分数为3.6%的稀盐酸,需该浓盐酸质量为多少克?
四、实验探究(每小题5分,共计20分)
1、某化学兴趣小组探究硝酸铵、氯化钙、氯化钠三种物质溶于水过程中的热量变化。
(药品器材)水、硝酸铵、氯化钙、氯化钠;烧杯、药匙、玻璃棒、量筒、温度计等。
(实验探究)三种物质各取1药匙于烧杯分别溶于水,另还有一个烧杯只加水,用温度计测量液体温度,并记录有关数据如下:
实验 | 水的体积 | 所加物质 | 测量液体温度(℃) |
实验1 | 50 mL | 硝酸铵 | 15 |
实验2 | 50 mL | 氯化钙 | 28 |
实验3 | X | 氯化钠 | 21 |
实验4 | 50 mL | 无 | 22 |
(数据分析)
(1)表中X为________mL。
(2)比较实验2与实验4,可获得的结论是______。
(3)如果要生产一种“冰袋”用于冷敷,上述三种物质中最合适的是_______。
(反思评价)
(4)经讨论认为本实验操作中存在缺陷,它是_____(可多选)。
A 实验操作过程没有采取较为严格的保温措施
B 加入物质的质量可能不相等
C 加入物质的种类不一样
2、某化学兴趣小组的同学准备探究影响化学反应速率的因素有哪些,同学们收集资料后发现:
(1)镁条在空气中可以剧烈燃烧,铁丝在氧气中能够剧烈燃烧,金在高温下也不能燃烧,说明影响反应速率的因素之一是______。分析可知,这三种金属活动性由弱到强的顺序是______。铁丝在空气中不能燃烧,在氧气中可以燃烧,说明影响反应速率的因素之二是______。
(2)同学们又利用压强传感器来探究影响铁和稀盐酸反应速率的因素,实验装置和测得的数据如图所示:
①锥形瓶内发生反应的化学方程式为______,基本反应类型为______。
②图中表示铁片与稀盐酸反应的曲线是______(填“a”或“b”),根据曲线得出的结论是______。
③实验测得的反应达到终点时,压强相等。若取少量锥形瓶中剩余溶液加入紫色石蕊溶液,均无明显现象,说明两锥形瓶内的______(填化学式)一定没有剩余。
附加问:
(3)同学们查阅资料发现工业上运输浓硫酸常用铁罐车,于是提岀疑问:铁能与浓硫酸反应吗?请参与实验设计完成相关探究。
实验步骤 | 实验现象 |
①将一打磨过的铁片放入硫酸铜溶液中 | ______ |
②另取一打磨过的铁片先放入浓硫酸中,一段时间后将铁片取出,用水冲洗干净后,放入硫酸铜溶液中,观察现象 | 在硫酸铜溶液中,铁片表面没有明显现象 |
(4)①常温下铁能与浓硫酸反应吗?______(填“能”或“不能”)
②运输浓硫酸的铁罐车能否用水冲洗?请回答并分析原因______。
3、某化学探究小组的同学在学习《溶液》这一单元时,进行了一系列探究活动并进行相关归纳,请你作为其中一员,参与他们的探究。
(活动一)梦凡对“物质溶于水是否都能形成溶液?”进行探究。选取生活中常见物质,仪器任选。选取的物质有:①食盐; ②花生油; ③面粉; ④泥土。
(1)通过该探究活动,梦凡得出结论:有的物质放入水中能形成溶液。如上述物质中______(填序号)放入水中就能形成溶液。
(活动二)苏苏以“物质溶解时热量的变化”为课题进行探究,其实验装置如下:
(2)若苏苏向小试管中加入一定量的硝酸铵固体(NH4NO3),完全溶解后,可观案到U形管内a端液面_____(填“低于”、“高于”或“相平”)b端液面。
(活动三)思敏为“证明影响物质溶解快慢的因素”为课题进行探究,她设计了如下部分实验:
(3)通过实验①②的对比,可得出的实验结论是___________。
(4)若要证明物质溶解的快慢与固体颗粒大小有关,需增加实验④与实验③进行对比,请帮思敏画出实验④的图示。 _______
4、某小组在学习“二氧化碳实验室制取的研究”课题时,探究了二氧化碳的收集方法.
(查阅资料)1.通常状况下,1体积水约溶解1体积二氧化碳,所得溶液的pH约为5.6,pH越小,二氧化碳在水中溶解越多.
2.石灰石中的杂质既不和盐酸反应,也不溶于水。
(提出问题)二氧化碳能不能用排水法收集?
(设计实验)
实验一:在通常状况下,测定二氧化碳溶于水所得溶液的pH,判断二氧化碳在水中溶解的体积,如图:
(1)甲装置中反应的化学方程式 ________________________.
(2)检查甲装置气密性的方法是 关闭活塞和止水夹K1,打开K2、K3双手握住锥形瓶,观察到____________________________,说明装置气密性良好。
(3)实验时,需先将甲装置中的空气排尽.其操作是打开止水夹 K1,关闭止水夹 K2,打开活塞,滴加稀盐酸至空气排尽。检验空气排尽的方法是 ____________________.
(4)关闭 K1,打开 K2、 K3待丙装置中收集半瓶气体时,关闭K2、 K3充分振荡丙装置,分别测得丙、丁瓶装置中溶液的pH为5.5和6.5。分析可知,溶解的二氧化碳体积丙装置中 ________________(填“大于”或“等于”或“小于”)丁装置中.实验中,乙装置的作用是 ____________________________.
(5)实验结束后,装置甲反应后溶液中溶质除了氯化钙还有没有其他物质?请设计实验证明你的猜想(写出实验方法、现象和结论)
实验方法:_____;
现象:_____;
结论:_____。
(6)实验二:用二氧化碳数字传感器测得收集的气体中二氧化碳体积分数.如图是收集的气体中二氧化碳体积分数随时间变化的关系图,从图中能得到哪些信息:
① ________________________,
② ________________________.
(结论反思)由实验一、二分析,改进实验装置,二氧化碳能用排水法收集.能降低二氧化碳在水中溶解性的措施③____________,④________
相关试卷
这是一份2021年度最新人教版九年级化学下册第九单元溶液期中复习试卷【汇总】,共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
这是一份2021-2022年最新人教版九年级化学下册第九单元溶液期中试卷汇总,共13页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
这是一份2021-2022年最新人教版九年级化学下册第九单元溶液期中复习试卷汇总,共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。












