

2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期中试卷(必考)
展开
这是一份2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期中试卷(必考),共11页。试卷主要包含了单选题,填空题,计算题等内容,欢迎下载使用。
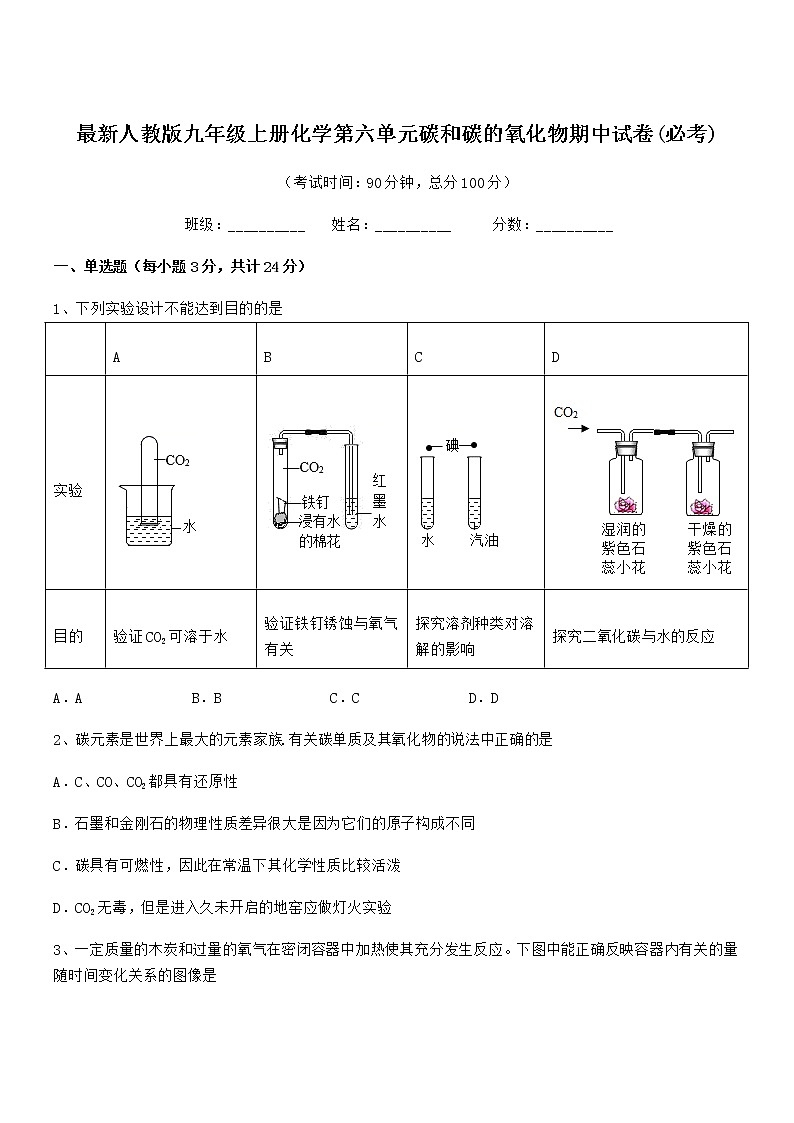
最新人教版九年级上册化学第六单元碳和碳的氧化物期中试卷(必考)(考试时间:90分钟,总分100分)班级:__________ 姓名:__________ 分数:__________一、单选题(每小题3分,共计24分)1、下列实验设计不能达到目的的是 ABCD实验目的验证CO2可溶于水验证铁钉锈蚀与氧气有关探究溶剂种类对溶解的影响探究二氧化碳与水的反应A.A B.B C.C D.D2、碳元素是世界上最大的元素家族.有关碳单质及其氧化物的说法中正确的是A.C、CO、CO2都具有还原性B.石墨和金刚石的物理性质差异很大是因为它们的原子构成不同C.碳具有可燃性,因此在常温下其化学性质比较活泼D.CO2无毒,但是进入久未开启的地窑应做灯火实验3、一定质量的木炭和过量的氧气在密闭容器中加热使其充分发生反应。下图中能正确反映容器内有关的量随时间变化关系的图像是A. B.C. D.4、下列各组气体中,不能用燃着木条区分的是A.氧气和空气 B.二氧化碳和氮气C.氢气和空气 D.氮气和氧气5、下列物质的鉴别或除杂方法正确的是A.用燃着的木条鉴别氮气与二氧化碳 B.用观察的方法鉴别稀盐酸和硫酸铜溶液C.用点燃的方法除去二氧化碳中混有的一氧化碳 D.用灼烧的方法除去铜粉中的碳粉6、下列实验得出的结论,正确的是A.氧气已集满 B.CO2密度比空气大,不可燃也不助燃C.该实验可以验证质量守恒定律 D.二氧化碳能与水反应7、下列不属于二氧化碳用途的是A.做燃料 B.做制冷剂 C.做气体肥料 D.用于人工降雨8、下列有关碳和碳的化合物说法错误的是A.金刚石、C60是由碳元素组成的单质 B.用石墨制取金刚石,发生的是化学变化C.CO2与CO的组成元素相同,化学性质也相同 D.在一定条件下,CO2与C可以相互转化二、填空题(每小题4分,共计40分)1、中国人民在抗击新冠肺炎中的表现得到世界的高度肯定。“战疫情”中,也涉及到许多化学知识。(1)在抗击“新冠肺炎”疫情战斗中,人们釆取了一系列行之有效的措施。①口罩是防疫必备品,其中医务工作者所戴的一种特殊口罩中含有活性炭,这利用了活性炭______性。②测量体温是防控的重要环节。家庭常备体温计中的液态金属是______(填化学式)。③利用过氧乙酸溶液消毒。过氧乙酸溶液中通常含有过氧化氢、醋酸(与稀盐酸化学性质类似)等物质,向其中加入下列物质,能产生气体的是______。A.C B.Fe C.NaCl D.MnO2(2)“84消毒液”是一种以次氯酸钠(NaC1O)为主要成分的含氯消毒剂,可有效灭活新冠病毒。“84消毒液”禁止与洁厕灵(有效成分盐酸)混合使用,原因是二者反应生成氯化钠、水和一种有毒的气体单质,该反应的化学方程式为_______。(3)75%的酒精能有效灭活新冠病毒,但酒精不适合大面积喷洒消毒,原因是______。(4)新冠肺炎病人因肺功能损害,急需吸氧,正常情况下,供氧为5L/min,但危重症病人往往需要50L/min,这会造成医院氧气供给严重短缺,以氧气钢瓶、杜瓦瓶、液氧槽车三种方式为医院运送医用氧。通常情况下,氧气钢瓶中盛放的是______态氧(填(“液”或“固”);一个常温150大气压40L的氧气钢瓶充满氧气时,相当于常温1大气压下氧气______L,这些氧气只够一个危重症病人使用____小时。(5)钢铁厂制氧气的方法是将空气在低温下液化,利用空气各组分沸点的差别,进行分馏而得氧,则分馏时首先得到______(填氮气或氧气,填化学式),钢铁厂的氧气主要用于炼钢,其作用是______。(6)检测新冠病毒的重要方法是核酸检测。核酸(DNA或RNA)是病毒的遗传物质,任何物种都有独一无二的核酸序列。用聚合酶链式反应(PCR)进行新冠病毒核酸检测的过程如下图所示,检测步骤主要包含提取基因片段,逆转录为DNA,扩增放大,从目前技术方法的特异性和敏感性来看,第二代实时荧光定量PCR技术相对是最佳的。下列相关说法中正确的是_______A.病毒将在灭活后提取基因片段B.核酸检测结果百分之百准确C.新冠病毒的RNA中有特征遗传物质2、一氧化碳可以将氧化铜还原成铜,反应的化学方程式为___________;在一定条件下,CO2与H2以质量比为11:2反应可生成甲烷。与该反应类似,在一定条件下,CO2与H2反应也能生成甲醇(CH4O)。生成甲醇时参加反应的CO2与H2的质量比为___________。3、我国科学家以二氧化碳、氢气为原料,通过十步反应制得淀粉[化学式为(C6H10O5)n],实现了二氧化碳到淀粉的人工合成。(1)二氧化碳、氢气、淀粉三种物质中,属于单质的是______。(2)关于二氧化碳合成淀粉的意义,下列说法正确的是______(填序号)。a.能够消耗二氧化碳,将有助于减少温室效应b.能够合成淀粉,将有利于解决粮食短缺问题4、按下图所示装置探究二氧化碳的性质并填空:(1)A中的实验现象说明具有的化学性质是______。(2)写出B中反应的化学方程式______。(3)C装置中干石蕊纸花不变色,湿石蕊纸花由紫色变红色的原因是______。5、小明同学去九仙山旅游时,用瓶装了一些山上的泉水,带回实验室。在老师的指导下,按下列流程进行实验制取蒸馏水。请回答下列问题:(1)取水后加入明矾的作用是________。(2)过滤操作结束后发现所得滤液仍浑浊,其原因可能是_________(答一条)。(3)向滤液中加入活性炭,利用其________性,除去水样中的色素和异味。(4)消毒剂高铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为________价。(5)向制取的蒸馏水中加适量肥皂水并搅拌,现象是________。6、气体的制取及其性质实验是初中化学的基础实验,回忆有关知识,根据下图回答:(1)检查装置A的气密性的方法是__________,说明气密性良好。(2)实验室可以利用装置A和F制备并收集CO2,石灰石应放在__________;装置的连接顺序a→___________;实验过程中若需要暂时停止反应,最便捷的操作是__________。(3)实验室里,可使用B装置加热氯化铵和氢氧化钙固体混合物制备氨气,收集氨气不选择装置D和装置E,由此推测氨气的物理性质是__________。(写一条)7、在A-H八种物质中,选择符合题意的物质并用字母填空。A.氧气 B.氮气 C.二氧化硫 D.二氧化碳 E.氦气 F.氢气 G.四氧化三铁 H.氯化钠(1)由离子构成的是_______ ;(2)可供给人呼吸的气体是_______ ;(3)可制硝酸和氮肥的是_______ ;(4)有刺激性气味的气体是_______ ;(5)能使澄清石灰水变浑浊的气体是_____;(6)可以填充探空气球的是______;(7)用作电光源的是________ ;(8)属于黑色固体的是___________ 。8、碳是人类接触得最早、利用得最多的元素之一。(1)碳元素在元素周期表中的信息如图甲所示。碳原子的相对原子质量是:__________。(2)第22届国际足联世界杯将于2022年在卡塔尔举行,小小足球牵动着亿万球迷的心。化学中有一种形似足球的物质(如图乙),其化学式为__________,该物质由__________(填“原子”或“分子”)构成。(3)炭雕(如图丙)是活性炭成型技术与传统雕刻工艺的完美结合。因为活性炭有__________的结构,具有__________能力,所以既可以净化室内空气,又可以美化居住环境。(4)图丁表示的物质的名称是__________,是自然界最__________的物质。(5)图乙、丁、戊表示的物质都是碳元素组成的单质,但其物理性质存在较大差异,原因是____________。9、水是生命之源,也是人类宝贵的自然资源。请回答下列问题:(1)生活中为降低水的硬度并杀灭水中的病原生物,可采用的方法是___________。(2)实验室中常通过___________的操作来除去水中不溶性的杂质,该操作中玻璃棒的作用是___________。(3)在天然水净化过程中,人们常用活性炭去除异味和色素,这是利用活性炭的___________性,此外还常加入二氧化氯进行杀菌和消毒,试写出二氧化氯的化学式:___________。(4)下图为电解水反应过程的微观模型图。该反应的化学方程式是___________;通过微观模型图可以看出,该反应前后___________(填具体微粒名称)的种类、数目都没有发生改变。10、二氧化碳制冰技术。在8座冰上场馆中,均选用了二氧化碳跨临界直接制冷系统。其制冷原理是液态二氧化碳蒸发_________热量,使环境温度降低。整个制冷系统的碳排放趋近于零,该技术有利于控制_________的加剧。空气中二氧化碳的体积分数约为__________。三、计算题(每小题4分,共计36分)1、某兴趣小组为测定如图1某品牌碳酸钙药片中碳酸钙的含量,他们取了4片药片,捣碎后,加入稀盐酸充分反应,产生二氧化碳和所用稀盐酸的质量关系如图2(杂质不含钙元素也不参与反应)。请回答:(1)计算每片药片中碳酸钙的质量。(2)该药片中钙元素含量是 ___________(“真实”或“虚假”)的。2、化学兴趣小组为了测定石灰石样品中碳酸钙的质量分数,取25g石灰石样品放在烧杯中,然后向其中逐滴加入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参加反应).随着反应进行,加入稀盐酸的质量与反应得到气体的质量变化关系如图所示。请计算样品中碳酸钙的质量分数是多少?(写出计算过程)3、学习小组的同学在实验室中制取二氧化碳,称取12g大理石样品,将80g稀盐酸分4次加入样品中(假设杂质不参与反应,也不溶于水),测得实验数据如下:次数第1次第2次第3次第4次加入稀盐酸的质量/g20202020剩余固体的质量/g9632请完成下列分析与计算:(1)12g大理石样品中碳酸钙的质量为___________g。(2)实验结束时制得二氧化碳的质量为多少?4、化学兴趣小组成员为了测定大理石中碳酸钙的质量分数分别进行了下图的实验。(杂质不溶于水也不 与酸反应,过滤后滤渣损失忽略不计,氯化钙易溶于水)(1)过滤时玻璃棒的作用是 ___________。(2)大理石中碳酸钙的质量分数是 ___________。(3)化学兴趣小组测定大理石的纯度过程中,生成二氧化碳的质量是多少?(写出计算过程)(4)实验过程中小红同学出现了以下问题。①过滤时得到的滤液浑浊,原因可能是___________ ;(只写一种)②过滤所得的滤渣未烘干就直接称量,这一操作会导致该样品中碳酸钙的质量分数计算结果___________。(选填“偏 大”、“不变”或“偏小”)5、石灰石的主要成分是碳酸钙。为了测定某石灰石中碳酸钙的质量分数,小邻同学进行了如下实验:称取5g石灰石固体放在烧杯里,然后往烧杯中加入足量的稀盐酸45g,充分反应后,称得烧杯中剩余物为48.68g(假设其它物质不与盐酸反应),计算:(1)产生二氧化碳的质量为________g;(2)计算该石灰石中碳酸钙的质量分数______。6、某化学兴趣小组发现一份石灰石样品,为测得该石灰石样品中碳酸钙的质量分数,兴趣小组同学进行了如下实验,过程如图所示:(杂质不溶于水也不与盐酸反应)。(1)反应中生成二氧化碳的质量为___________。(2)该石灰石样品中碳酸钙的质量。(根据化学方程式计算)7、某补钙剂的主要成分是碳酸钙,欲测定补钙剂中碳酸钙的质量分数,某同学进行了如图的操作:(已知:其他成分不参与反应且不溶于水)(1)生成CO2的质量为 ______g。(2)计算该补钙剂中碳酸钙的质量分数。(根据化学方程式计算,写出完整步骤)8、某学校的学习小组对当地的石灰石矿区进行调查,欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16 g,把80 g稀盐酸分四次加入,实验过程中所得数据如下表。(已知石灰石样品中含有的二氧化硅等杂质不溶于水,也不与稀盐酸反应)加入次数加入稀盐酸的质量/g剩余固体的质量/g1201122063202.4420n根据实验数据计算:(1)表中n的数值为___________。(2)样品中碳酸钙的质量分数是___________。(3)取50 kg这种石灰石高温煅烧,可得含杂质的氧化钙多少千克?9、鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,取12.5g干燥的鸡蛋壳,捣碎,放在烧杯中,然后向其中滴加某浓度的稀盐酸,滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(鸡蛋壳中除CaCO3外的其他成分都不溶于水,也不与稀盐酸反应)。试计算:(1)产生CO2的质量为___________ g;(2)该鸡蛋壳中CaCO3的质量分数。
相关试卷
这是一份2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期中复习试卷【精选】,共11页。试卷主要包含了单选题,填空题,计算题等内容,欢迎下载使用。
这是一份2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期中试卷(精品),共10页。试卷主要包含了单选题,填空题,计算题等内容,欢迎下载使用。
这是一份2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期中复习试卷A4版,共11页。试卷主要包含了单选题,填空题,计算题等内容,欢迎下载使用。









