





高中化学苏教版选修4 化学反应原理第二单元 溶液的酸碱性课文配套ppt课件
展开学习目标1、熟悉滴定管的构造和使用2、能用中和滴定原理进行计算3、会进行中和滴定操作4、会误差分析5、了解指示剂的选择
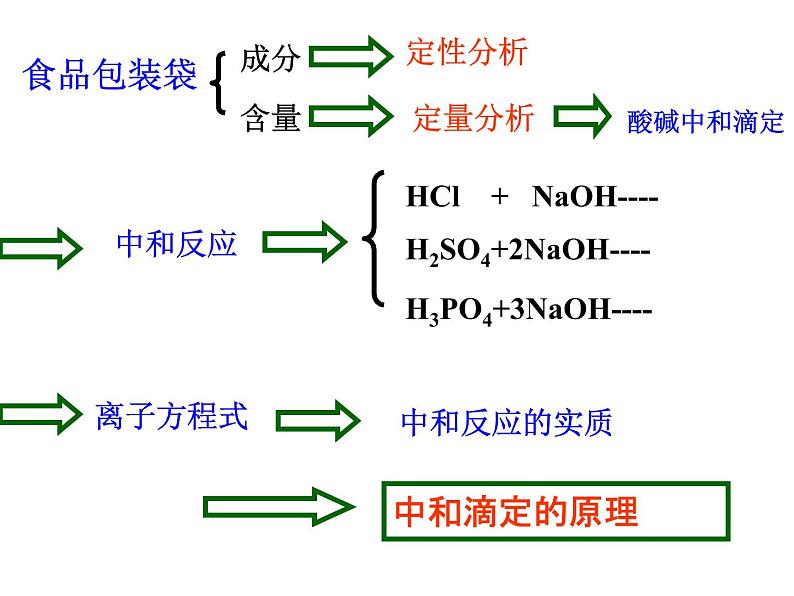
实验室有一瓶盐酸,由于长时间的放置,标签掉落。现请设计实验方案测出其准确浓度 。
你们所设计的方案哪种最好?
HCl + NaOH----
H2SO4+2NaOH----
H3PO4+3NaOH----
一、酸碱中和滴定的原理
酸碱恰好完全反应时,酸提供的n(H+)等于碱提供的n(OH-)即: n(H+)=n(OH-)
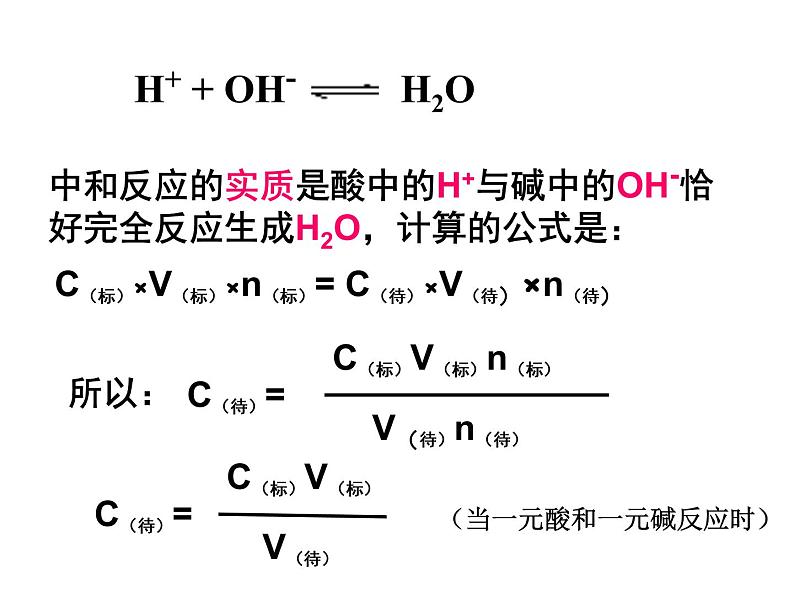
中和反应的实质是酸中的H+与碱中的OH-恰好完全反应生成H2O,计算的公式是:
C(标)×V(标)×n(标)= C(待)×V(待)×n(待)
H+ + OH- H2O
(当一元酸和一元碱反应时)
用已知物质的量浓度的酸(或碱)来测定未知物质的量浓度的碱(或酸)的方法叫酸碱中和滴定。
注:原理简单,在实验中,要减少误差,还需用精密的仪器和严格的实验操作。
如何准确量取一定体积的未知浓度盐酸? 如何测出所消耗NaOH标准溶液的体积?
【思考】 有一支25ml酸式滴定管内盛有溶液,液面在10.00ml刻度处,当管内溶液全部排出时,所得溶液的体积是_________。
这两种容器哪种更适合于实际操作?
①酸式滴定管(酸性、中性、强氧化性溶液)
②碱式滴定管(碱性溶液)
不能放碱液、水解呈碱性的溶液、氢氟酸
不能盛放酸性溶液和强氧化性溶液
3、酸碱中和滴定的仪器和试剂
①刻度:由上而下,“0”在上。
②量程:不能测定超出量程范围和使用温度的体积。
④使用时不能有气泡,否则会带来误差。
③准确程度:0.01ml
⑤酸式滴定管用玻璃管连接,碱式滴定管用橡皮管连接。
怎么知道所加的氢氧化钠溶液与盐酸恰好反应完全呢?
强酸滴定强碱常用酚酞、甲基橙作指示剂
强碱滴定强酸常用酚酞作指示剂
强酸滴定弱碱常用甲基橙作指示剂
通过指示剂颜色的变化确定滴定终点,故要求变色灵敏、明显。
记忆口诀:强酸滴碱甲基橙,强碱滴酸用酚酞
苏教版 (2019)选择性必修1第二单元 溶液的酸碱性试讲课课件ppt: 这是一份苏教版 (2019)选择性必修1第二单元 溶液的酸碱性试讲课课件ppt,共31页。PPT课件主要包含了课前导入,滴定管,小专题,滴定实验中的误差分析,误差分析的方法,作业布置,预习盐类水解等内容,欢迎下载使用。
化学苏教版 (2019)第二单元 溶液的酸碱性评优课课件ppt: 这是一份化学苏教版 (2019)第二单元 溶液的酸碱性评优课课件ppt,共60页。PPT课件主要包含了内容索引,酸碱中和滴定,中和滴定误差分析,课时对点练,锥形瓶,装待测液,2滴定,控制活塞,内溶液颜色变化,摇动锥形瓶等内容,欢迎下载使用。
苏教版 (2019)选择性必修1第二单元 溶液的酸碱性教学演示课件ppt: 这是一份苏教版 (2019)选择性必修1第二单元 溶液的酸碱性教学演示课件ppt,共60页。PPT课件主要包含了酸碱中和滴定,中和滴定误差分析,课时对点练,锥形瓶,装待测液,2滴定,控制活塞,内溶液颜色变化,摇动锥形瓶,不变回原色等内容,欢迎下载使用。













