

2021学年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷最新
展开最新人教版九年级化学下册第十单元 酸和碱期末复习试卷最新
(考试时间:90分钟,总分100分)
班级:__________ 姓名:__________ 分数:__________
一、单选题(每小题3分,共计24分)
1、三甲基一氯硅[(CH3)3SiCl]是一种生产有机硅化合物的原料,遇明火或氧化剂会引起爆炸,在空气中燃烧生成一氧化碳、二氧化碳、二氧化硅和氯化氢,与水接触可产生雾状盐酸。则下列说法错误的是
A.保存三甲基一氯硅时应密封防水
B.三甲基一氯硅水溶液pH小于7
C.三甲基一氯硅分子由3个碳原子、9个氢原子、1个硅原子和1个氯原子构成
D.扑灭三甲基一氯硅引发的着火,应使用二氧化碳、干粉灭火剂,并用弱碱性水处理
2、下列化学方程式中书写正确的是
A.铁丝在氧气中燃烧:4Fe+3O2 2Fe2O3
B.铁和盐酸混合:2Fe+ 6HC1=2FeCl3+3H2↑
C.检验二氧化碳:CO2 +Ca(OH)2=CaCO3 + H2O
D.用稀硫酸除去铁锈:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
3、下列实验操作或图标正确的是
A.稀释浓硫酸
B.蒸发食盐水
C.储存和运输浓盐酸的容器上贴的图标
D.禁止吸烟
4、下列实验现象的描述正确的是
A.二氧化碳通入紫色石蕊溶液中,溶液变红,再加热,溶液变为无色
B.红磷在空气中燃烧,产生大量的白烟
C.铁在空气中燃烧,火星四射,生成黑色固体
D.镁条在空气中燃烧产生耀眼的白光,生成白色固体氧化镁
5、逻辑推理是学习化学的重要思维方法,以下推理正确的是
A.离子都是带电粒子,则带电粒子一定是离子
B.单质由同种元素组成,则由同种元素组成的纯净物一定是单质
C.中和反应生成盐和水,则能生成盐和水的反应一定是中和
D.同种元素的质子数相同,则质子数相同的微粒一定是同种元素
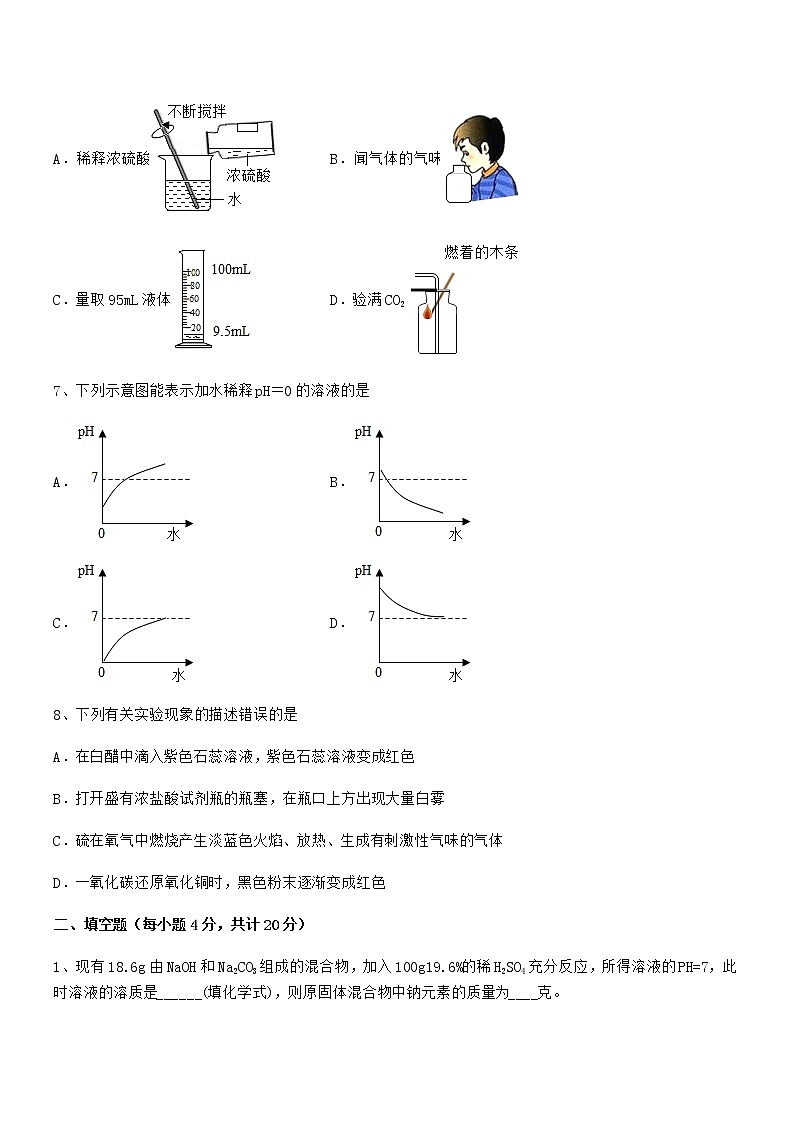
6、规范的实验操作是进行科学实验的重要保障。下列实验操作中,正确的是
A.稀释浓硫酸 B.闻气体的气味
C.量取95mL液体 D.验满CO2
7、下列示意图能表示加水稀释pH=0的溶液的是
A. B.
C. D.
8、下列有关实验现象的描述错误的是
A.在白醋中滴入紫色石蕊溶液,紫色石蕊溶液变成红色
B.打开盛有浓盐酸试剂瓶的瓶塞,在瓶口上方出现大量白雾
C.硫在氧气中燃烧产生淡蓝色火焰、放热、生成有刺激性气味的气体
D.一氧化碳还原氧化铜时,黑色粉末逐渐变成红色
二、填空题(每小题4分,共计20分)
1、现有18.6g由NaOH和Na2CO3组成的混合物,加入100g19.6%的稀H2SO4充分反应,所得溶液的PH=7,此时溶液的溶质是______(填化学式),则原固体混合物中钠元素的质量为____克。
2、化学就在我们身边,与我们的生活有着密切的联系,请回答以下问题。
(1)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放,检测废水呈碱性的简单方法是_____。
(2)用适量盐酸可以将热水瓶胆壁上的水垢[主要成分是Mg(OH)2和CaCO3]除去。
请用化学方程式说明去垢的原理:①_____;②_____;
(3)在清洗餐具时常加入少量洗涤剂,这是因为洗涤剂具有_____功能;碱性洗发水易去油污,但对头发有损坏,于是人们通常用洗发水洗净头发后,再用护发素护理,由此可知护发素的pH_____7.(填“>”、“<”或“=”)
(4)海水“晒盐”主要发生_____(填“物理”和“化学”)变化。
(5)用于治疗胃酸过多的药物中常含有Al(OH)3等碱性物质,用化学方程式表示Al(OH)3治疗胃酸过多症的原理:_____;
3、填写下表
实验内容 | 反应的现象 | 结论(反应的化学方程式) |
向硫酸铜溶液中加入几滴氢氧化钠溶液 | ________ | _________ |
再向上述试管中加入稀盐酸 | ________ | _________ |
4、向紫色石蕊溶液中通入CO2,溶液变为______色,反应的方程式是__________,加热后溶液呈______色,反应的方程式是_________;盛装石灰水的瓶壁上常有一层白膜,这层白膜的成分主要是________,要洗净表面的白膜要用__________,其反应的化学方程式可表示为________。
5、下列物质是由H、C、O、Ca、Cl、Fe中的几种元素组成它们是初中化学常见的物质,按如图所示装置进行实验。当胶头滴管中的液体滴入瓶中,U型管中的液面发生了明显变化,请分别写出符合下列实验现象的液体及物质的化学式。
现象 序号 | ①a处液面降低 | ②b处液面降低 |
液体 | ________ | ________ |
物质 | ________ | ________ |
三、计算题(每小题4分,共计36分)
1、50克稀盐酸和150克8%NaOH溶液混合后恰好完全中和,则反应后溶液溶质的质量分数为____?
2、为测定一瓶敞口放置的浓盐酸的溶质质量分数,某同学量取20 mL(密度为1.1 g/mL该盐酸与大理石充分反应,共用去含碳酸钙85%的大理石7.1 g。
(1)浓盐酸需要密封保存的原因是_________。
(2)计算该盐酸的溶质质量分数。
3、小明同学想测量某赤铁矿样品中氧化铁的纯度(假设其他成分不和酸反应,也不溶于水),进行如下实验:称取10g赤铁矿样品,加入到烧杯中,再加入92.5g的稀硫酸,恰好完全反应。过滤得滤渣2.5g。试计算:
(1)赤铁矿样品中氧化铁的质量分数?______
(2)求所用稀硫酸的溶质质量分数?_______
4、利用中和反应可以测定酸或碱溶液中溶质的质量分数,向20g氢氧化钾溶液中不断滴加溶质质量分数为3.65%的稀盐酸40g。
(1)如图中a、b、c三溶液能表示酸碱恰好完全反应的是______溶液,滴入石蕊试液呈红色的是______溶液,b溶液中微粒有 (写微粒符号)。
(2)氢氧化钾溶液中溶质质量分数为______。(精确到0.1%,下同)
(3)求c点溶液中氯化钾的质量分数。(要有计算过程)
5、欲测定一瓶标签破损的氢氧化钠溶液的溶质质量分数,现取8g氢氧化钠溶液样品于烧杯中,将3.65%的稀盐酸逐滴加入烧杯中,边加边搅拌,随着稀盐酸的不断加入,数字化传感器测得溶液pH的变化如图所示:
(1)当加入稀盐酸质量为32g时,溶液的pH______7(填“>”、“<”或“=”)。
(2)计算该氢氧化钠溶液的溶质质量分数(写出计算过程)。
6、取铜与氧化铜的混合物5g于烧杯中,向烧杯中加入稀硫酸,发现烧杯中剩余固体的质量与加入稀硫酸质量的关系如图所示。回答下列问题:
(1)剩余的3.4克固体物质是______,该物质在原混合物中的质量分数是______。
(2)求所加稀硫酸的溶质质量分数。
7、胃酸主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g。某患者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用如图所示抑酸剂,发生反应:,请计算并回答:按说明书用法用量,每天最多可中和胃液中盐酸溶质质量是多少克?(写出计算过程,结果精确到0.001)
8、某同学对上述实验继续展开探究,利用溶质质量分数为3.65%的稀盐酸溶液来测定10gNaOH溶液样品的溶质质量分数,用数字化传感器测得溶液中pH的变化如图所示。
(1)a点时向溶液中滴入无色酚酞试液,溶液显_______色。
(2)c点时溶液中的溶质有________种。
(3)当pH=7时恰好完全反应,求10 g NaOH溶液样品中溶质的质量分数。(反应的化学方程式:)
9、往150克含有稀硝酸和硝酸钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图(假设生成的气体全部逸出),试分析
计算:
(1)c→d段溶液的pH大于7的原因是______。
(2)反应到c点时,所得溶液的溶质质量分数是多少?(写出计算过程,精确到0.1%)
四、实验探究(每小题5分,共计20分)
1、化学小组围绕“铁丝在氧气中燃烧现象及产物”的问题,进行了相应的探究活动。
活动 1:“火星四射”的现象与铁丝含碳量的关系:
实验操作 | 实验现象 | 实验结论 |
实验1:取直径0.20mm,含碳0.1%的铁丝在氧气中燃烧 | 零星火星 生成黑色固体 | 铁丝燃烧的 “火星四射”与铁丝含碳量的关系是_______。 |
实验2:取直径______mm,含碳0.3%的铁丝在氧气中燃烧 | 较明显的火星四射生成较多黑色固体 |
活动 2:黑色固体中是否含有铁?
资料:①铁粉是黑色或灰黑色粉末。四氧化三铁为黑色固体,具有磁性。
②铁、四氧化三铁均能溶于稀盐酸
(即: ;)
③氯化亚铁溶液为浅绿色,氯化铁溶液为黄色。
小明质疑小刚用磁铁来检验黑色固体是否含有铁的方案,其理由是________;
同学们都认可了下列实验方案:
实验操作 | 实验现象 | 实验结论 |
取少量黑色固体于试管中,加入一定量_______,放置一段时间。 | 有气泡产生,溶液由无色变成黄色 | ____________ |
2、某实验小组的同学用氢氧化钠溶液和盐酸做中和反应的实验。
(演示实验)他们向盛有氢氧化钠溶液的烧杯中滴加一定量的稀盐酸,发生的化学反应方程式是:______。
(提出问题)反应后溶液中溶质的成分是什么?
(猜想与假设)甲组同学猜想如下:
猜想一:可能是 NaCl 和 HCl;
猜想二:可能只有 NaCl;
猜想三:______。
猜想四:可能是 NaCl、HCl 和 NaOH
乙组同学对以上猜想提出质疑,认为猜想四不合理,其理由是______。
(进行实验)为了验证其余猜想,各小组进行了下列两个方案的探究。
实验步骤 | 实验操作 | 实验现象 | 结论 |
① | 取少量烧杯内的溶液于试管中,滴入几滴酚酞溶液,振荡 | ______ | 猜想三不成立 |
② | 方案一:取少量烧杯内的溶液于试管中,加入______ | ______ | 猜想一成立 |
方案二:取少量烧杯内的溶液于试管中,加入(与方案一不同类别的物质)______ | ______ |
3、铜锈又叫铜绿,是一种绿色固体,它的化学式是Cu2(OH)2CO3,将铜锈加热,会生成固态、液态、气态三种氧化物。化学兴趣小组对这三种生成物进行了探究.
(猜想)
猜想一:此三种物质分别是CuO、H2O、CO2
猜想二:此三种物质分别是CuO、H2O、CO
(查阅资料)
无水硫酸铜是一种白色粉末,遇水变成蓝色。
(实验)
实验小组取铜锈若干克,低温干燥后加入试管中加热,后续实验如下
实验步骤 | 实验现象 | 实验结论 |
步骤 1:将反应产生的气体通入如下装置中 | (1)观察到装置A中的实验现象是_______ | 说明该气体中有H2O |
装置B中澄清石灰水变浑浊 | (2)说明该气体中有_____;写出装置B中发生反应的化学方程式_______。 | |
步骤2:取少量反应后试管中的黑色粉末于另一试管中,往其中加入稀硫酸,将试管置于酒精灯上加热。 | 溶液由无色变成蓝色 | 说明黑色粉末是CuO |
(总结)
(3)综上所述,写出加热铜锈发生反应的化学方程式_______。
(反思)
(4)实验步骤1的装置中,气球的作用是________。
(5)甲同学认为实验步骤1中,装置A和B的位置可以对调,乙同学不同意,其原因是_______。
4、 “自热米饭”中带有一个发热包,遇水后可迅速升温至150℃,能将生米做成熟饭。某化学小组对发热包的固体进行了探究。
(查阅资料)发热包可能由生石灰、铁粉、铝粉、炭粉、氯化钠中的若干种物质组成。
(实验探究)
探究一:发热包的发热原理。
(1)取出发热包加入凉水,发生剧烈反应,迅速放出大量的热,写出产生该现象的主要化学反应方程式__________。
探究二:发热包的固体成分的探究。
(2)完成下表
步骤 | 实验操作 | 实验现象 | 实验结论 |
(1) | 取发热包内灰黑色的固体粉末,分成两份 | / | / |
(2) | 用磁铁多次重复靠近其中一份粉末 | 有部分黑色固体被磁铁吸引 | ___________ |
(3) | 取步骤(2)的剩余的固体于试管中,加入足量稀盐酸 | __________溶液呈无色。 | 原粉末一定含有铝粉和炭粉 |
(4) | 取另一份粉末加水溶解,过滤,向滤液通入__________ | 滤液变浑浊 | 原粉末中一定含有生石灰 |
(反思与评价)
(3)综合上述实验,无法确定该发热包中是否含有_________。
2021年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷最新: 这是一份2021年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷最新,共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2021学年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷精品: 这是一份2021学年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷精品,共15页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2021学年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷(完整): 这是一份2021学年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷(完整),共12页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。












