
2022学年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷【全面】
展开
这是一份2022学年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷【全面】,共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
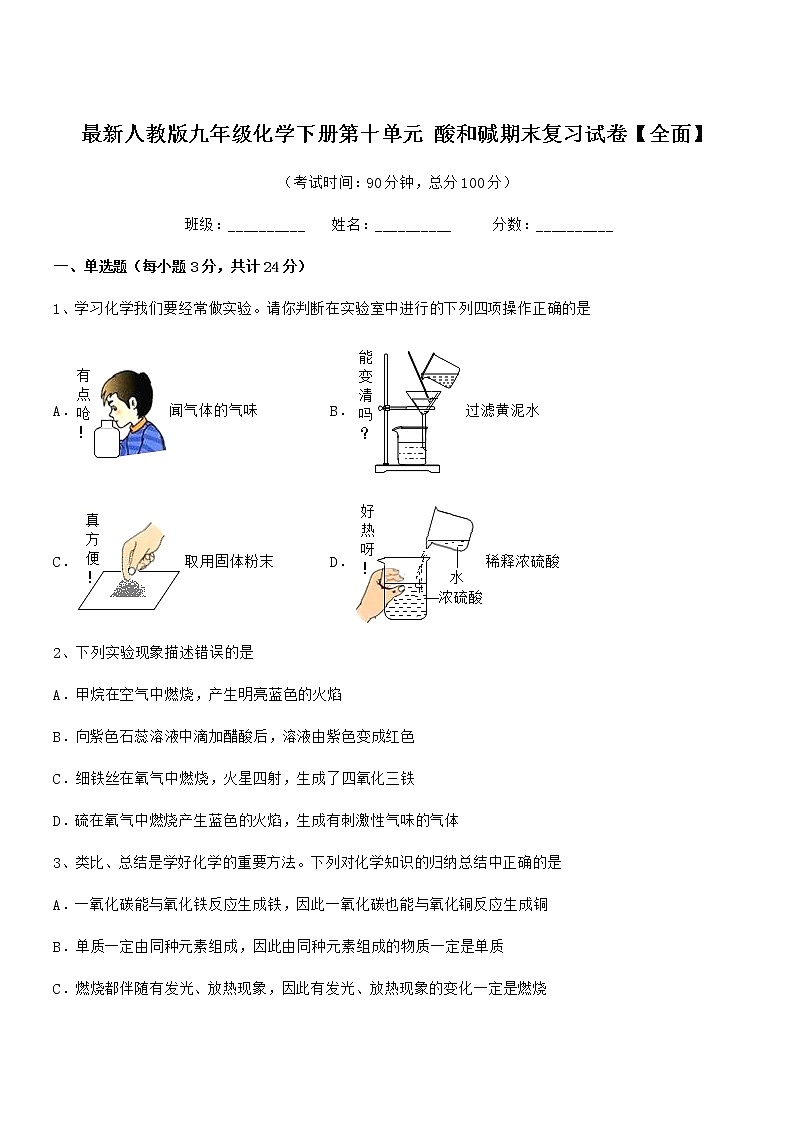
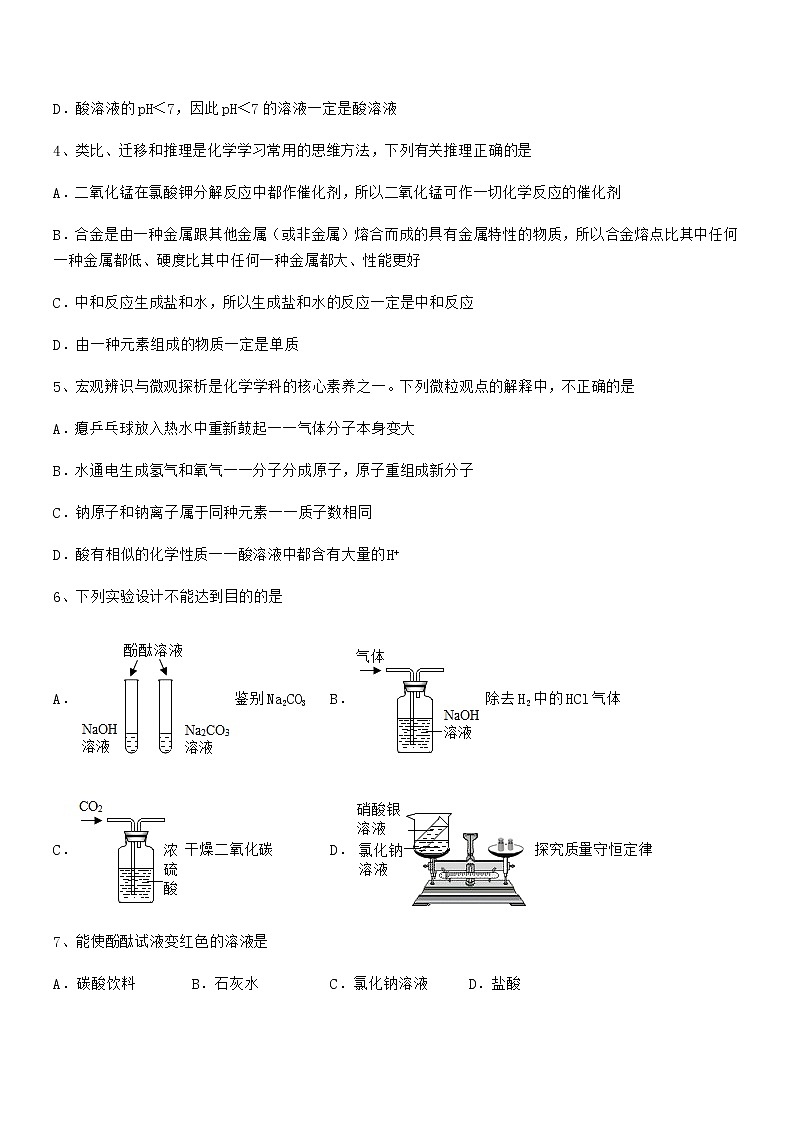
最新人教版九年级化学下册第十单元 酸和碱期末复习试卷【全面】(考试时间:90分钟,总分100分)班级:__________ 姓名:__________ 分数:__________一、单选题(每小题3分,共计24分)1、学习化学我们要经常做实验。请你判断在实验室中进行的下列四项操作正确的是A.闻气体的气味 B.过滤黄泥水C.取用固体粉末 D.稀释浓硫酸2、下列实验现象描述错误的是A.甲烷在空气中燃烧,产生明亮蓝色的火焰B.向紫色石蕊溶液中滴加醋酸后,溶液由紫色变成红色C.细铁丝在氧气中燃烧,火星四射,生成了四氧化三铁D.硫在氧气中燃烧产生蓝色的火焰,生成有刺激性气味的气体3、类比、总结是学好化学的重要方法。下列对化学知识的归纳总结中正确的是A.一氧化碳能与氧化铁反应生成铁,因此一氧化碳也能与氧化铜反应生成铜B.单质一定由同种元素组成,因此由同种元素组成的物质一定是单质C.燃烧都伴随有发光、放热现象,因此有发光、放热现象的变化一定是燃烧D.酸溶液的pH<7,因此pH<7的溶液一定是酸溶液4、类比、迁移和推理是化学学习常用的思维方法,下列有关推理正确的是A.二氧化锰在氯酸钾分解反应中都作催化剂,所以二氧化锰可作一切化学反应的催化剂B.合金是由一种金属跟其他金属(或非金属)熔合而成的具有金属特性的物质,所以合金熔点比其中任何一种金属都低、硬度比其中任何一种金属都大、性能更好C.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应D.由一种元素组成的物质一定是单质5、宏观辨识与微观探析是化学学科的核心素养之一。下列微粒观点的解释中,不正确的是A.瘪乒乓球放入热水中重新鼓起一一气体分子本身变大B.水通电生成氢气和氧气一一分子分成原子,原子重组成新分子C.钠原子和钠离子属于同种元素一一质子数相同D.酸有相似的化学性质一一酸溶液中都含有大量的H+6、下列实验设计不能达到目的的是A.鉴别Na2CO3 B.除去H2中的HCl气体C.干燥二氧化碳 D.探究质量守恒定律7、能使酚酞试液变红色的溶液是A.碳酸饮料 B.石灰水 C.氯化钠溶液 D.盐酸8、下列有关实验现象或事实叙述错误的是A.铁丝在氧气在燃烧,火星四射,生成黑色固体B.用带火星的木条复燃来检验氧气C.排水法收集氧气时,导管口冒出气泡,立即收集D.浓硫酸不慎溅到皮肤上先用大量的水冲洗,再涂上3%-5%的碳酸氢钠溶液二、填空题(每小题4分,共计20分)1、化学与生活联系密切,生活中处处有化学。(1)市场上调味品种类丰富,有碘盐、钙盐、加铁酱油等,其中含有的碘、钙、铁三种元素中属于非金属元素的是___________。(2)农村一些家庭用“沼气”做燃料,沼气的主要成分是甲烷(CH4)。写出甲烷完全燃烧的化学方程式___________。(3)长期饮用硬水对人体健康不利,生活中可用___________来区别硬水和软水,用___________方法将硬水变成软水;实验室软化水的方法是___________。(4)氢氧化铝治疗胃酸过多的方程式___________。(5)交警通常用一种“酒精检测仪”检查司机呼出的气体中的酒精含量是否超标,其反应原理为:C2H5OH+4CrO3+6H2SO4═2X+2CO2↑+9H2O,反应中红色的CrO3转变为绿色的化合物X,则X的化学式为___________。A.Cr2O3 B.CrSO3 C.Cr2(SO4)3 D.CrS2、化学与我们的生活生产息息相关,生活处处有化学。2020年10月郴政办印发《郴州市生活垃圾分类工作实施方案》,从此郴州市全面推行垃圾分类。如图是某街道的垃圾分类箱。(1)图中属于金属材料的是___________(填序号)。(2)废纸、金属易拉罐应投入___________(填“可回收”或“不可回收”)筒中。(3)使用铝合金做内筒的优点是___________(写出一点即可)。(4)用稀盐酸除铁锈的原理是___________(用化学方程式表示)。3、如图是两种稀释浓硫酸的操作:回答下列问题:(1)B图中盛水的仪器的名称是_______。(2)稀释浓硫酸操作正确的是(填序号A、B)_______。(3)A图中玻璃棒进行搅拌操作的目的是_________。4、酸与金属氧化物的反应 反应的现象结论(反应的化学方程式)过量稀盐酸和生锈的铁钉①________;②________。①________;②________; 5、水是生命之源,“爱惜水,保护水”是每个公民的义务和责任.(1)海水淡化是获取淡水的方法之一.用如图所示的方法获得淡水的过程中发生的是______变化(填“物理”或“化学”)。(2)高铁酸钾(K2FeO4)可以用于灾区饮用水的净化,制备K2FeO4的化学反应方程式为:2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,X的化学式为_____,K2FeO4中Fe的化合价_____。(3)化学工业中的废水是污染水源的主要原因之一,某硫酸厂的废水含有Na2SO4、H2SO4等物质,工厂用废铁粉、熟石灰等物质进行无害化处理后再排放,写出发生中和反应的化学方程式_____。三、计算题(每小题4分,共计36分)1、废旧金属的回收利用既能保护环境,又能节约资源和能源。某冶金厂回收了一批废黄铜屑,需测定其中铜元素的质量分数。现称取100.0g样品,加入足量稀硫酸,充分反应后得无色溶液,产生氢气的质量及剩余固体的质量与消耗稀硫酸的质量关系分别如图所示。(设该批次黄铜屑只含铜、锌和少量黄铜锈。黄铜锈与稀硫酸反应生成CuSO4、ZnSO4、CO2和H2O。)请回答下列问题:(1)完全反应时,样品消耗稀硫酸的质量为______g。(2)样品中铜元素的质量分数为______%(计算结果精确到0.1%,下同);(3)计算稀硫酸中溶质的质量分数(写出计算过程)。2、利用中和反应可以测定酸或碱溶液中溶质的质量分数,向20g氢氧化钾溶液中不断滴加溶质质量分数为3.65%的稀盐酸40g。(1)如图中a、b、c三溶液能表示酸碱恰好完全反应的是______溶液,滴入石蕊试液呈红色的是______溶液,b溶液中微粒有 (写微粒符号)。(2)氢氧化钾溶液中溶质质量分数为______。(精确到0.1%,下同)(3)求c点溶液中氯化钾的质量分数。(要有计算过程)3、为测定某赤铁矿样品中氧化铁的含量,化学兴趣小组同学将赤铁矿样品粉碎,取赤铁矿样品25g于烧杯中,加入200g溶质质量分数为13.7%的稀盐酸,恰好完全反应。(样品中杂质不溶于水,也不与盐酸发生反应)(1)稀盐酸溶液溶质的质量为______g。(2)赤铁矿样品中氧化铁的质量。(计算结果保留整数)4、实验室欲测定一瓶标签破损的稀硫酸的溶质质量分数。现取10 g稀硫酸样品,将5%的氢氧化钠溶液逐滴加入到样品中,边加边搅拌。随着氢氧化钠溶液的不断加入,溶液pH的变化如图所示。试回答:(1)a点溶液中含有的溶质有_______;(2)求该稀硫酸的溶质质量分数是____?当硫酸恰好反应完时,求所得溶液的溶质质量分数____?(写出计算过程,不能整除的结果保留一位小数)5、往150克含有稀硝酸和硝酸钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图(假设生成的气体全部逸出),试分析计算:(1)c→d段溶液的pH大于7的原因是______。(2)反应到c点时,所得溶液的溶质质量分数是多少?(写出计算过程,精确到0.1%)6、实验室预测定一瓶标签破损的稀硫酸的质量分数。现取10克稀硫酸样品,将5%的氢氧化钠溶液逐滴加入,边加边搅拌,同时测定pH值,其记录结果如图:回答下列问题:(1)a点溶液中含有的阳离子有________。(2)求该稀硫酸总溶质的质量分数。7、200g盐酸溶液与100g16%的氢氧化钠溶液充分反应, NaOH + HCl = NaCl + H2O求:(相对原子质量: H-1 O-16 Na-23 Cl-35.5 )(1)盐酸溶液中溶质的质量分数;(2)所得溶液中溶质的质量分数。8、实验室欲测定一瓶标签破损的稀H2SO4的溶质质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液加入,溶液液的pH的变化如图所示试回答:(1)a点溶液中含有的离子有______。(2)当pH=7时,消耗NaOH溶液中NaOH的质量为_______。(3)计算生成溶液中溶质的质量分数_______(小数点后保留一位小数)9、欲测定一瓶标签破损的氢氧化钠溶液的溶质质量分数,现取8g氢氧化钠溶液样品于烧杯中,将3.65%的稀盐酸逐滴加入烧杯中,边加边搅拌,随着稀盐酸的不断加入,数字化传感器测得溶液pH的变化如图所示:(1)当加入稀盐酸质量为32g时,溶液的pH______7(填“>”、“<”或“=”)。(2)计算该氢氧化钠溶液的溶质质量分数(写出计算过程)。四、实验探究(每小题5分,共计20分)1、实验室中有一瓶长期使用的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究。(发现问题)该样品中含有哪些物质?(查阅资料)①NaOH在空气中不会转化成 NaHCO3②BaCl2溶液呈中性,Ba(OH)2是可溶性碱。③CO2在饱和的 NaHCO3溶液中几乎不溶解。(提出猜想)猜想Ⅰ:NaOH 猜想Ⅱ:Na2CO3猜想Ⅲ:NaOH和Na2CO3(设计实验)实验操作实验现象①:取少量样品于试管中,滴加足量水样品全部溶解,得到无色溶液②:取步骤①所得无色溶液于试管中,滴加足量X溶液观察到现象A(收集证据)(1)若现象A是有气泡产生,则X溶液为__________,则猜想________(填“Ⅰ”、“Ⅱ”或“Ⅲ”)不成立。(2)若X溶液为BaCl2溶液,现象A是_______________;再取反应后的上层清液,______________(填实验操作和现象),则证明猜想Ⅲ成立。(定量分析)确定部分变质样品中Na2CO3的质量分数。兴趣小组的同学用如图所示装置进行实验。步骤如下:①按图连接好装置,并检查气密性;②准确称取该样品1.0g,放入烧瓶内;③打开活塞,滴加30.0%的稀硫酸至过量,关闭活塞;④反应结束后,量筒内液体的读数为55.0mL。(已知:室温条件下,CO2的密度为1.6g·L-1)(1)B装置集气瓶内原有的空气对实验结果_________(填“有”或“没有”)影响。饱和 NaHCO3溶液如果用水代替,则所测CO2体积____________(填“偏大”、偏小”或“不变”)。(2)该样品中Na2CO3的质量分数_____________(保留一位小数)。(实验反思)实验中量筒的作用是____________。2、49中学化学兴趣小组同学在学习酸和碱发生中和反应时进行下面的实验探究:(实验活动)(观察与结论)同学们观察到B烧杯中________现象,于是判断氢氧化钠和稀盐酸发生了反应,该反应的化学方程式为___________。(反思与总结)由此实验可知:验证没有明显现象的反应发生了,可以通过验证有新物质生成或验证________来判断反应发生了。(提岀问题)同学们对反应后B烧杯中溶液溶质的成分产生了兴趣,B烧杯中溶液溶质是什么物质?(酚酞除外)(猜想与假设)猜想1:NaCl 猜想2:HC1 NaCl NaOH 猜想3:HCl NaCl(交流讨论)小月同学认为猜想2不成立,其理由是_______。(实验活动)为了探究溶液中溶质成分,小亮取少许B烧杯中溶液,向其中加入有色溶液,观察到_______,得出猜想3成立的结论;(反思与总结)通过此题的探究,我们可以推而广之,在探究反应后溶液中溶质成分时,只需要选择与需要验证的物质是否_______,即可得出正确结论。3、为适应铁路高铁时代提速的要求,需把短轨连成长轨,常用反应:2Al+Fe2O3Al2O3+2Fe进行焊接,该反应称为“铝热反应”。镁和氧化铜也能发生类似的反应,写出反应方程式_______某小组同学在实验室中进行镁和氧化铜反应的实验,充分反应后对于固体剩余物进行了实验探究。(提出问题)固体剩余物是什么?(猜想假设)假设①铜和氧化镁;假设②_______;假设③_______。(均写化学式)(查阅资料一)大多数金属氧化物都能与硫酸发生复分解反应(实验探究)请完成下列实验。实验操作实验现象实验结论取少量固体剩余物于试管中,向其中加入足量的稀硫酸。固体部分溶解,溶液为无色。假设①成立。_______。假设②成立。_______。假设③成立。(思考)是否任何一种金属单质都能与另一种金属氧化物反应? (查阅资料二)该小组同学通过查阅资料,获得以下几组反应信息。 实验组别IIIIIIIVV药品AlFeAgAlCuCuOCuOCuOFe2O3Fe2O3相同条件下是否反应是是否是否(总结)根据上表对比分析得出:金属单质与金属氧化物能发生反应,需满足的条件是:在金属活动顺序表中金属单质要比氧化物中的金属位置靠_______。(填写“前”或“后”)4、下图“黑面包”实验中,蔗糖(C12H22O11)变黑,体枳膨胀,变成疏松的炭,放出有刺激性气味的气体。(提出问题)改变糖的种类、浓硫酸的体积、水的滴数和温度是否会影响实验效果呢?(进行实验)分别取5g糖粉进行实验,根据前2min的现象对实验效果进行评分,记录如下;表1实验记录实验糖浓硫酸体积/mL水的滴数温度/℃效果得分1蔗糖4522652蔗糖51030813蔗糖61550934冰糖41050915冰糖51522886冰糖a530757葡萄糖4153008葡萄糖555009葡萄糖610220(处理数据)分析表1,计算效果得分均值,结果如下:表2 效果得分均值因素糖浓硫酸体积/mL水的滴数温度/℃蔗糖冰糖葡萄糖45651015223050均值79.784.7052.056.356.046.757.360.351.052.061.3依据均值推断最佳实验方案,均值越高,效果越好。(解释与结论)(1)蔗糖变成黑色的炭,发生了______(填“物理”或“化学”)变化。(2)实验6中,a为______mL。(3)根据表2推断,“黑面包”实验最好选择5g冰糖、5mL浓硫酸、______滴水和50℃(反思与评价)(4)表2中,22℃对应的均值为51.0,计算该值所依据的3个实验分别是______。(填编号)(5)综合分析,使实验3的效果得分高于实验4的因素有______。
相关试卷
这是一份2022学年最新人教版九年级化学下册第十单元 酸和碱期末考试卷【全面】,共13页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
这是一份2022学年最新人教版九年级化学下册第十单元 酸和碱期末考试卷(全面),共12页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
这是一份2022学年最新人教版九年级化学下册第十单元 酸和碱期末复习试卷精品,共13页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。









