

所属成套资源:2022高考化学一轮复习专练含解析专题
2022高考化学一轮复习专练22化学工艺流程题含解析
展开
这是一份2022高考化学一轮复习专练22化学工艺流程题含解析,共10页。
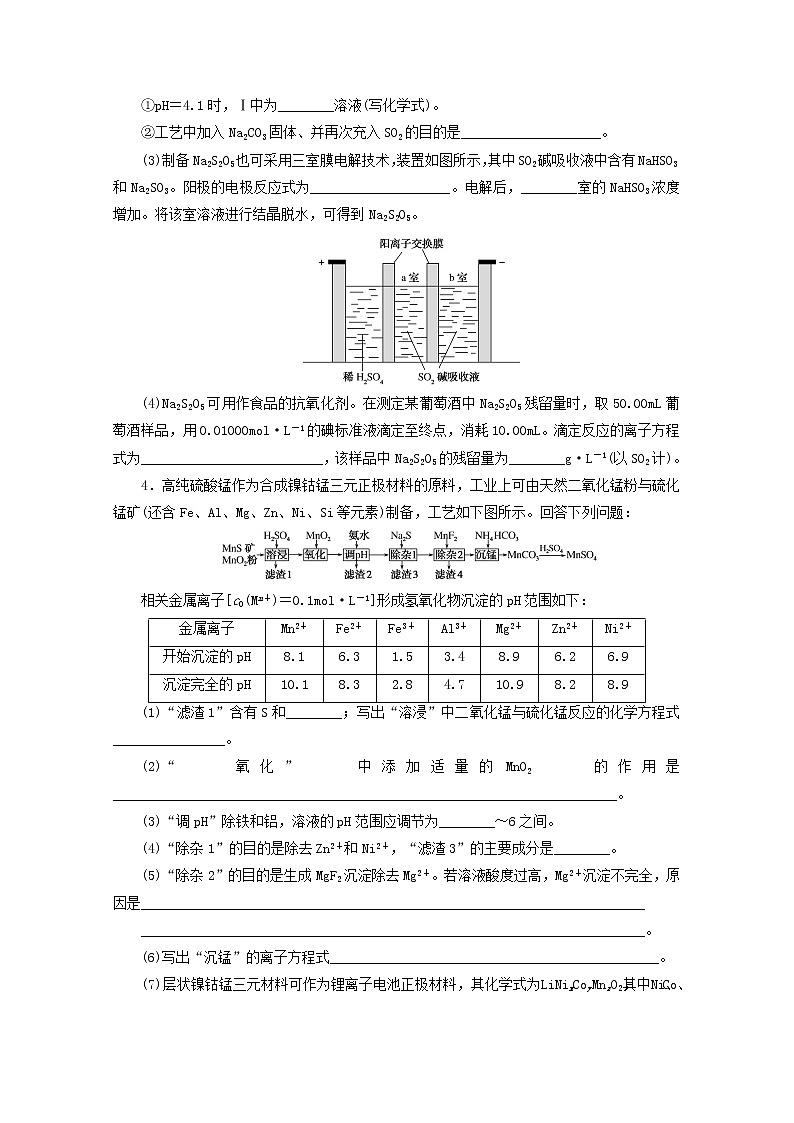
专练22 化学工艺流程题1.[2020·全国卷Ⅰ]钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:金属离子Fe3+Fe2+Al3+Mn2+开始沉淀pH1.97.03.08.1完全沉淀pH3.29.04.710.1回答下列问题:(1)“酸浸氧化”需要加热,其原因是_________________________________________。(2)“酸浸氧化”中,VO+和VO2+被氧化成VO,同时还有________离子被氧化。写出VO+转化为VO反应的离子方程式______________________________________________。(3)“中和沉淀”中,钒水解并沉淀为V2O5·xH2O,随滤液②可除去金属离子K+、Mg2+、Na+、________,以及部分的________。(4)“沉淀转溶”中,V2O5·xH2O转化为钒酸盐溶解。滤渣③的主要成分是________。(5)“调pH”中有沉淀生成,生成沉淀反应的化学方程式是________________________________。(6)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是____________________________。 2.[2021·湖南卷]碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定产品中少量碳酸氢钠的含量,过程如下:步骤Ⅰ.Na2CO3的制备步骤Ⅱ.产品中NaHCO3含量测定①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用0.1000mol·L-1盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸V1mL;③在上述锥形瓶中再加入2滴指示剂N,继续用0.1000mol·L-1盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸V2mL;④平行测定三次,V1平均值为22.45,V2平均值为23.51。已知:(ⅰ)当温度超过35℃时,NH4HCO3开始分解。(ⅱ)相关盐在不同温度下的溶解度表(g/100gH2O)温度/℃0102030405060NaCl35.735.836.036.336.637.037.3NH4HCO311.915.821.027.0 NaHCO36.98.29.611.112.714.516.4NH4Cl29.433.337.241.445.850.455.2回答下列问题:(1)步骤Ⅰ中晶体A的化学式为________,晶体A能够析出的原因是________________________________;(2)步骤Ⅰ中“300℃加热”所选用的仪器是________(填标号);(3)指示剂N为________,描述第二滴定终点前后颜色变化________________________;(4)产品中NaHCO3的质量分数为________(保留三位有效数字);(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则NaHCO3质量分数的计算结果________(填“偏大”“偏小”或“无影响”)。 3.焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。回答下列问题:(1)生产Na2S2O5,通常是由NaHSO3过饱和溶液经结晶脱水制得。写出该过程的化学方程式______________________________________。(2)利用烟道气中的SO2生产Na2S2O5的工艺为:①pH=4.1时,Ⅰ中为________溶液(写化学式)。②工艺中加入Na2CO3固体、并再次充入SO2的目的是____________________。(3)制备Na2S2O5也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。阳极的电极反应式为____________________。电解后,________室的NaHSO3浓度增加。将该室溶液进行结晶脱水,可得到Na2S2O5。(4)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00mL葡萄酒样品,用0.01000mol·L-1的碘标准液滴定至终点,消耗10.00mL。滴定反应的离子方程式为__________________________,该样品中Na2S2O5的残留量为________g·L-1(以SO2计)。4.高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:金属离子Mn2+Fe2+Fe3+Al3+Mg2+Zn2+Ni2+开始沉淀的pH8.16.31.53.48.96.26.9沉淀完全的pH10.18.32.84.710.98.28.9(1)“滤渣1”含有S和________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式________________。(2)“氧化”中添加适量的MnO2的作用是________________________________________________________________________。(3)“调pH”除铁和铝,溶液的pH范围应调节为________~6之间。(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是________。(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是________________________________________________________________________________________________________________________________________________。(6)写出“沉锰”的离子方程式_______________________________________________。(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=时,z=________。5.[2020·全国卷Ⅲ]某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):溶液中金属离子开始沉淀和完全沉淀的pH如下表所示: 金属离子Ni2+Al3+Fe3+Fe2+开始沉淀时(c=0.01mol·L-1)的pH7.23.72.27.5沉淀完全时(c=1.0×10-5mol·L-1)的pH8.74.73.29.0回答下列问题:(1)“碱浸”中NaOH的两个作用分别是______________________________________。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式______________________。(2)“滤液②”中含有的金属离子是__________________。(3) “转化”中可替代H2O2的物质是________________。若工艺流程改为先“调pH”后“转化”,即,“滤液③”中可能含有的杂质离子为________。(4)利用上述表格数据,计算Ni(OH)2的Ksp=__________________(列出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0mol·L-1,则“调pH”应控制的pH范围是________。(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式____________________________。(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是____________________________。6.[2021·广东卷]对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝(Al)、钼(Mo)、镍(Ni)等元素的氧化物,一种回收利用工艺的部分流程如下:已知:25℃时,H2CO3的Ka1=4.5×10-7,Ka2=4.7×10-11;Ksp(BaMoO4)=3.5×10-8;Ksp(BaCO3)=2.6×10-9;该工艺中,pH>6.0时,溶液中Mo元素以MoO的形态存在。(1)“焙烧”中,有Na2MoO4生成,其中Mo元素的化合价为________。(2)“沉铝”中,生成的沉淀X为________。(3)“沉钼”中,pH为7.0。①生成BaMoO4的离子方程式为________________________。②若条件控制不当,BaCO3也会沉淀。为避免BaMoO4中混入BaCO3沉淀,溶液中c:c=____________________________(列出算式)时,应停止加入BaCl2溶液。(4)①滤液Ⅲ中,主要存在的钠盐有NaCl和Y,Y为________。②往滤液Ⅲ中添加适量NaCl固体后,通入足量____________(填化学式)气体,再通入足量CO2,可析出Y。(5)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止H2O2刻蚀液与下层GaAs(砷化镓)反应。①该氧化物为________。②已知:Ga和Al同族,As和N同族。在H2O2与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为________。 专练22 化学工艺流程题1.(1)加快酸浸和氧化反应速率(促进氧化完全)(2)Fe2+ VO++MnO2+2H+===VO+Mn2++H2O(3)Mn2+ Al3+和Fe3+(4)Fe(OH)3(5)NaAl(OH)4+HCl===Al(OH)3↓+NaCl+H2O(6)利用同离子效应,促进NH4VO3尽可能析出完全解析:(1)加热的目的是使反应完全,加快酸浸速率。(2)Fe3O4与硫酸反应生成Fe2+和Fe3+,Fe2+能够被氧化为Fe3+;VO+中钒元素化合价为+3,VO中钒元素化合价为+5,VO+被MnO2氧化为VO,MnO2被还原为Mn2+,结合得失电子守恒、原子守恒和电荷守恒配平:VO++MnO2+2H+===VO+Mn2++H2O。(3)pH=3.0~3.1时,Mn2+还未沉淀,所以滤液②中有Mn2+,另外Fe3+、Al3+在该pH范围内没有沉淀完全,部分留在滤液②中。(4)滤饼②中除了有V2O5·xH2O,还有少量Fe(OH)3和Al(OH)3,加NaOH调pH>13,V2O5·xH2O与NaOH反应生成NaVO3,Al(OH)3与NaOH反应生成NaAl(OH)4,Fe(OH)3不与NaOH反应,所以滤渣③是Fe(OH)3。(5)“调pH”的目的是将NaAl(OH)4转化为Al(OH)3沉淀除去,反应的化学方程式为NaAl(OH)4+HCl===Al(OH)3↓+NaCl+H2O,则滤渣④为Al(OH)3。(6)加入过量NH4Cl固体,c(NH)增大,根据同离子效应,可促进NH4VO3晶体尽可能完全析出。2.(1) NaHCO3 30~35℃,NaHCO3的溶解度小于NaCl、NH4HCO3和NH4Cl的溶解度(2)D(3)甲基橙 溶液由黄色变为橙色,且半分钟内不变色(4)3.56%(5)偏大解析:(1)根据相关盐在不同温度下的溶解度可知,30~35℃,NaHCO3的溶解度明显小于NaCl、NH4HCO3和NH4Cl的溶解度,因此NaHCO3在步骤Ⅰ中结晶析出。(2)300℃给固体加热选用的仪器应为坩埚。(3)本题中测定碳酸氢钠含量采用了双指示剂滴定法,第一滴定过程以酚酞为指示剂,Na2CO3转化为NaHCO3,第二滴定过程以甲基橙为指示剂,NaHCO3转化为NaCl、CO2和H2O,所以第二滴定终点前后溶液由黄色变为橙色,且半分钟内不变色。(4)由(3)的分析过程可知,25.00mL待测液中所含NaHCO3的物质的量为0.1000mol·L-1×(V2-V1)×10-3L,则2.500g产品中所含NaHCO3的质量为84g·mol-1××0.1000mol·L-1×(23.51-22.45)×10-3L≈0.089g,则产品中NaHCO3的质量分数=×100%≈3.56%。(5)第一次滴定终点时,俯视读数,导致测得的V1偏小,NaHCO3质量分数的计算结果偏大。3.(1)2NaHSO3===Na2S2O5+H2O(2)①NaHSO3 ②得到NaHSO3过饱和溶液(3)2H2O-4e-===4H++O2↑ a(4)S2O+2I2+3H2O===2SO+4I-+6H+ 0.128解析:(1)由题可知,NaHSO3脱水转化为Na2S2O5,故可写出化学方程式:2NaHSO3===Na2S2O5+H2O。(2)①Na2S2O5由NaHSO3过饱和溶液脱水结晶而来,因而溶液Ⅲ为NaHSO3,而Ⅰ和ⅢPH相同,溶质相同,也为NaHSO3。②通SO2使得NaHSO3变多,浓度变大,得到NaHSO3过饱和溶液。(3)阳极发生氧化反应,电极反应式为2H2O-4e-===4H++O2↑,H+通过阳离子交换膜由阳极向a室移动,得到NaHSO3,故a室NaHSO3增多。(4)根据题意,S2O与I2发生氧化还原反应,生成SO和I-,即解得x=0.5×10-4,则SO2物质的量为0.5×2×10-4mol,所以最后的残留量==0.128g·L-1。4.(1)SiO2(不溶性硅酸盐)MnO2+MnS+2H2SO4===2MnSO4+S+2H2O(2)将Fe2+氧化为Fe3+(3)4.7(4)NiS和ZnS(5)F-与H+结合形成弱电解质HF,MgF2Mg2++2F-平衡向右移动(6)Mn2++2HCO===MnCO3↓+CO2↑+H2O(7)解析:本题涉及元素化合物知识的综合应用,通过工艺流程形式给出信息,考查分析和解决化学工艺流程问题的能力,根据题给信息书写相应的化学方程式和离子方程式,体现了证据推理与模型认知的学科核心素养。(1)由题干信息可知,滤渣有生成的S和不与H2SO4反应的SiO2(或写不溶性硅酸盐);依据氧化还原反应原理可知,MnO2作氧化剂,MnS作还原剂,由此可写出化学方程式。(2)Fe溶于H2SO4中得到Fe2+,为了去除方便,需将Fe2+氧化为Fe3+。(3)由相关金属离子形成氢氧化物沉淀的pH范围可知除铁和铝时溶液pH范围应调节为4.7~6之间。(4)NiS和ZnS是难溶于水的硫化物。(5)MgF2(s)Mg2+(aq)+2F-(aq),若增大H+浓度,F-与H+会结合成弱电解质HF而使沉淀溶解平衡正向移动,导致溶液中Mg2+沉淀不完全。(6)由于HCOH++CO,CO与Mn2+可形成MnCO3沉淀,使HCO电离平衡正向移动,H+浓度增大,H+与HCO反应生成H2O和CO2,所以离子方程式为Mn2++2HCO===MnCO3↓+CO2↑+H2O。(7)根据化合物中各元素正、负化合价的代数和为0,可知+1+(+2)×x+(+3)×y+(+4)×z+(-2)×2=0,将x=y=代入计算,可得z=。5.(1)除去油脂、溶解铝及其氧化物 Al(OH)+H+===Al(OH)3↓+H2O(2)Ni2+、Fe2+、Fe3+(3)O2或空气 Fe3+(4)0.01×(107.2-14)2[或10-5×(108.7-14)2] 3.2~6.2(5)2Ni2++ClO-+4OH-===2NiOOH↓+Cl-+H2O(6)提高镍回收率解析:(1)油脂可在NaOH溶液中发生水解反应生成可溶性的高级脂肪酸钠和甘油,并且NaOH溶液能溶解Al和Al2O3,2Al+2NaOH+2H2O===2NaAlO2+3H2↑、Al2O3+2NaOH===2NaAlO2+H2O,故“碱浸”中NaOH的两个作用分别是除去油脂和溶解铝及其氧化物。“滤液①”中含有Na[Al(OH)4](也可写成NaAlO2),向其中加入稀H2SO4调为中性会生成Al(OH)3沉淀,反应的离子方程式为Al(OH)+H+===Al(OH)3↓+H2O或AlO+H++H2O===Al(OH)3↓。(2)“滤饼①”中含有Ni、Fe、NiO、FeO、Fe2O3以及少量其他不溶物,加入稀H2SO4后主要发生反应Ni+2H+===Ni2++H2↑、Fe+2H+===Fe2++H2↑、NiO+2H+===Ni2++H2O、FeO+2H+===Fe2++H2O、Fe2O3+6H+===2Fe3++3H2O,故“滤液②”中含有的金属离子是Ni2+、Fe2+、Fe3+。(3)H2O2的作用是在酸性条件下将Fe2+氧化为Fe3+(2Fe2++H2O2+2H+===2Fe3++2H2O),且在“转化”中不引入新杂质,故可替代H2O2的物质是O2或空气,发生反应4Fe2++O2+4H+===4Fe3++2H2O,也不引入新杂质。加NaOH溶液“调pH”的目的是生成Fe(OH)3沉淀除去Fe3+,为除尽Fe3+而又不生成Ni(OH)2沉淀,需控制pH范围:3.2≤pH<7.2;此时溶液中还存在Fe2+,H2O2可将Fe2+氧化为Fe3+,故“滤液③”中可能含有的杂质离子为Fe3+。(4)开始形成Ni(OH)2沉淀或沉淀完全时,都存在沉淀溶解平衡:Ni(OH)2(s)Ni2+(aq)+2OH-(aq),Ksp=c(Ni2+)·c2(OH-),开始沉淀时,c(Ni2+)=0.01mol·L-1,c(OH-)=1.0×107.2-14mol·L-1,故Ksp=0.01×(107.2-14)2;沉淀完全时,c(Ni2+)=1.0×10-5mol·L-1,c(OH-)=1.0×108.7-14mol·L-1,Ksp=10-5×(108.7-14)2。由上述分析得Ksp=1.0×10-15.6,若“转化”后的溶液中c(Ni2+)=1.0mol·L-1,生成Ni(OH)2沉淀的最小c(OH-)==mol·L-1=1.0×10-7.8mol·L-1,c(H+)=mol·L-1=1.0×10-6.2mol·L-1,pH=6.2,故既要除尽Fe3+,又不形成Ni(OH)2沉淀,应控制的pH范围是3.2~6.2。(5)Ni2+被氧化为NiOOH,ClO-被还原为Cl-,故在强碱溶液中该反应的离子方程式为2Ni2++ClO-+4OH-===2NiOOH↓+Cl-+H2O。(6)分离出NiSO4晶体后的母液中含有Ni2+(饱和NiSO4溶液),故将母液收集、循环使用,其意义是提高镍回收率。6.(1)+6(2)Al(OH)3( 3)①MoO+Ba2+===BaMoO4↓ ②×(4)①NaHCO3 ②NH3(5)①Al2O3 ②4:1解析:(1)根据化合物Na2MoO4中Na为+1价,O为-2价,由化合物中化合价代数和为0,可计算出Na2MoO4中Mo元素的化合价为+6。(2)“750℃焙烧”时,废催化剂中的氧化铝发生反应:Al2O3+2NaOH===2NaAlO2+H2O,“滤液Ⅰ”中主要存在NaAlO2和Na2MoO4,通入过量CO2时,发生反应:NaAlO2+CO2+2H2O===Al(OH)3↓+NaHCO3,生成的沉淀X为Al(OH)3。(3)由(2)的分析可知“滤液Ⅱ”的主要成分是NaHCO3和Na2MoO4。①“滤液Ⅱ”中加入BaCl2溶液生成BaMoO4的离子方程式为MoO+Ba2+===BaMoO4↓。②开始生成BaCO3时,溶液中==,又因为Ka2==4.7×10-11,由于“沉钼”中,pH为7.0,则==,因此可得=×。(4)①由于“滤液Ⅱ”的主要成分是NaHCO3和Na2MoO4,加入适量BaCl2溶液“沉钼”后,“滤液Ⅲ”中主要存在的钠盐有NaCl和NaHCO3,则Y为NaHCO3。②由“滤液Ⅲ”制备NaHCO3,原理类似侯氏制碱法,加入NaCl固体后,通入足量碱性气体NH3,再通入足量CO2,发生反应:NH3+H2O+CO2===NH4HCO3、NH4HCO3+NaCl===NaHCO3↓+NH4Cl,析出溶解度较小的NaHCO3固体。(5)①由题给芯片制造的刻蚀过程示意图可知,加入H2O2刻蚀液,GaAs逐渐溶解,当H2O2刻蚀液接触AlAs时,反应生成一种致密的氧化膜,由此可知,Ga、As均可溶于H2O2刻蚀液中,形成的致密氧化膜是AlAs中的铝被氧化为致密的Al2O3膜。②GaAs与H2O2反应时,As由-3价变为+5价,O由-1价变为-2价,由氧化还原反应中得失电子守恒规律可知,氧化剂(H2O2)与还原剂(GaAs)的物质的量之比为4:1。
相关试卷
这是一份新高考2024版高考化学一轮复习微专题小练习专练22化学工艺流程题,共7页。试卷主要包含了1),9%,5×10-6,8×10-6等内容,欢迎下载使用。
这是一份统考版2024版高考化学一轮复习微专题小练习专练22化学工艺流程,共7页。
这是一份全国通用高考化学一轮复习专练22化学工艺流程题含答案








