





化学选修4 化学反应原理第一单元 化学反应中的热效应说课课件ppt
展开
这是一份化学选修4 化学反应原理第一单元 化学反应中的热效应说课课件ppt,共21页。PPT课件主要包含了获得物质和能源,反应的焓变,放出能量放热反应,吸收能量吸热反应,吸热反应,放热反应,书写步骤,质→量→能,BCE,巩固练习等内容,欢迎下载使用。
问题讨论: 化学研究的目的是什么?
通过反应可以获得新物质也可以获得能源(化学反应中伴随着能量变化)
如何表示化学反应中的能量变化呢?
化学反应过程中,当反应物和生成物具有相同温度时,所吸收或放出的热量称为化学反应的反应热.
符号: ΔH ,单位:kJ/ml 或 kJ•ml-1
在恒温、恒压的条件下,化学反应过程中吸收或释放的热量称为反应的焓变
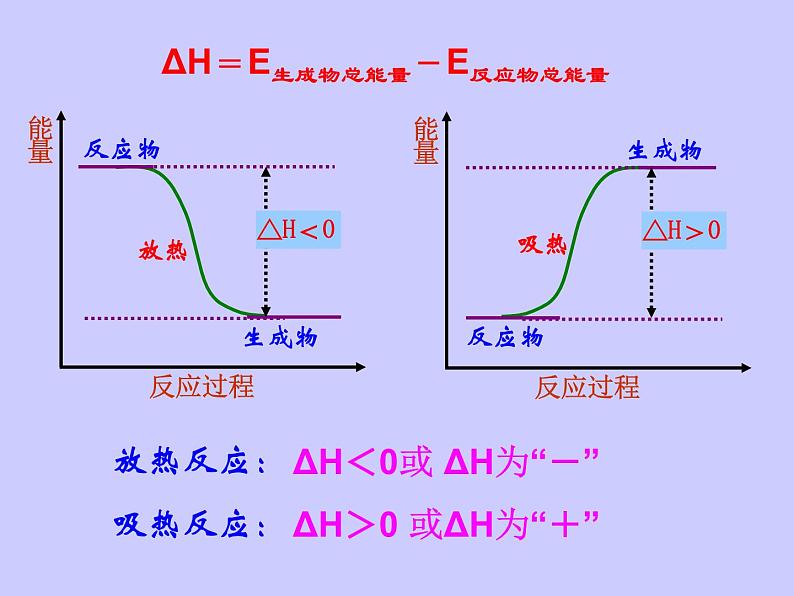
ΔH<0或 ΔH为“-”
ΔH>0 或ΔH为“+”
ΔH=E生成物总能量-E反应物总能量
规 律: E反:反应物的能量之和 E生:生成物的能量之和
(1)若E反> E生,
(2)若E反< E生,
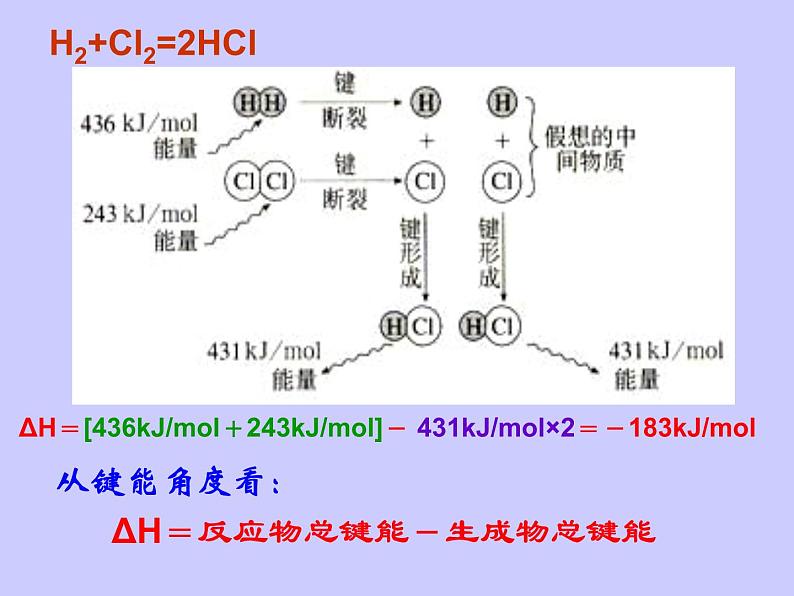
反应热:△H = E生- E反 吸热反应:△H >0或者ΔH为“-” 放热反应:△H 4Q3 B. 2Q1 + Q2 < 4Q3 C. Q1 + Q2 < Q3 D. Q1 + Q2 = Q3
3、在同温同压下,下列各组热化学方程式中Q2>Q1的是 ( )A.H2(g)+Cl2(g)=2HCl(g); △H1 =-Q1 1/2H2(g)+1/2Cl2(g)=HCl(g); △H2=-Q2B.C(s)+1/2O2(g)=CO (g); △H1=-Q1 C(s)+O2(g)=CO2 (g); △H2=-Q2C.2H2(g)+O2(g)=2H2O(l); △H1=-Q1 2H2(g)+O2(g)=2H2O(g); △H2=-Q2D.S(g)+O2(g)=SO2 (g); △H1=-Q1 S(s)+O2(g)=SO2 (g); △H2=-Q2
4、 1ml C与1ml 水蒸气反应生成1ml CO 和1ml H2,需要吸收 131.5 kJ的热量。写出此反应的热化学方程式。
相关课件
这是一份高中苏教版 (2019)第一单元 化学反应的热效应教学课件ppt,共33页。PPT课件主要包含了反应热与焓变,热化学方程式,从微观角度分析,典型例题,考题体验,标准燃烧热,例题体验,中和热等内容,欢迎下载使用。
这是一份化学选择性必修1专题1 化学反应与能量第一单元 化学反应的热效应完整版ppt课件,共21页。PPT课件主要包含了思考探究·一,习题探究,作业布置等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第一节 反应热精品ppt课件,共28页。PPT课件主要包含了Qcm△t,随堂小练等内容,欢迎下载使用。










