






2021学年课题2 溶解度示范课ppt课件
展开可溶物在一定量的水中能否无限溶解?
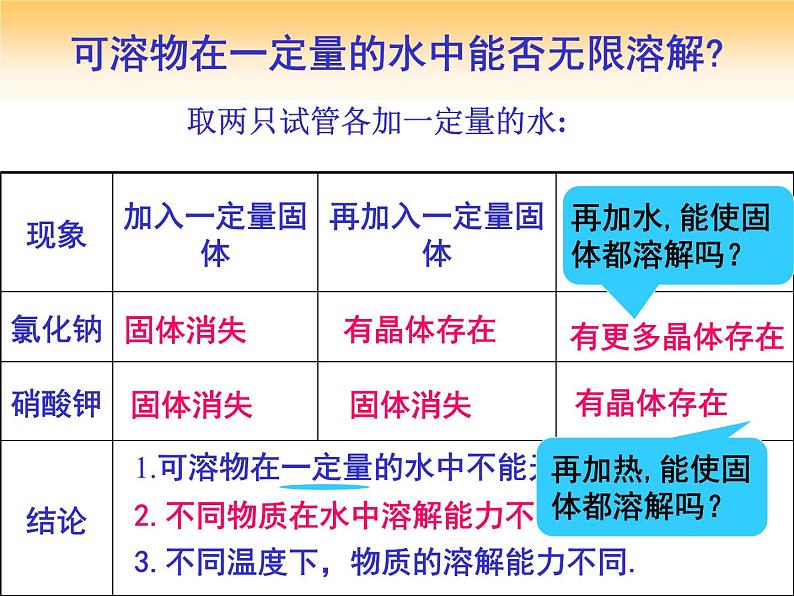
取两只试管各加一定量的水:
1.可溶物在一定量的水中不能无限溶解;
2.不同物质在水中溶解能力不一样;
3.不同温度下,物质的溶解能力不同.
1、饱和溶液(不饱和溶液)的前提条件是什么?2.在上面的前提条件下,关键看什么?3.为什么必须说明是“这种溶质”的饱和溶液?
一定温度、一定量的溶剂。
在上述条件下,还能继续溶解的溶液.
1.硝酸钾的饱和溶液能 继续溶解氯化钠
2.此液为硝酸钾饱和溶液
[练习] 20度时,将33克食盐放入100克水中,食盐全部溶解,此时溶液质量为 克,再向此溶液加入3克食盐又恰好全部溶解,则溶质为 克,现在溶液恰好饱和,此时溶液的质量为 克,再向此溶液加入3克食盐,溶液的质量是 克。
不饱和溶液 饱和溶液
在其它条件不变的情况下,要使接近饱和溶液的硝酸钾溶液达到饱和溶液,下列措施达不到目的的是: 1)降低溶液温度; 2)加入溶质硝钾; 3)升高溶液的温度; 4)蒸发溶液中的溶剂。
二、 溶液的相互转化:
指出下列各题的错误之处,并加以改正:1.不能再溶解某种溶质的溶液叫饱和溶液;2.装有饱和溶液的瓶的瓶底,一定有这种溶质的固体; 3.使一接近饱和的溶液变成饱和溶液,可将其中的溶 液倒出一些; 4.浓溶液一定是饱和溶液,稀溶液一定是不饱和溶液。
在一定温度.一定量的溶剂中,不能…….
不一定,有可能刚好达到饱和.
浓溶液不一定是饱和溶液
浓溶液不一定是饱和溶液,稀溶液不 一定是不饱和溶液。
但是, 在一定的温度下,同一物质的饱和溶液一定比不饱和溶液的浓度大。 即:在一定温度下,某物质的饱和溶液是它在该温度下最浓的溶液。
三、浓稀溶液与饱和溶液的关系:
思考:20℃时,氯化钠的饱和溶液的浓度为26.5%,能否配制出该温度下浓度为28%的溶液?
饱和溶液若继续降温或蒸发溶剂,会有 什么现象呢?
结晶方法
有晶体析出
P41:5.为什么汗水带咸味?被汗水浸湿的衣服晾干后,为什么常出现白色的斑痕?
6.有一瓶蒸馏水和一瓶稀氯化钾溶液,用什么简单的方法把它们区分开?
答:人分泌的汗水,是氯化钠溶液.因为溶有氯化钠,所以带咸味.凉干,是将水分蒸发,所以有氯化钠析出。
1.在一定______下,一定量的______里______再溶解某种溶质的溶液叫做这种溶质的饱和溶液。
2.要使饱和的石灰水变成不饱和溶液,可采取的措施有(1)______________;(2)______________。
3.30℃饱和硝酸钾溶液升高温度至100 ℃,则杯底____(有或无)晶体,则该100 ℃的硝酸钾溶液是______溶液(填饱和、不饱和)
4.在一定温度下,某物质的饱和溶液一定是A.很浓的溶液 B.很稀的溶液C.不能继续溶解该物质的溶液D.不能溶解任何物质的溶液.
5.某物质的饱和溶液中,加入一些该溶质的固体, 则下列说法正确的是A.溶质质量减少;B.溶液质量增大;C.固体质量不变;D.溶质质量增加.
6、在一定温度下,某物质的饱和溶液一定是:1)非常浓的溶液;2)增加该溶质,能继续溶解的溶液;3)非常稀的溶液;4)增加该溶质,不能继续溶解的溶液。
7.20℃时,往50克硝酸钾溶液中加入5克硝酸钾固体充分搅拌后,尚有部分固体未溶解,稍加热后固体全部溶解。下列说法正确的是A、搅拌后加热前一定是饱和溶液。B、搅拌后加热前一定是不饱和溶液。C、加热后一定是饱和溶液。D、加热后一定是不饱和溶液。
8.一定温度下,从500克的饱和溶液中倒出100克溶液,剩余的溶液里,下列数值比原溶液减少的是①溶质的质量; ②溶剂的质量; ③溶液的密度; ④溶液的质量; ⑤溶质的质量分数(即:浓度); A.①②③④ B.②③④⑤ C. ①②④ D.①②③④⑤
1、饱和溶液和不饱和溶液的定义、区别、判断方法和相互转化;
2、饱和溶液和浓溶液,不饱和溶液与稀溶液的关系。
饱和溶液 不饱和溶液
一、溶液 1、定义: 2、分类:(1)饱和溶液:在一定温度下,向一定量里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做饱和溶液。(2)不饱和溶液:在上述条件下,还能继续溶解的溶液,叫做不饱和溶液。 3、结晶方法: 降温结晶;蒸发结晶。
4、饱和溶液和不饱和溶液的相互转化关系
1、溶解度是指在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
(1)20℃时氯化钠的溶解度为36克,含义?20℃时,在100克水中溶解36克氯化钠刚好达饱和状态。或在20ºC时,在100克水中最多能溶解36克氯化钠。(2)20℃时,硝酸钾的溶解度为31.6克,含义?20℃时,31.6克硝酸钾溶解在100克水中刚好达饱和状态。(3)20℃时,50克水中最多能溶解15.8克硝酸钾,问:20℃时,硝酸钾的溶解度是多少?
[课堂练习] 1.20℃时100克水中最多能溶解36克食盐,据此下列叙述正确的是 …………( )A. 食盐的溶解度是36℃ B.20℃时食盐的溶解度是36克C.食盐的溶解度是100克 D.食盐的溶解度是36克
2.判断下列说法是否正确,并指明错误原因。①把20克某物质溶解在100克水里恰好制成饱和溶液,这种物质的溶解度就是20克。( )②20℃时10克氯化钠溶解在水里制成饱和溶液,故20℃时氯化钠的溶解度是10克。( )③20℃时10克氯化钠可溶解在100克水里,故20℃时氯化钠的溶解度是10克。( )④20℃时36克食盐溶解在100克水中恰好饱和,故20℃时食盐的溶解度是36。( ) 20℃时,硝酸钾的溶解度为31.6克,表示20℃时,100g硝酸钾溶液中含有31.6克硝酸钾
3.在60℃时50克水中溶解硝酸钾55克恰好饱和。下列叙述正确的是 ………( )A.硝酸钾的溶解度是55克 B.硝酸钾的溶解度是110克C. 60℃时硝酸钾的溶解度是55克 D.60℃时硝酸钾的溶解度是110克
2、溶解度与溶解性的关系:(室温时,即20℃)
(1)20℃时,50克水中最多能溶解某物质0.8克,则这种物质属于( )A、难溶物质 B、微溶物质 C、可溶物质 D、易溶物质(2)20℃时,20克水中最多能溶解5克某物质,则这种物质的溶解度是多少克?
(1)内因: (2)外因:
3、影响固体溶解度的因素
4、固体溶解度曲线及意义
点:曲线上的点均表示某物质在该温度下的溶解度。
交点:曲线的交点表示这两种物质在该温度下的溶解度相同。
曲线:曲线越陡,该物质的溶解度受温度影响越大。
40℃时,硝酸钠的溶解度为110克。
70 ℃时,硝酸钠和硝酸钾溶解度相同,都是140克。
讨论: 固体物质溶解度与温度变化关系:
大多数固体物质溶解度随温度升高而增大,例如硝酸钾等。
少数固体物质溶解度受温度影响变化不大,例如氯化钠。
极少数固体物质溶解度随温度升高反而减小,例如熟石灰。
饱和石灰水 不饱和石灰水
1、固体溶解度: 在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。2、影响固体溶解度的因素: (1)内因……;(2)外因……3、固体物质溶解度与温度变化关系: 大多数……;少数……;极少数……4、固体溶解度曲线上点的意义
练习:判断下列说法是否正确
1、在20ºC时,100克水中溶解了23克食盐,则食盐在20ºC时的溶解度为23克。2、在20ºC时,100克溶液中含有溶质23克,则该物质的溶解度为23克。3、在100克水中最多能溶解NaCl36.5克,则氯化钠的溶解度为36.5克。4、在20ºC时,在100克水中最多能溶解NaCl36.5克,则20ºC时,氯化钠的溶解度为36.5克
例:如图是A、B、C三种物质在水中的溶解度曲线,回答:(1)t1℃时,A、B、C的溶解度由大到小的顺序 。 (2)t3℃时,A、B、C的溶解度大小 。(3)M点的含义是 。 (4) t2℃、 t3℃两温度下,A的溶解度大小
t2℃时,A、C溶解度相等
溶解度大小比较的条件:
①温度相同时,必须不同种溶质进行比较;
②温度不同时,必须同种溶质进行比较。
1、定义: 在一定温度时,在压强为101KPa时,某气体溶解在1体积水中达饱和状态时所溶解的气体体积。
(1)20℃时,氮气的溶解度为0.024,含义? 在压强为101KPa和20 ℃时,1体积水里溶解0.024体积的氮气刚好达饱和状态。 (2)t℃时,氧气的溶解度为0.036,含义?
(1)内因: (2)外因:
2、影响气体溶解度的因素
即: 当压强一定时,气体溶解度一般随温度升高而减小;随温度下降而增大;
(气体溶解度与温度成反比,与压强成正比)
当温度一定时,气体溶解度一般随压强升高而增大;随压强减小而减小。
1、利用所学知识解释下列现象?①打开健力宝盖时我们为何会看到有气体冒出?②给水加热时我们为何可以看到水中出现气泡?
2、增大二氧化碳在水中的溶解度的方法( ) A、升温增压 B、升温减压 C、降温增压 D、降温减压
3、下列几种物质:①硝酸钾②熟石灰③氧气④二氧化碳,溶解度随温度的升高而增大的是( ) A、①② B、③④ C、①③④ D、只有①
初中化学人教版九年级下册第九单元 溶液课题2 溶解度精品课件ppt: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c9866_t3/?tag_id=26" target="_blank">第九单元 溶液课题2 溶解度精品课件ppt</a>,共60页。PPT课件主要包含了饱和溶液,不饱和溶液,曲线上点的含义,abc,bac等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度教学课件ppt: 这是一份初中化学人教版九年级下册课题2 溶解度教学课件ppt,共8页。PPT课件主要包含了探究问题,实验9-5,实验9-6,实验探究,剩余固体全部溶解,全部溶解,有固体剩余,有晶体析出,实验讨论,饱和溶液等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度课前预习ppt课件: 这是一份初中化学人教版九年级下册课题2 溶解度课前预习ppt课件,共8页。PPT课件主要包含了溶解度,溶解度四大理解要点,01g,P37活动与探究,几种物质的溶解度曲线等内容,欢迎下载使用。













