
海南省海口市2021届高三下学期5月高考调研测试化学试题(二模)含答案
展开
这是一份海南省海口市2021届高三下学期5月高考调研测试化学试题(二模)含答案,共9页。试卷主要包含了设NA为阿伏加德罗常数的值等内容,欢迎下载使用。
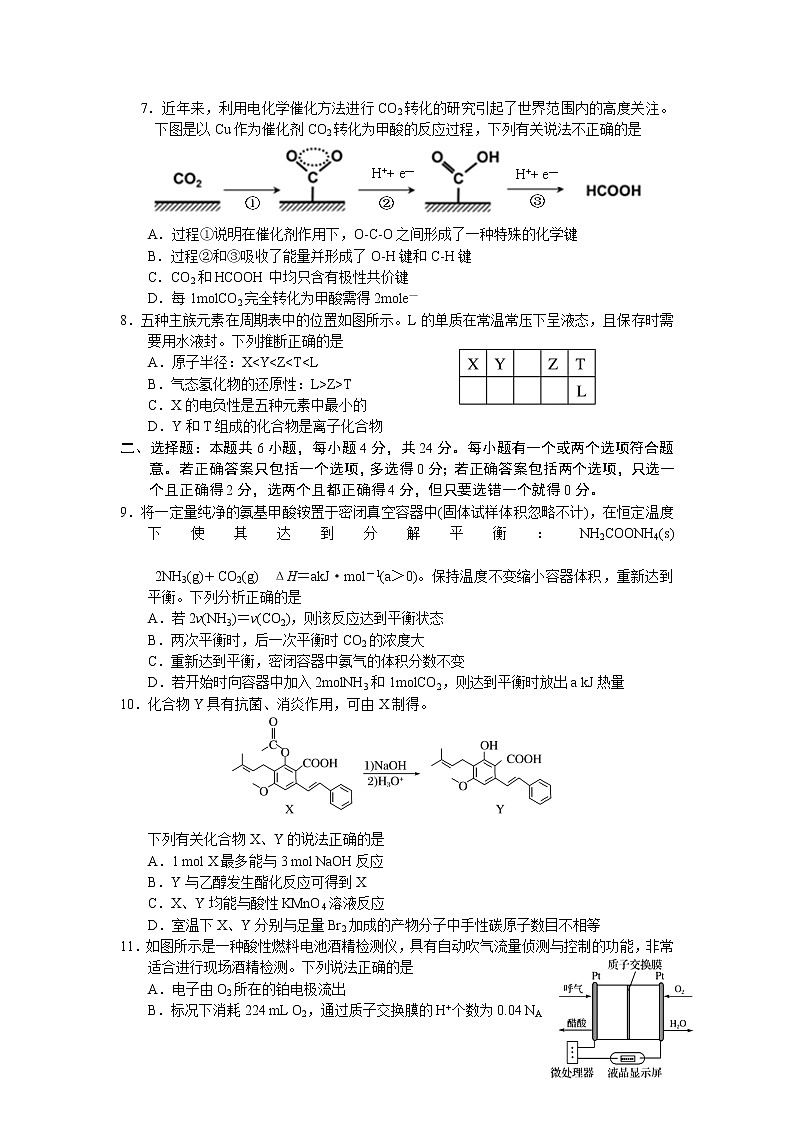
海口市2021年高考调研测试化学试卷注意事项:1.答卷前,考生务必将自己的姓名、班级、准考证号填写在答题卡上。2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。3.考试结束后,将本试卷和答题卡一并交回。可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 Cl 35.5 Ni 59一、选择题:本题共8小题,每小题2分,共16分。在每小题给出的四个选项中,只有一项是符合题目要求的。1.改革开放40年,我国取得了很多世界瞩目的科技成果,下列说法不正确的是A.蛟龙号潜水器用到钛合金,22号钛元素属于过渡元素B.中国天眼传输信息用的光导纤维材料是硅单质C.国产C919用到的氮化硅陶瓷是新型无机非金属材料D.港珠澳大桥用到的合金材料,具有强度大、密度小、耐腐蚀等性能 2.下列化学用语表达不正确的是A.乙烯的实验式:CH2 B.氨气的电子式: C.次氯酸的结构式:H-Cl-O D.2-甲基丁烷的键线式:3.化学在生活中有着广泛的应用,下列说法正确的是A.利用溶解度不同,可用水鉴别乙酸和乙酸乙酯B.根据淀粉的特性,木材纤维和土豆淀粉遇碘水均显蓝色C.脱脂棉、滤纸、蚕丝的主要成分均为纤维素,完全水解能得到葡萄糖 D.蛋白质溶液中加入 (NH4)2SO4、CuSO4溶液均能凝结析出,加水后又能溶解4.实验室完成下列操作,一般不宜使用锥形瓶的是 A.实验室制蒸馏水 B.酸碱中和滴定 C.配制一定浓度的H2SO4溶液 D.用高锰酸钾与浓盐酸制Cl25.设NA为阿伏加德罗常数的值。下列说法正确的是A.1 L 0.1 mol·L-1 NaClO溶液中含有ClO-的数目为0.1NAB.将1 mol NH3完全溶于水,所得溶液中n(NH3·H2O)+n(NH4+)=NAC.1 L 0.1 mol·L-1 NaHSO4溶液中含有的阳离子数目为0.1NA D.将1 mol CH3COONa溶于稀醋酸中使溶液呈中性,溶液中含CH3COO-数目为NA6.硫元素的几种化合物存在下列转化关系: 下列判断不正确的是A.反应①中浓硫酸作氧化剂 B.反应②表明SO2有酸性氧化物的性质C.反应③的原子利用率是100% D.反应④稀H2SO4作还原剂7.近年来,利用电化学催化方法进行CO2转化的研究引起了世界范围内的高度关注。下图是以Cu作为催化剂CO2转化为甲酸的反应过程,下列有关说法不正确的是 A.过程①说明在催化剂作用下,O-C-O之间形成了一种特殊的化学键B.过程②和③吸收了能量并形成了O-H键和C-H键C.CO2和HCOOH中均只含有极性共价键D.每1molCO2完全转化为甲酸需得2mole—8.五种主族元素在周期表中的位置如图所示。L的单质在常温常压下呈液态,且保存时需要用水液封。下列推断正确的是A.原子半径:X<Y<Z<T<L B.气态氢化物的还原性:L>Z>TC.X的电负性是五种元素中最小的 D.Y和T组成的化合物是离子化合物二、选择题:本题共6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得2分,选两个且都正确得4分,但只要选错一个就得0分。9.将一定量纯净的氨基甲酸铵置于密闭真空容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g) ΔH=akJ·mol-1(a>0)。保持温度不变缩小容器体积,重新达到平衡。下列分析正确的是A.若2v(NH3)=v(CO2),则该反应达到平衡状态B.两次平衡时,后一次平衡时CO2的浓度大C.重新达到平衡,密闭容器中氨气的体积分数不变D.若开始时向容器中加入2molNH3和1molCO2,则达到平衡时放出a kJ热量10.化合物Y具有抗菌、消炎作用,可由X制得。下列有关化合物X、Y的说法正确的是A.1 mol X最多能与3 mol NaOH反应B.Y与乙醇发生酯化反应可得到XC.X、Y均能与酸性KMnO4溶液反应D.室温下X、Y分别与足量Br2加成的产物分子中手性碳原子数目不相等11.如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法正确的是 A.电子由O2所在的铂电极流出 B.标况下消耗224 mL O2,通过质子交换膜的H+个数为0.04 NA C.电池的负极反应式为CH3CH2OH+3H2O–12e− = 2CO2↑+12H+ D.微处理器通过检测电流大小而计算出被测气体中酒精的含量 12.下列离子方程式正确的是A.过量的铁粉溶于稀硝酸:Fe+4H++NO3—= Fe3++NO↑+2H2OB.澄清石灰水与少量小苏打溶液混合:Ca2++OH—+HCO3—=CaCO3↓+H2OC.用惰性电极电解MgCl2溶液:2Cl—+2H2O ==== Cl2↑+H2↑+2OH—D.室温下,氯化铵溶液pH<7的原因:NH4++H2O = NH3·H2O+H+13.下列物质的性质变化规律与与键能无关的是
A.与硅相比,金刚石的硬度大、熔点高
B.HF、HCl、HBr、HI热稳定性依次减弱
C.F2、Cl2、Br2、I2的沸点逐渐升高
D.H2、O2、H2S在水中的溶解性依次为难溶、微溶、可溶14.探究铝片与Na2CO3溶液的反应。无明显现象铝片表面产生细小气泡出现白色浑浊,产生大量气泡(经检验为H2和CO2)下列说法不正确的是A.Na2CO3溶液中存在水解平衡:CO32— + H2O HCO3—+ OH—B.对比Ⅰ、Ⅲ,说明Na2CO3溶液能破坏铝表面的保护膜C.推测出现白色浑浊的原因:AlO2— + HCO3—+ H2O = Al(OH)3↓+ CO32—D.加热和H2逸出对CO32—水解平衡移动方向的影响是相反的三、非选择题:共5题,60分。15.(10分)次磷酸钠(NaH2PO2)广泛应用于化学镀镍,次磷酸钠的生产与镀镍过程如下: 据此回答下列问题:(1)红磷与黄磷之间的关系为_____________________。(2)次磷酸钠中磷元素的化合价为______________。(3)写出碱溶过程的化学反应方程式________________________________________,该反应中氧化剂与还原剂物质的量之比为_________________。(4)已知次磷酸钠中的H2PO2—为四面体结构,请写出H2PO2—的结构式 , 次磷酸钠NaH2PO2为____________填“酸式盐”、“碱式盐”、“正盐”。(5)请简述化学镀镍的反应原理 。16.(10分)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:(1)Deacon直接氧化法可按下列催化过程进行:CuCl2(s)===CuCl(s)+Cl2(g) ΔH1=+83 kJ·mol-1CuCl(s)+O2(g)===CuO(s)+Cl2(g) ΔH2=-20 kJ·mol-1CuO(s)+2HCl(g)===CuCl2(s)+H2O(g) ΔH3=-121 kJ·mol-1则4HCl(g)+O2(g)===2Cl2(g)+2H2O(g)的ΔH=________kJ·mol-1。(2)Deacon发明的直接氧化法原理为:4HCl(g)+O2(g)===2Cl2(g)+2H2O(g),在刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系如图所示: 据图像分析可知:反应平衡常数K(300 ℃)________K(400 ℃)(填“大于”或“小于”)。(3)设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=1∶1的数据,计算K(400 ℃)=______(列出计算式)。(4)按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O2)过低、过高的不利影响分别是______________、_____________。在一定温度的条件下,进一步提高HCl的转化率的方法是___________。(写出2种)17.(12分)二氯异氰尿酸钠[(CNO)3Cl2Na]是常用的杀菌消毒剂,常温下为白色固体,难溶于冷水。某同学利用高浓度的NaClO溶液和(CNO)3H3固体,在10℃时反应制备二氯异氰尿酸钠,实验装置如下图所示(部分夹持装置略)。 已知:2NaClO + (CNO)3H3 = (CNO)3Cl2Na + NaOH + H2O 回答下列问题:(1)仪器a的名称为恒压滴液漏斗,与分液漏斗相比其优点是 。(2)待装置B中出现 现象时,可由三颈烧瓶上口加入(CNO)3H3固体;反应过程中仍需不断通入 Cl2的理由是 。 (3)反应结束后,装置B中的浊液经过滤、 、干燥得粗产品。上述装置存在一处缺陷会导致装置B中NaOH利用率降低,改进的方法是 。 (4)通过下列实验测定二氯异氰尿酸钠样品中有效氯的含量。 反应原理: [(CNO)3Cl2]—+ H+ +2H2O = (CNO)3H3 + 2HClO, HClO + 2I— + H+ = I2 + Cl—+ H2O, I2 + 2S2O32—= S4O62—+ 2I—实验步骤:准确称取m g样品,用容量瓶配成250 mL溶液;取25.00 mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,充分反应后,用 c mol/L Na2S2O3标准溶液滴定至溶液呈微黄色。加入淀粉指示剂继续滴定至终点,消耗Na2S2O3溶液平均为 V mL。 ①滴定终点现象为 。 ②该样品的有效氯含量表达式为 。 18.(14分)2-氨-3-氯苯甲酸是白色晶体,是重要的医药中间体,其制备流程如下: 回答下列相关问题(1) 的名称是___________。反应②的反应类型为___________。(2)为了实现反应③的转化,通常可采用的试剂是___________。(3)生成2-氨-3-氯苯甲酸的方程式为____________________。(4)同时符合下列两个条件的有机物共有________种同分异构体。其中仅有3种等效氢的有机物结构简式为___________。①相对分子质量比大42的苯的同系物;②与酸性KMnO4反应能生成二元羧酸; (5)事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。请从步骤⑥产率低的原因进行推测,上述过程能提高产率的原因可能是 。若想要进一步提高产率,2-氨-3-氯苯甲酸的合成流程中,可以优化的步骤还有 。19.(14分)金属Ni可以与Mg、C形成一种化合物M,M是一种新型超导体,它的临界温度为8K。回答下列问题:(1)在基态Mg原子中,核外存在________对自旋相反的电子。(2)碳在矿物中,通常以碳酸盐形式存在。根据价层电子对互斥理论,可推知CO32—的空间构型为 ________,其中碳原子的杂化轨道类型为_________。NaHCO3的溶解度比Na2CO3的小,其原因是HCO3—在水溶液中易形成多聚离子,请解释HCO3—形成多聚离子的原因是 。(3)Ni的基态原子的价层电子排布式为 。区分晶体Ni和非晶体Ni的最可靠的科学方法为 。向绿色的NiSO4溶液中滴加过量的氨水,溶液会变成深蓝色,其原因是溶液中生成了一种六配体的配离子,该配离子的化学式为 。(4)已知M的晶胞(α = β = γ = 90°)结构如下图所示,则M的化学式为 。其晶胞参数为:a = b = c = d pm,该晶体的密度为 g·cm-3。(列出计算式) 海口市2021年高考调研测试化学参考答案 一、选择题:本题共8小题,每小题2分,共16分。在每小题给出的四个选项中,只有一项是符合题目要求的。题号12345678答案BCACDDBC 二、选择题:本题共6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得2分,选两个且都正确得4分,但只要选错一个就得0分。题号91011121314答案CACBDBCDD 三、非选择题:共60分。15.(10分)(1)同素异形体 (1分)(2)+1 (1分) (3) (2分) 1:3 (1分) (4) (2分) 正盐 (1分)(5)次磷酸钠作为还原剂将硫酸镍中的镍还原成金属单质,沉积在镀件表面。(2分)16.(10分)(1) -116 (2分)(2)大于 (2分)(3) (2分)(4)O2和Cl2分离能耗较高(1分) HCl转化率较低 (1分) 增加反应体系压强、及时除去产物(2分)17.(12分)(1)恒压分液漏斗的支管可以使漏斗下方与漏斗中的压强一致,可以使漏斗内液体顺利流下。(2分)(2)液面上方有黄绿色气体 (1分) 使反应生成的 NaOH再次生成 NaClO,提高原料的利用率(2分) (3)冰水洗涤 (1分) 在装置 A、B之间加装盛有饱和食盐水的洗气瓶(2分)(4)①滴入最后一滴标准液时,锥形瓶内溶液蓝色刚好褪去(或颜色恰好由蓝色变成无色),且半分钟不恢复(2分)②(2分)18.(14分)(1)邻硝基苯甲酸(2-硝基苯甲酸)(1分) 取代(硝化)反应(1分) (2)酸性高锰酸钾溶液(其他合理答案也可给分) (2分)(3) (2分) (4) 9(2分); (2分) (5) 利用磺酸基占位,减少5号位上H原子的取代(2分) 步骤②(2分)19.(14分)(1)6(1分)(2)平面三角形(1分) sp2 (1分) HCO3—中的—OH可以与另一HCO3—中的氧原子形成氢键,故可形成多聚体(2分) (3)3d84s2 (2分) X射线衍射法(1分) [Ni(NH3)6]2+(2分)(4)MgCNi3 (2分) (2分)
相关试卷
这是一份海南省海口市2023届高三下学期一模联考化学试题(含解析),共21页。试卷主要包含了单选题,多选题,工业流程题,原理综合题,实验题,有机推断题等内容,欢迎下载使用。
这是一份海南省海口市海南华侨中学2023届高三下学期二模考试化学试题(含答案),共10页。试卷主要包含了单选题,多选题,工业流程题,原理综合题,实验题,有机推断题,结构与性质等内容,欢迎下载使用。
这是一份海南省海口市海南华侨中学2023届高三下学期二模考试化学试题(含解析),共19页。试卷主要包含了单选题,多选题,工业流程题,原理综合题,实验题,有机推断题,结构与性质等内容,欢迎下载使用。







