
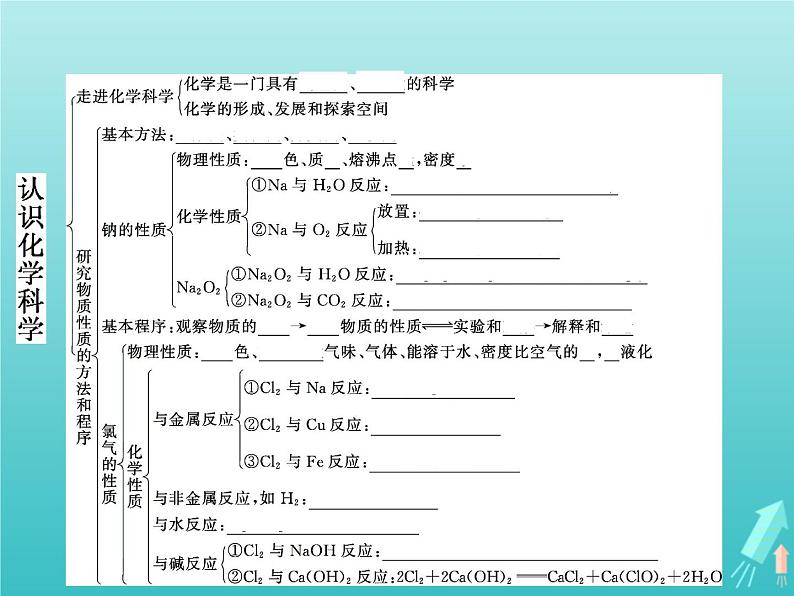
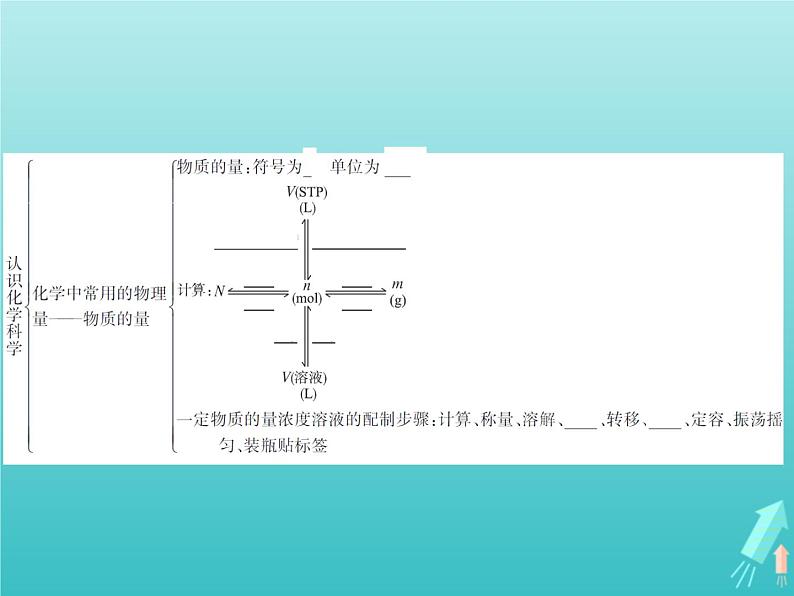





鲁科版必修1第1章 认识化学科学综合与测试课堂教学课件ppt
展开阿伏加德罗常数的应用
通过阿伏加德罗常数可以将物质的质量、气体的体积、物质的量等物理量与微粒数联系起来,在科研、生产中的使用非常广泛,因此阿伏加德罗常数及其应用一直是高考的热点,解答题目时需注意以下几点:(1)物质的状态,如水在标准状况下不是气态。(2)某些物质分子中的原子个数,如Ne、O3、白磷(P4)等。(3)要用到22.4 L·ml-1时,必须注意气体是否处于标准状况下。(4)混合气体中的原子数目和分子数目。(5)给出一定质量的气体,同时又给出“标准状况”等。
【应用举例】设阿伏加德罗常数的数值为NA,下列说法正确的是( )A.1 g氢气含有NA个H2分子B.常温下22.4 L水含有NA个H2O分子C.在0 ℃、101 kPa时,22.4 L氢气中含有NA个氢原子D.NA个一氧化碳分子和0.5 ml甲烷的质量比为7∶2解析:1 g氢气的物质的量为0.5 ml,故含H2分子数为0.5NA,A选项错误;水在常温下为液态,B选项错误;0 ℃、101 kPa时,22.4 L氢气的物质的量为1 ml,含有2NA个氢原子,C选项错误;NA个CO的质量为28 g,0.5 ml甲烷的质量为8 g,质量之比为28∶8=7∶2,故D选项正确。答案:D
物质的量应用于化学方程式的计算方法
1.化学方程式中化学计量数的含义化学方程式 H2 + Cl2 2HCl化学计量数之比为1∶1 ∶2分子个数比为1∶1 ∶2扩大NA倍之比为NA∶NA ∶2NA物质的量之比为1 ml∶1 ml ∶2 ml所以,对于该反应来说,可以理解为1 ml H2和1 ml Cl2在点燃条件下恰好完全反应生成2 ml HCl。
2.反应中各物质的物理量之间的比例关系 aA(g)+bB(g) cC(g)+dD(g)化学计量数之比为 a∶ b ∶ c∶ d质量之比为 aMA∶ bMB ∶ cMC∶ dMD物质的量之比为 a∶ b ∶ c∶ d气体体积之比为 a∶ b ∶ c∶ d
不同物质的相同物理量之间的换算可以按上述比例进行。解题时要注意化学方程式中对应关系的单位问题。一般来说,在一个题目里如果都用统一的单位,不会出现错误,但如果题目所给的两个物理量单位不一致,再换算成同一个单位,有时显得很烦琐,这时只要做到两个物理量的单位“上下一致,左右相当”即可,例如:
3.有关过量的计算(1)过量计算的原则:物质发生化学反应是按化学方程式中确定的比例关系进行的,若题目给出两个或两个以上反应物的量,则应先判断反应物谁过量,然后按不足量的反应物的量进行计算。(2)反应物过量的判断方法:方法一:先求出给定反应物的物质的量之比,与化学方程式中相应反应物的化学计量数之比比较,进行过量判断。方法二:假设其中一种反应物不足,完全反应,求另一反应物的量,然后把另一反应物的所求量与已知量相比较。若所求量小于已知量,说明假设正确;若所求量大于已知量,说明假设不正确。
【应用举例】将13.0 g锌投入400 mL 1.25 ml·L-1的盐酸中,锌和盐酸恰好完全反应。求:(1)13.0 g锌的物质的量为 ml; (2)反应中生成的H2在标准状况下的体积为 L; (3)反应后所得溶液中ZnCl2的物质的量浓度为 ml·L-1(反应前后溶液体积变化忽略不计)。
答案:(1)0.2 (2)4.48 (3)0.5
有关物质的量浓度计算思维的起点
物质的量浓度的计算是中学化学计算的重要组成部分,是近年各类考试的“热点”,此类题涉及的概念较多(如物质的量、质量、摩尔质量、气体的摩尔体积等),知识范围广,内容灵活多变,解题过程中不少同学感到无所适从。其中最主要的原因是不会选解题的思维起点。所以我们通过对具体的例题剖析,讲解有关物质的量浓度计算中思维起点的选择。
1.从“定义式”出发物质的量浓度的定义的数学表达式为 ,其中n为溶质的物质的量(ml),V为溶液的体积(L),c的单位为ml·L-1。由此可知,欲求c,应先分别求出n及V。
【应用举例1】100 mL 0.3 ml·L-1 Na2SO4溶液和50 mL 0.2 ml·L-1 Al2(SO4)3溶液混合后,溶液中 的物质的量浓度为( )A.0.2 ml·L-1 ml·L- ml·L-1 ml·L-1
2.从“换算式”出发溶质的物质的量浓度与溶质的质量分数之间的换算公式为其中ρ为溶液的密度(g·cm-3),w为溶质的质量分数,M为溶质的摩尔质量(g·ml-1),由上述公式可知,已知ρ、w、M,就可以求出c。
【应用举例2】将溶质的质量分数为a%、物质的量浓度为c1 ml·L-1的稀硫酸加热蒸发掉一定量的水,使溶质的质量分数变为2a%,此时硫酸的物质的量浓度为c2 ml·L-1,则c1和c2的数值关系是( )A.c2=2c1B.c2<2c1C.c2>2c1D.c1=2c2
解析:由换算公式 得c1=1 000×ρ1×a%÷98,c2=1 000×ρ2×2a%÷98,由此可知:c1∶c2=ρ1∶2ρ2,因为ρ2>ρ1,故有c2>2c1。
高中化学鲁科版 (2019)必修 第一册第1节 走进化学科学授课ppt课件: 这是一份高中化学鲁科版 (2019)必修 第一册第1节 走进化学科学授课ppt课件,文件包含鲁科版高中化学必修第一册第1章认识化学科学本章整合课件ppt、鲁科版高中化学必修第一册第1章认识化学科学测评试题含答案doc等2份课件配套教学资源,其中PPT共42页, 欢迎下载使用。
高中化学鲁科版必修1第1章 认识化学科学综合与测试课前预习ppt课件: 这是一份高中化学鲁科版必修1第1章 认识化学科学综合与测试课前预习ppt课件,共20页。PPT课件主要包含了专题1,专题2,专题3,答案C等内容,欢迎下载使用。
鲁科版必修1第4章 材料家族中的元素综合与测试课堂教学课件ppt: 这是一份鲁科版必修1第4章 材料家族中的元素综合与测试课堂教学课件ppt,共18页。PPT课件主要包含了专题1,专题2,铝及其化合物的性质,工艺流程题解题技巧等内容,欢迎下载使用。













