




精品解析:2020年河南省新乡市辉县市中考二模化学试题(解析版+原卷版)
展开2020年河南省普通高中招生考试模拟试卷
化学
注意事项:
1.本试卷分试题卷和答题卡两部分,试题卷共4页,四大题,满分50分,考试时间50分钟。
2.答卷前将装订线内的项目填写清楚。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 A1-27 P-31 C135.5 Fe-56 Cu-64 Ag-108
一、选择题(14个小题,每小题1分,共14分。)
1. 我们生活在不断变化的物质世界里。下列变化一定属于化学变化的是
A. 用干冰进行人工降雨 B. 铁制品在潮湿空气中生锈
C. 用空气作原料制取氧气 D. 固体物质加热后全部变成气体
【答案】B
【解析】
A、用干冰进行人工降雨是利用干冰升华吸热,使周围温度降低,水蒸气冷凝成水滴,属于物理变化,故A错;B、铁制品在潮湿空气中生锈,生成了主要成分是氧化铁的新物质,属于化学变化,故B正确;C、用空气作原料制取氧气是利用分离液态空气法,属于物理变化,故C错;D、固体物质加热后全部变成气体,可能是化学变化,也可能是物理变化,故D错。故选B。
点睛:正确区别物理变化和化学变化关键是判断是否有新物质的生成,方法是比较变化前后物质的差别:是只限于物质的状态变化,还是物质发生了根本变化。
2. 2019年12月3日,世界气象组织(WMO)指出2019年1月至10月期间,全球平均温度较工业化前水平升高约1.1℃。如果任由温室气体继续排放到大气中,将会对多方面带来更严峻的威胁。下列做法与低碳环保理念一致的是( )
A. 垃圾分类回收,增强节约意识
B. 鼓励开私家车,带动经济发展
C. 燃放烟花爆竹,增添节日气氛
D. 为了方便卫生,使用一次性餐具
【答案】A
【解析】
【分析】
【详解】A、垃圾回收有利于物质循环使用,增强节约意识可以减少浪费,二者均与低碳环保理念一致,符合题意;
B、鼓励开私家车加大汽油的使用量,增加二氧化碳的排放,不符合题意;
C、燃放烟花爆竹会导致空气污染,不符合题意;
D、使用一次性餐具,会导致资源浪费和环境污染,不符合题意。
故选:A。
3. 2019年诺贝尔化学奖颁给了锂电池研发的领域。锂元素在元素周期表中的相关信息如图所示,下列说法正确的是
A. 锂属于金属元素,在化学反应中易得一个电子
B. 锂原子的中子数为3
C. 地壳中锂的含量为6.941%
D. 锂元素在化合物中显+1价
【答案】D
【解析】
【详解】A、锂带“钅”字旁,属于金属元素;最外层电子数是1,在化学反应中易失去1个电子而形成阳离子,故选项说法错误。
B、根据元素周期表中的一格可知,左上角的数字为3,表示原子序数为3;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数和核外电子数为3,而不是中子数为3,故选项说法错误。
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为6.941,而不是地壳中锂的含量为6.941%,故选项说法错误。
D、锂原子的最外层电子数为1,在化学反应中易失去1个电子而形成带1个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+1价,故选项说法正确。
故选:D。
4. (NH4)2SO4是一种化肥,其溶液的pH<7,下列有关该化肥的说法正确的是( )
A. 是一种复合肥
B. 长期使用不会使土壤酸化
C. 能与碱性物质混合施用
D. 能促使植物茎、叶生长
【答案】D
【解析】
【分析】
【详解】A、含有氮、磷、钾中的两种或是那种元素的化学肥料,叫做复合肥,(NH4)2SO4只含有氮元素,属于氮肥,不属于复合肥,说法错误,不符合题意;
B、(NH4)2SO4溶液的pH<7,长期使用会导致土壤酸化,说法错误,不符合题意;
C、铵态氮肥与碱反应生成氨气,降低肥效,不能和碱性物质混合使用,说法错误,不符合题意;
D、(NH4)2SO4只含有氮元素,属于氮肥,氮肥能促使作物的茎和叶的生长茂盛,叶色浓绿,说法正确,符合题意。
故选:D。
5. 玻璃棒是化学实验的常用仪器,下列实验过程中不需要使用玻璃棒的是( )
A. 稀释浓硫酸
B. 用量筒量取一定体积的水
C. 蒸发氯化钠溶液
D. 除去悬浮在河水中的不溶物
【答案】B
【解析】
【分析】
【详解】A、溶液的稀释时,使用玻璃棒搅拌可以加快物质的混溶,使热量迅速散失,不符合题意;
B、用量筒量取一定量的液体可以采用:倾倒法和滴加法两种方法,不需要使用玻璃棒,符合题意;
C、蒸发溶液时,使用玻璃棒搅拌可以使溶液均匀受热,不符合题意;
D、除去悬浮在河水中的不溶物,需要采用过滤的方法,操作过程中玻璃棒可以用来引流,不符合题意。
故选:B。
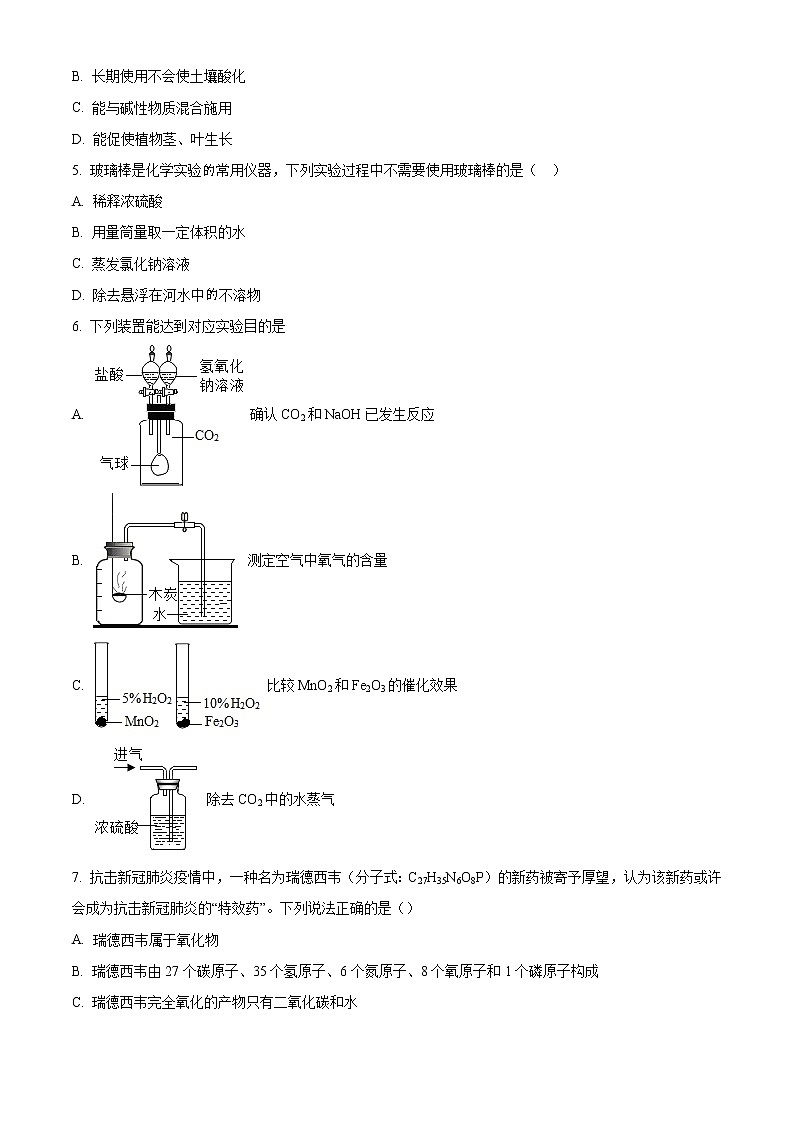
6. 下列装置能达到对应实验目的是
A. 确认CO2和NaOH已发生反应
B. 测定空气中氧气的含量
C. 比较MnO2和Fe2O3的催化效果
D. 除去CO2中的水蒸气
【答案】A
【解析】
【详解】A、先滴加适量氢氧化钠溶液,后滴加足量稀盐酸,产生气泡,是因为氢氧化钠和二氧化碳反应生成了碳酸钠,碳酸钠和盐酸反应生成了二氧化碳,该选项能够达到实验目的;
B、木炭燃烧生成二氧化碳,瓶内的气压几乎不降低,导致水不能进入集气瓶,不能测定氧气含量,该选项不能达到实验目的;
C、由于过氧化氢溶液浓度不同,不能比较MnO2和Fe2O3的催化效果,该选项不能达到实验目的;
D、除去二氧化碳中的水蒸气时,气体应该从右边长导管导入,该选项不能达到实验目的。
故选:A。
7. 抗击新冠肺炎疫情中,一种名为瑞德西韦(分子式:C27H35N6O8P)的新药被寄予厚望,认为该新药或许会成为抗击新冠肺炎的“特效药”。下列说法正确的是()
A. 瑞德西韦属于氧化物
B. 瑞德西韦由27个碳原子、35个氢原子、6个氮原子、8个氧原子和1个磷原子构成
C. 瑞德西韦完全氧化的产物只有二氧化碳和水
D. 瑞德西韦的相对分子质量是602
【答案】D
【解析】
【分析】
【详解】A、氧化物是由两种元素组成的,其中一种的氧元素的化合物,瑞德西韦是由五种元素组成的,不属于氧化物,故A错误;
B、一个瑞德西韦分子由27个碳原子、35个氢原子、6个氮原子、8个氧原子和1个磷原子构成,故B错误;
C、化学反应前后,元素种类不变,瑞德西韦中含有碳、氢、氧、氮、磷元素,所以燃烧产物除了二氧化碳和水,还有氮、磷元素的化合物,故C错误;
D、瑞德西韦的相对分子质量是27×12+35×1+6×14+8×16+31=602,故D正确。
故选D。
【点睛】氧化物是由两种元素组成的,其中一种的氧元素的化合物。
8. 下列说法不正确的是
A. 液氧和臭氧都由氧元素组成,所以化学性质相同
B. 用洗洁精洗去餐具上的油污,利用了乳化原理
C. 用金属和酸制H2时,可采用与制CO2相同的发生装置
D. 糖类、蛋白质、油脂、无机盐、维生素和水都是营养素
【答案】A
【解析】
【详解】A、液氧和臭氧都由氧元素组成,但它们分子的构成不同,化学性质不同,故选项说法错误。
B、用洗洁精洗去餐具上的油污,是因为洗洁精具有乳化作用,利用了乳化原理,故选项说法正确。
C、用金属和酸制H2时,属于固液常温型,可采用与制CO2相同的发生装置,故选项说法正确。
D、糖类、蛋白质、油脂、无机盐、维生素和水都是营养素,属于六大营养素,故选项说法正确。
故选:A。
9. 如图为甲、乙两种固体物质的溶解度曲线。下列说法正确的是
A. 20℃时,100g甲的饱和溶液中含30g甲
B. 甲中混有少量乙,可以用降温结晶的方法提纯甲
C. 40℃时,分别将等质量的甲、乙配制成饱和溶液,需要水的质量:甲>乙
D. 将甲、乙两种物质的饱和溶液从20℃升温到40℃时,所得溶液的溶质质量分数:甲>乙
【答案】B
【解析】
【详解】A、20℃时,100g水中最多溶解30甲形成130g饱和溶液。即20℃时130 g甲的饱和溶液中含30 g甲。错误。
B、甲物质的溶解度随温度的升高而增大,且受温度的影响较大,乙物质的溶解度受温度影响较小。故甲中混有少量乙时可用降温结晶的方法提纯甲。正确。
C、40℃时,取50g的甲配制成饱和溶液,所需要水的质量为100g;50g的乙配置成饱和溶液,因为乙在此温度下的溶解度小于50g,因此溶解50g乙需要的水的质量超过100g,因此所需水的质量:甲<乙。错误。
D、分别将甲、乙的饱和溶液从20℃升温到40℃。由于甲、乙的溶解度随温度的升高而增大,则升温后甲乙的溶液转化为不饱和溶液,溶质与溶液质量不变。溶质质量分数不变。所得溶液的溶质质量分数:甲=乙。错误。
故选B。
10. 实验小组用传感器探究稀氢氧化钠溶液与稀盐酸反应过程中温度和pH的变化,测定结果如图所示。下列说法正确的是
A. 实验中溶液的温度一直升高、pH一直增大
B. 该实验是将稀氢氧化钠溶液滴入稀盐酸中
C. 40s时溶液中的溶质为氢氧化钠和氯化钠
D. 氢氧化钠与盐酸的中和反应先放热后吸热
【答案】B
【解析】
详解】A、由温度的变化图,实验中溶液的温度不是一直升高,故选项说法错误。
B、图象中pH值的变化是从小于7逐渐的增大到大于7,可知原溶液显酸性,然后不断的加入碱性溶液,该实验是将稀氢氧化钠溶液滴入稀盐酸中,故选项说法正确。
C、40s时放出的热量还没有达到最高,还没有完全反应,稀盐酸有剩余;或根据pH小于7,说明溶液显酸性,稀盐酸有剩余,则40s时溶液中的溶质为氯化氢和氯化钠,故选项说法错误。
D、反应过程中温度升高,说明氢氧化钠与盐酸的中和反应属于放热反应,完全反应后,随着氢氧化钠溶液的加入,温度逐渐降低,故选项说法错误。
故选:B。
11. 如图实验过程中,下列有关说法不正确的是
A. 为了减少空气污染,应增加尾气处理装置
B. 酒精灯加网罩的目的是集中火焰并提高温度
C. 加热药品前,应先通一会儿一氧化碳,以防爆炸
D. 实验现象为黑色粉末变成红棕色,澄清石灰水变浑浊
【答案】D
【解析】
A. 该实验的尾气中有未反应的一氧化碳,为了减少空气污染,应将尾气点燃或收集;B. 酒精灯加网罩的目的是集中火焰并提高温度;也可以用酒精喷灯;C. 加热或点燃可燃性气体和空气的混合物有可能发生爆炸,所以实验中应先通一会儿一氧化碳,排净装置内的空气,以防爆炸;D. 实验现象为红棕色粉末变成黑色,澄清石灰水变浑浊;选D
12. 下列各组物质在给定pH的溶液中能大量共存的是
A. pH=3:FeCl3、NaNO3、NaCl
B. pH=12:BaCl2、Na2CO3、NH4C1
C. pH=5:MgSO4、Na2CO3、Na2SO4
D. pH=10:KC1、K2SO4、HNO3
【答案】A
【解析】
【详解】A、pH=3的溶液中含有大量的氢离子,氯化铁、硝酸钠、氯化钠在pH=3的溶液中不能形成沉淀、气体和水,可以大量共存,符合题意;
B、pH=12的溶液中,含有氢氧根离子,氯化钡能与碳酸钠反应生成碳酸钡沉淀,铵根离子能与氢氧根离子结合生成氨气和水,不能大量共存,不符合题意;
C、pH=5的溶液中,含有氢离子,氢离子能与碳酸根离子结合生成二氧化碳和水,不能大量共存,不符合题意;
D、pH=10的溶液中,含有氢氧根离子,氢离子能与氢氧根离子结合生成水,不能大量共存,不符合题意,
故选A。
13. 下列四个图象的变化趋势,能正确描述对应操作的是
A. 加热一定质量的高锰酸钾固体
B. 向等质量的镁和氧化镁中分别加入足量的稀盐酸
C. 足量的铁和铝分别与等质量、等浓度的稀盐酸反应
D. 向一定量pH=13的氢氧化钠溶液中滴加大量的水
【答案】C
【解析】
【详解】A、高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,完全反应后还剩有固体锰酸钾和二氧化锰,不符合题意;
B、反应的稀盐酸质量相等时,生成氯化镁质量相等,等质量的镁和氧化镁与足量盐酸反应,镁生成的氯化镁多,不符合题意;
C、足量的铁片和铝片分别与等质量、等浓度的稀盐酸反应,产生的氢气相同,因为铝比铁活泼,先反应完,所以铝的曲线先到达最高点,符合题意。
D、向一定量pH=13的氢氧化钠溶液中滴加大量的水,随着水的增多,溶液碱性减弱,pH减小,但是不能减小到7,更不能小于7,不符合题意。
故选C。
14. 相同质量的H2、CH4和CO完全燃烧需要氧气的质量( )
A. CO最多,H2最少 B. H2最多,CH4最少
C. H2最多,CO最少 D. CH4最多,CO最少
【答案】C
【解析】
【分析】
【详解】利用化学方程式根据反应的质量可知:氢气与氧气的反应比为1:8即7:56;甲烷与氧气反应的质量比为1:4即7:28;一氧化碳与氧气反应的质量比为7:4 。所以氢气的需氧气的质量最多,一氧化碳的需氧气的质量最少,故选C。
二、填空题(本题包括6个小题,每空1分,共16分)
15. 用化学用语按下列要求填空:空气中含量最多的元素______________;能使木材、纸张变黑的酸__________;用于造纸、做洗涤剂的盐_____________________。
【答案】 (1). N (2). H2SO4 (3). Na2CO3
【解析】
【详解】空气中最多的物质是氮气,占空气体积的78%,所以空气中含量最多的元素是氮元素,对应的元素符号是N。
浓硫酸具有脱水性,能使木材、纸张变黑。物质可用化学式表示,硫酸化学式为H2SO4。
纯碱 碳酸钠可用于造纸、做洗涤剂。物质可用化学式表示,碳酸钠的化学式为Na2CO3。
16. 为了探究“水的净化”过程,某实验小组从河水中取了水样,并进行如下处理:
(1)向水样中加入明矾搅拌溶解,静置后,进行__________________(填操作名称),即可除去固体小颗粒。
(2)为了判断净化所得的水是硬水或软水,可加入__________进行检验。
(3)用水可鉴别氢氧化钠和氯化钠,加水后温度升高的是______________。
【答案】 (1). 过滤 (2). 肥皂水 (3). 氢氧化钠
【解析】
【详解】(1)过滤将不溶性固体和液体分离,向水样中加入明矾搅拌溶解,明矾形成的胶体易吸附不溶性固体小颗粒形成大颗粒,然后经过过滤除去不溶性固体小颗粒;
(2)加入等量的肥皂水搅拌,泡沫多的是软水,泡沫少、浮渣多的是硬水;
(3)氢氧化钠是易溶于水且溶于水放热的物质,氯化钠易溶于水,温度几乎无变化,如物质遇水放热,则该物质的是氢氧化钠。
故答案为:(1)过滤;(2)肥皂水;(3)氢氧化钠。
17. 在做“燃烧的条件”实验时,把同样大小的滤纸碎片和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,如图所示,观察到的现象是 先燃烧,通过此实验,说明燃烧的条件之一是 。
【答案】 乒乓球碎片 ,温度需达到可燃物的着火点
【解析】
试题分析:滤纸碎片和乒乓球碎片都与空气接触,并且温度也一样,观察到的现象是乒乓球碎片先燃 烧, 说明燃烧的条件之一是温度需达到可燃物的着火点。
考点:探究可燃物燃烧的条件。
18. 习书记于2020年5月12日在山西太钢考察的“手撕钢”厚度是0.02mm,只有A4纸的1/4,被广泛那应用于航空航天、新能源、柔韧性折叠屏等领域。“手撕钢”能制成世界上最薄的不锈钢是由于它具有良好的_______________;生活中用水银体温计测量体温,从微观角度分析体温计原理_________________;俄国化学家门捷列夫在公布元素周期表时曾预言了性质与铝相似的“类铝”元素的存在,现命名为镓(Ga)。在化合物中显+3价,请写出镓与盐酸反应的化学方程式____________________。
【答案】 (1). 延展性 (2). 汞原子间隔随温度升高而增大,随温度降低而减小(或者原子间间隔随温度发变化) (3).
【解析】
【分析】
【详解】①“手撕钢”能制成世界上最薄的不锈钢体是由于它具有良好的延展性。
②水银体温计是利用汞的热胀冷缩来测量体温,从微观的角度来看,温度升高汞原子之间间隔变大,温度降低汞原子之间的间隔变小。
③金属与酸反应生成盐和氢气,镓与盐酸反应生成氯化镓和氢气,其化学方程式为。
19. 已知A、B、C、D、E是初中化学常见的五种物质。其中A是光合作用的原料之一,B、C属于同一类物质,C为白色难溶性固体。(“一”表示相连的两种物质能发生反应,“→”表示相连物质能向箭头所指一方转化)部分反应物、生成物及反应条件已省略。
(1)物质E的化学式为_____________。
(2)D物质的用途是_____________。
(3)写出反应①B→C的化学方程式_____________。
【答案】 (1). CaO (2). 改良酸性土壤(消毒、建筑材料等合理答案) (3).
【解析】
【分析】
A、B、C、D、E是初中化学常见的五种物质。其中A是光合作用的原料之一,A能与C相互转化,C为白色难溶性固体,可推出A为二氧化碳,C为碳酸钙,B、C属于同一类物质,且B能与D反应生成碳酸钙,可推出B为碳酸钠,A能与D反应,且D能转化为C,可推出D为氢氧化钙,C能转化为E,E能转化为D,可推出E为氧化钙,代入验证,符合题意。
【详解】(1)由分析可知,E为氧化钙,化学式为:CaO;
(2)D为氢氧化钙,氢氧化钙显碱性,可用于改良酸性土壤;
(3)反应①B→C为碳酸钠与氢氧化钙反应生成碳酸钙和氢氧化钠,该反应化学方程式为:。
20. 镁与氮气反应生成氮化镁(氮显-3价),氮化镁与水反应生成难溶性碱和氨气。请写出生成碱的化学反应方程式_____________;由这种碱和MgO组成的混合物,测得其中含镁元素的质量分数为48%。取该混合物10g,将其投入适量的稀硫酸中恰好完全反应,所得溶液中溶质的质量为_____________g。
【答案】 (1). (2). 24
【解析】
【详解】(1)氮化镁与水反应生成氨气和难溶性碱,根据质量守恒定律和碱的组成可知,该碱是氢氧化镁,反应的化学方程式为Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑;
(2)因Mg(OH)2+H2SO4═MgSO4+2H2O,MgO+H2SO4═MgSO4+H2O,混合物恰好完全反应,则混合物中镁元素的质量等于MgSO4中镁元素的质量,设反应后溶液中的溶质MgSO4的质量为x,则
x=24g
所得溶液中溶质的质量为24g。
三、简答题(本题包括4个小题,10分)
21. 如图所示为葡萄糖(C6H12O6)溶液的标签,请回答:
(1)葡萄糖属于_____________(填“无机物”或“有机物”)。
(2)要把这瓶葡萄糖溶液加水稀释为2%的葡萄糖溶液,需要加水_____________g。
【答案】 (1). 有机物 (2). 750
【解析】
【详解】(1)葡萄糖含碳元素,属于有机物;
(2)解:设需加水的质量为x,根据稀释前后,溶质的质量不变,可得500g×5%=(500g+x)×2%,x=750。
22. 科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为HCHO),该反应过程的微观示意图如图所示。请回答问题:
(1)写出该反应的化学方程式_____________。
(2)计算反应生成丙和丁的质量比_____________;
【答案】 (1). (2). 22:9
【解析】
【分析】
【详解】(1)由图可知,该反应是甲醛与氧气在催化剂的作用下反应生成二氧化碳和水,该反应的化学方程式为:;
(2)反应生成的丙和丁的质量比为:44:18=22:9。
23. 某化学小组用一定量Al(NO3)3、Cu(NO3)2、AgNO3混合溶液进行了右图实验,并对溶液A和固体B的成分进行了分析和实验探究。
(1)若溶液A中加入稀盐酸没有白色沉淀产生,则写出该实验过程中一定发生反应的化学方程式_____________。
(2)若向固体B中加入稀盐酸,有气泡产生,则溶液中一定含有的金属阳离子有哪些_?(写离子符号)
(3)请分析溶液质量前后的变化_____________。
【答案】 (1). (2). Fe2+、Al3+ (3). 溶液质量减小,因为消耗铁的质量小于生成银和铜的质量,所以溶液质量减小
【解析】
【分析】
向一定量Al(NO3)3、Cu(NO3)2、AgNO3混合溶液中加入铁粉,由于金属活动性:Al>Fe>Cu>Ag,则铁先与硝酸银反应生成硝酸亚铁和银,待硝酸银完全反应后,铁与硝酸铜反应生成硝酸亚铁和铜,铁与硝酸铝不反应。
【详解】(1)若溶液A中加入稀盐酸没有白色沉淀产生,说明硝酸银已经完全反应,一定发生的反应是铁与硝酸银反应生成硝酸亚铁和银,该反应的化学方程式为:;
(2)若向固体B中加入稀盐酸,有气泡产生,说明铁粉剩余,则硝酸银、硝酸铜已经完全反应,硝酸铝与铁不反应,故溶液中一定含有的金属阳离子有亚铁离子和铝离子,故填:Fe2+、Al3+;
(3)铁与硝酸银反应:,56份铁置换出216份银,固体质量增加,溶液质量减小,铁与硝酸铜反应:,56份铁置换出64份铜,固体质量增加,溶液质量减小,故溶液质量变化为:溶液质量减小,因为消耗铁的质量小于生成银和铜的质量,所以溶液质量减小。
24. 某兴趣小组采用如下装置进行实验,实验时打开弹簧夹,并推压加液器的活塞加入稀盐酸。
(1)写出制气管中发生反应化学方程式_____________;
(2)当制气管中盐酸消耗完,反应停止后能观察到什么现象_____________?
(3)请设计实验证明烧杯中剩余溶液中含有NaOH_____________。(写出实验步骤和现象)
【答案】 (1). (2). 烧杯中的溶液被倒吸进制气管中,有白色沉淀产生 (3). 取少量溶液,加入足量的CaCl2(或 BaCl2等)溶液,静置,向上层清液中滴加酚酞溶液,溶液变红
【解析】
【分析】
【详解】(1)石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,则该反应的化学方程式为:;
(2)当制气管中盐酸消耗完,氢氧化钠与二氧化碳反应生成碳酸钠和水,二氧化碳被消耗,装置内压强减小,在外界大气压的作用下,烧杯中的溶液被倒吸入制气管中,反应生成的氯化钙与碳酸钠反应生成碳酸钙和氯化钠,产生白色沉淀,故反应停止后能观察到烧杯中的溶液被倒吸进制气管中,有白色沉淀产生;
(3)氢氧化钠显碱性,能使无色酚酞试液变红,可用无色酚酞试液来检验氢氧化钠,但是氢氧化钠与二氧化碳反应生成了碳酸钠,碳酸钠也呈碱性,也能使无色酚酞试液变红,故可加入过量的氯化钙,过量的氯化钙与碳酸钠反应生成碳酸钙和氯化钠,将碳酸钠除尽,然后向上层清液中加入无色酚酞试液,无色酚酞试液变红,说明含氢氧化钠,故填:取少量溶液,加入足量的CaCl2(或 BaCl2等)溶液,静置,向上层清液中滴加酚酞溶液,溶液变红。
四、综合应用题(共10分)
25. “84”消毒液在新冠肺炎预防措施中使用较为广泛,其还具有漂白、杀菌、消毒的功效。某化学兴趣小组对一瓶敞口久置的“84”消毒液的成分产生兴趣,在老师的指导下展开探究。已知:“84”消毒液和洁厕灵作用会产生氯气。
【提出问题】该敞口久置的消毒液中溶质有哪些?
【查阅资料】“84”消毒液的主要成分是次氯酸钠( NaClO)和氯化钠; NaClO为有效成分,有腐蚀性并易与空气中的CO2反应()。HClO不稳定,受热或光照条件下会发生分解。NaC1O溶液、HC1O都具有漂白、杀菌、消毒功效。
【分析讨论】小组同学经过讨论,认为该消毒液中的溶质一定有_____________,可能还有
NaC1O、Na2CO3、HC1O中的一种或多种。
【实验探究】
实验操作
实验现象
实验结论
Ⅰ.向装入红色布条的试管中加入适量该消毒液
布条长时间不褪色
消毒液中不含①_______
Ⅱ.另取少量该消毒液于试管中,滴入氯化钡溶液
白色沉淀
消毒液中含②_____,发生反
应化学方程式为③__。
【交流反思】生活中,“84”消毒液贮藏时应注意_______存放。
【拓展延伸】
(1)“84”消毒液__________(“能”或“不能”)与洁厕灵混合使用。
(2)次氯酸钠与稀硫酸可发生复分解反应,化学方程式为___________。
(3)已知:氯气与水反应的化学方程式为。“84”消毒液一般通过氯气与氢氧化钠反应制得,现有200g10%的氢氧化钠溶液与氯气反应制备消毒液。计算需要消耗氯气的体积是多少_______?(氯气的密度是3.21g/cm3,结果保留一位小数)
【答案】 (1). NaCl (2). NaClO、HClO (3). Na2CO3 (4). (5). 密封避光 (6). 不能 (7). (8). 5.5cm3
解:设需要氯气的体积是V。
V=5.5cm3
答:需要消耗氯气的体积是 5.5cm3
【解析】
【详解】【分析讨论】因为“84”消毒液的主要成分是次氯酸钠( NaClO)和氯化钠; NaClO为有效成分,氯化钠不参加反应,不会变质。所以一定会存在氯化钠。
【实验探究】因NaC1O溶液、HC1O都具有漂白性,而布条长时间不褪色。所以消毒液中不含NaClO、HClO。
滴入氯化钡溶液会产生白色沉淀,可能物质中只有碳酸钠与氯化钡反应生成白色沉淀,化学方程式为:。
【实验探究】 因NaClO能与空气中CO2反应生成HClO,HClO不稳定,受热或光照条件下会发生分解,所以应该密封避光保存。
【拓展延伸】(1)“84”消毒液不能与洁厕灵混合使用。因为洁厕灵中的氯化氢与次氯酸会发生反应生成氯气,降低效果,并会放出有毒气体。
(2)因为发生的是复分解反应,两种化合物的阴阳离子互换,化学方程式为:
(7)详见答案。
精品解析:2020年河南省新乡市新乡县中考化学二模试题(解析版+原卷版): 这是一份精品解析:2020年河南省新乡市新乡县中考化学二模试题(解析版+原卷版),文件包含精品解析2020年河南省新乡市新乡县中考化学二模试题解析版doc、精品解析2020年河南省新乡市新乡县中考化学二模试题原卷版doc等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
2021年河南省新乡市辉县市中考二模化学试题及答案: 这是一份2021年河南省新乡市辉县市中考二模化学试题及答案,共8页。
精品解析:2020年河南省南阳市邓州市中考二模化学试题(解析版+原卷版): 这是一份精品解析:2020年河南省南阳市邓州市中考二模化学试题(解析版+原卷版),文件包含精品解析2020年河南省南阳市邓州市中考二模化学试题解析版doc、精品解析2020年河南省南阳市邓州市中考二模化学试题原卷版doc等2份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。












