











初中化学人教版九年级下册课题2 溶解度课文内容课件ppt
展开
这是一份初中化学人教版九年级下册课题2 溶解度课文内容课件ppt,文件包含922溶解度同步课件pptx、922溶解度导学案docx、922溶解度同步练习doc、922溶解度教学设计doc、增加鱼池中的含氧量wmv等5份课件配套教学资源,其中PPT共29页, 欢迎下载使用。
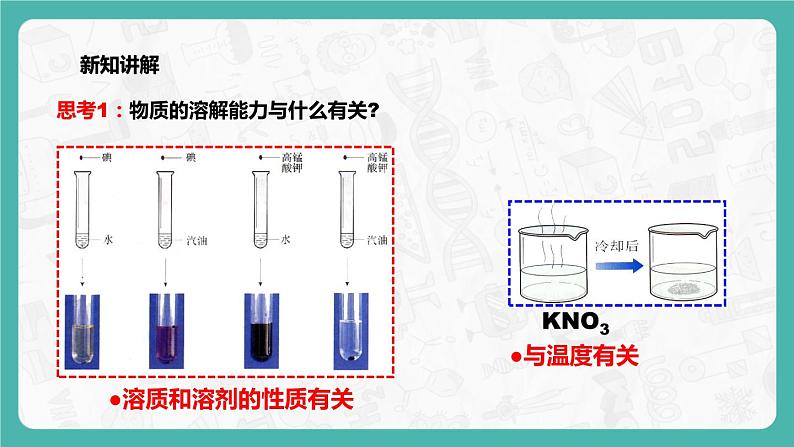
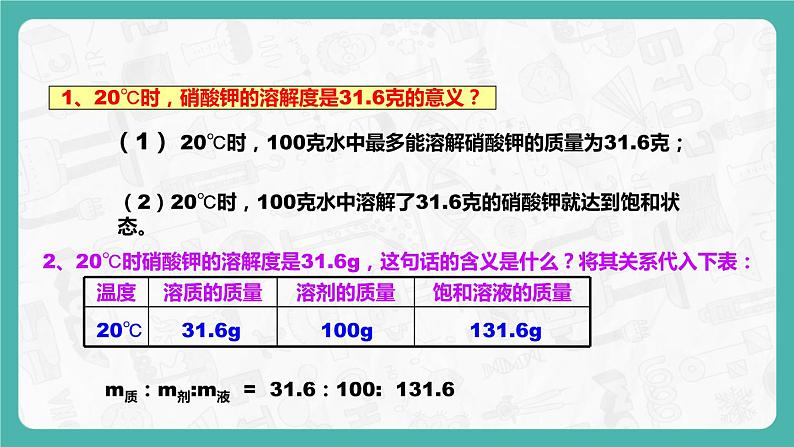
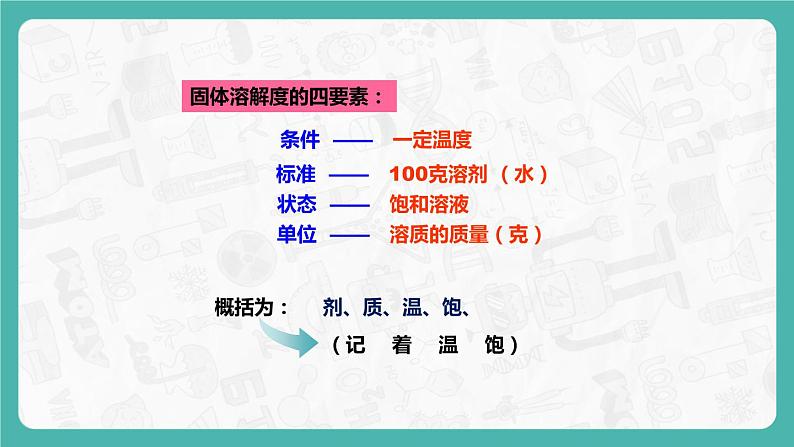
导学案 导学目标:1. 了解固体物质溶解度的涵义。2. 学会熟练利用溶解性表或溶解度曲线,查阅相关物质的溶解性或溶解度,并进行相关知识的推知和判断。3. 知道影响气体溶解度的一些因素。会利用有关气体溶解度的知识解释身边的一些现象。自主预习:1. 固体溶解度是指在一定温度下,某固体在 溶剂里达到 状态时所溶解的 ,单位是 。2. 影响固体物质在水中溶解度大小的外在因素是: ,大部分物质如硝酸钾的溶解度随 ,少数物质如食盐的溶解度随 ,只有极少数物质如_________溶解度随 。3.溶解度的相对大小:在20℃时,难溶是指溶解度_______;微溶是指溶解度______;可溶是指溶解度______;易溶是指溶解度_______。4.气体的溶解度随温度的升高而_____,随压强的增大而______。【尝试挑战】5.根据图1信息判断,下列叙述不正确的是( ) 图1A.硝酸钾的溶解度随温度升高而增大B.t1 ℃时,氯化钠和硝酸钾的溶解度相同C.将t2℃时的硝酸钾饱和溶液降温到t1℃,有晶体析出 D.t2℃时,80g 硝酸钾溶于100g水中可制得饱和溶液课堂导学【导学探究】探究一 固体物质的溶解度探究指导: 1. 概念:一定温度下,某固体物质在100克溶剂里达到饱状态时所溶解的溶质的质量,叫做这种溶质在这种溶剂里的溶解度。若不指明溶剂,通常所说的溶解度是指物质在水中的溶解度。2. 定义中的四要素:一定温度、100克溶剂、达饱和状态、溶质质量(单位:克)①条件:在一定温度下。因为影响固体物质溶解度的内因是溶质和溶剂的性质,而外因就是温度,如果温度改变则固体物质的溶解度也会改变。因此只有指明温度时,溶解度才有意义;②标准:在100g溶剂中。此处100g是指溶剂质量,不能误认为是溶液质量;③状态:达到饱和时。④单位:以克为单位。3. 溶解度的意义:指某温度下,100g水中最多可溶解某种溶质的质量。例如:“20℃时,氯化钠的溶解度为36克”指:20℃时,氯化钠在100水里溶解达到饱和状态,可以溶解36克。也可指:20℃时,100水中最多可以溶解36克氯化钠。4. 固体物质溶解度与溶解性的关系:温度为20℃:溶解度/克<0.010.01~11~10>10溶解性分类难溶微溶可溶易溶例题1: 下列说法正确的是( )A. 100克水中最多能溶解某物质40克,则该物质的溶解度为40克B. 4℃时,溶质N的饱和溶液120克中含N物质20克,所以4℃时,溶质N的溶解度为20克。C. 一定温度下,物质M的饱和溶液100克中含M物质30克,则物质M在该温度时溶解度为30克D. 20℃时,50克水中溶有溶质P20克,则物质P在20℃时的溶解度为40克。思路分析: 理解溶解度的概念及意义,一定要注意其四要素,即:一定温度、100g溶剂、饱和状态及单位(g),只有全部包含了这四个要素才是正确的。A中脱离了温度,谈溶解度无意义;B中120克4℃时N的饱和溶液含N物质20克,即此温时100克水中最多溶N物质20克。满足了溶解度的四个要素;C中100克指的是溶液,而不是溶剂;D中未体现达饱状态这一要素,未必是所溶解的最大量。答案:D方法指导: (1)影响溶解度的因素:溶质的性质;溶剂的性质;温度。在溶质和溶剂一定的情况下,温度是影响固体溶解度的重要因素;(2)固体物质的溶解度与溶质的质量和溶剂质量的多少无关。【跟踪训练】:1.下列做法能改变固体物质溶解度的是( )A.升高温度 B.增加溶质 C.增加溶剂D.增大压强2.将物质甲5g充分溶解在100g水中,恰好得到饱和溶液,则该物质的溶解性属于( )A.易溶 B.可溶 C.难溶 D.不能确定 3.已知20℃时,硝酸钾的溶解度为30g。现有20℃时硝酸钾饱和溶液200g,则其中溶质、溶剂与溶液的质量比为( )A.3∶7∶10 B.7∶3∶10 C.3∶10∶13 D.10∶3∶13探究二 固体物质溶解度的表示方法探究指导: 1. 表示方法:①列表法:如硝酸钾在不同温度时的溶解度:温度/℃020406080100溶解度/g13.331.663.9110169246②曲线法:用纵坐标表示溶解度,横坐标表示温度,得到物质溶解度随温度变化的曲线,这种曲线叫溶解度曲线。如图2所示: 图22.溶解度曲线的变化规律: 绝大多数固体物质的溶解度随温度的升高而增大,如KNO3;少数固体的溶解度随温度的变化而变化不大,如NaCl;极少数固体物质的溶解度随温度的升高而减小,如Ca(OH)2。3.溶解度曲线的意义:①溶液度曲线上的点表示某温度下某物质的溶解度;②溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度变化的情况;③溶解度曲线上的交叉点表示交点所对应温度时,不同物质有相同的溶解度。这些物质的饱和溶液的溶质质量分数也相同;④溶解度曲线下方的点表示某温度下某物质的不饱和溶液。4.溶解度曲线的应用:①判断某物质溶解度随温度的变化情况;②判断不同物质在某一温度下的溶解度大小;③判断某物质饱和溶液与不饱和溶液的转换方式;④判断提纯某种物质所用的方法。例题2:如图3是X、Y两种固体物质的溶解度曲线,下列说法中错误的是( )A.X、Y两种物质的溶解度都随温度升高而增大B.X物质的溶解度大于Y物质的溶解度C.降低温度可使接近饱和的X溶液变为饱和溶液D.t℃时,X物质的溶解度等于Y物质的溶解度思路分析: 由X和Y的溶解度曲线知:X、Y两种物质的溶解度都随温度的升高而增大,故A正确;X、Y两种物质的溶解度在小于t℃时Y的溶解度大于X的溶解度,在t℃时它们的溶解度相等,当大于t℃时,X物质的溶解度大于Y物质的溶解度,故B错误,D正确;X物质的溶解度受温度变化影响大,可采用降温结晶法使其饱和,故C正确。答案:B规律总结:溶解度曲线是中考试题中必定会涉及考查的重点内容.我们复习溶解度曲线时,关键是必须能读懂溶解度曲线所提供的以下信息:(1)某物质的溶解度随温度的变化而变化的趋势;(2)在某一温度下,不同物质的溶解度大小关系;(3)交点的意义;(4)物质的溶解性:易溶、可溶、微溶、难溶(20℃);(5)溶解度曲线上、曲线之下、曲线之上的“点”的意义;(6)相同温度下不同溶质的相同质量的饱和溶液降温至同一温度时,析出晶体多少的判断:高温与低温时的溶解度的差距越大,析出的晶体就越多。【跟踪训练】4.图4是甲、乙两种固体的溶解度曲线,下列说法正确的是 ( )A.甲的溶解度等于乙的溶解度 B.升高温度可以将甲的不饱和溶液变为饱和溶液C.20 ℃时,100 g乙的饱和溶液中溶质质量是30 gD.40 ℃时,分别用100g水配制甲、乙的饱和溶液,所需 甲的质量大于乙的质量5.图5为A、B、C三种物质的溶解度曲线,回答下列问题:图5(1)t1℃时,溶解度最小的物质是____(填序号)。(2)t2℃时为20℃,则A物质是________物质(填“易溶”“可溶”“微溶”或“难溶”)(3)分别通过加溶质、蒸发溶剂、升温三种手段均可使不饱和溶液变为饱和溶液的是___________。(4)将t1℃三种物质的饱和溶液各ag升温到t2℃,有晶体析出的是_______________。6.图6是三种固体物质的溶解度曲线。(1)物质c的溶解度随温度的升高而________;(2)物质a的溶解度大于物质c的溶解度的温度范围______________;(3)t2℃时,用50g水配制物质a的饱和溶液,至少需要___g物质。探究三 气体的溶解度探究指导: 1.概念:气体的溶解度是指在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。2.影响因素:温度和压强。温度越高,气体溶解度越小;压强越大,气体溶解度越大。3.单位:气体溶解度单位是体积。例题3: 广东佛山市三水健力宝生产的“魔水”驰名中外.“魔水”内溶有一定量的二氧化碳气体.打开瓶盖,“魔水”会自动喷出,喝了“魔水”后常会打嗝.说明气体在水中的溶解度与压强、温度有关.以下关于气体溶解度的说法正确的是( )A.压强增大,气体溶解度不变 B.压强减小,气体溶解度增大C.温度升高,气体溶解度减小 D.温度降低,气体溶解度减小思路分析: “魔水”喝入胃中,温度升高,气体溶解度减小,所以会打嗝;“魔水”开盖后,压强减小,气体溶解度减小,所以会逸出气泡答案:C【跟踪训练】:7.气体的溶解度也有一定的变化规律。(1)打开可乐瓶,逸出大量气泡。由此可见,压强越小,CO2的溶解度越_________。为增大CO2的溶解度,可采用的一种方法是________。(2)不同温度下,氧气的溶解度随压强的变化如图7所示,图中t1对应的温度为40℃,则t2对应的温度________(填编号)。a.大于40℃ b.小于40℃ c.无法确定当堂达标8.已知下列物质在20℃时的溶解度,其中属于可溶物质的是( )A.CaCO3为0.0013g B.食盐为36g C.熟石灰为0.17g D.KClO3为7.4g9.如图8是甲、乙两种固体物质的溶解度曲线。据此判断下列说法不正确的是( )A.t2℃时,甲、乙的溶解度相等B.t3℃时,将60g乙加入100g水中可得l60g溶液C.乙的溶解度受温度影响很小D.tl℃时,乙的溶解度大于甲的溶解度10.下列有关溶液的说法,不正确的是( )A.蔗糖溶液是均一的、稳定的混合物B.硝酸钾在20℃时溶解度是31.6g,则lOOg 硝酸钾溶液中含有硝酸钾31.6gC.在鱼池中设立水泵,把水喷向空中可以增加水中氧气的溶解量D. 冷却或蒸发溶剂都能使接近饱和的氯化钠溶液达到饱和11.氢氧化钙的溶解度随温度升高而减小。要想把一瓶接近饱和的石灰水变成饱和,具体措施有:①加入氢氧化钙;②升高温度;③降低温度;④加入水;⑤蒸发水。其中措施正确的是( )A.①②④ B.①③④ C.①③⑤ D.①②⑤12.图9是A、B两种固体物质的溶解度曲线:(1)p点表示的意义__________________;(2)t1℃时,两种物质的溶解度由大到小的顺序为____________;(3)t3℃时,将45g的A物质加入到盛有50g水中的烧杯中,充分搅拌,得到A溶液的质量为______g。13.图10是A、B两种固体物质的溶解度随温度变化的曲线。请回答:(1) ℃时,A、B两物质的溶解度相等。(2)20℃时,A物质的溶解度 B物质的溶解度(填“>”、“<”或“=”)。(3)40℃时,将A、B各15 g分别加到均盛有50g水的两只小烧杯中,充分搅拌后, 物质有剩余(填“A”或“B”)。(4)现有50℃时A物质的不饱和溶液在不减少溶剂的情况下,欲使其变成饱和溶液,下列措施肯定不能实现的是 (填序号)。①降低温度 ②升高温度 ③加入A物质14.下表是NaCl、NH4Cl在不同温度时的溶解度。温度/℃020406080溶解度/ gNaCl35.736.036.637.3[38.4NH4Cl29.437.245.855.265.6(1)以上两种物质溶解度的变化受温度影响较小的是____________。(2)20℃时,将40gNaCl加入到100g水中充分搅拌后,所得溶液的质量为______g。 (3)40℃时,要使接近饱和的NH4Cl溶液变为饱和溶液,下列方法中一定能达到目的的是___(填序号)。① 升高温度 ②加溶质NH4Cl ③加水 ④恒温蒸发水课后提高1.一定温度下,向图11所示烧杯中加入一定量水,仅有部分晶体溶解。所得溶液与原溶液相比,说法正确的是( ) 图11A.溶剂的质量增加,溶液颜色变浅 B.溶质溶解度不变,溶液颜色变深 C.溶质的质量增加,溶液颜色变深 D.溶质溶解度不变,溶液颜色不变2.图12表示M、N两种固体物质的溶解度曲线,下列对图示信息的描述正确的是( )A.30℃时M的溶解度小于N的溶解度B.P点表示t℃时M、N的溶解度相等C.M、N都是难溶物质 D.阴影处各点对应的溶液(不包含曲线上的点)是M的不饱和溶液,N的饱和溶液3.图13为A物质的溶解度曲线。M、N两点分别表示A物质的两种溶液。下列做法不能实现M、N间的相互转化的是( )(A从溶液中析出时不带结晶水)A.从N→M:先向N中加入适量固体A再降温B.从N→M:先将N降温再加入适量固体AC.从M→N:先将M降温再将其升温D.从M→N:先将M升温再将其蒸发掉部分水4.在初中化学中,我们学习了溶液的有关知识。图14是KNO3的溶解度曲线。(1)从图中溶解度曲线可以得到的信息是(写一条)___________________________。(2)小明参照图15在常温20℃时进行了如下实验:图15小明观察到A中所加固体全部溶解,则B中_______。上述实验过程中属于不饱和溶液的是(填字母)____。5. A、B、C三种物质的溶解度曲线如图16所示。(1)在t1℃时,A、B、C三种物质的溶解度由大到小的顺序是_________。其中,可能是气态物质的是_______。(2)P点表示t2℃时,完全溶解a g A物质最少需______g水。(3)若B是KCl,则B溶液中的溶质粒子是(填符号)___________。 答案与点拨自主预习1.100g 饱和 质量 克2.温度 温度的升高而增大 温度的变化而变化不大 熟石灰 温度的升高而减小3.<0.01g 0.01-1g 1-10g >10g4.减小 增大5. D 点拨:从曲线上可知硝酸钾随温度升高,溶解度增大;t1 ℃时两曲线的交点,表示其溶解度相同;硝酸钾t2℃比t1 ℃溶解度大,降温硝酸钾饱和溶液有晶体析出;t2℃时硝酸钾溶解度为85g,即100g水中溶解85g硝酸钾刚好饱和。课堂导学1. A 点拨:只要温度一定,固体物质的溶解度就是固定的。固体物质的溶解度不受压强影响,增加溶剂量只能影响溶质被溶解的质量,与溶解度无关。固体物质的溶解度只受温度影响。2. D 点拨:根据数据进行计算,可知物质甲此时的溶解度为5g,但是这不能得出该物质属于可溶的结论。因为只有在20℃时,才能根据数据进行溶解性的分类,本题缺乏温度,因此不能作出判断。3. C 点拨:无论饱和溶液的具体质量是多少,由于在确定温度下,物质的溶解度是确定的,因此,其中溶质、溶剂与溶液的质量比也是确定的,三者之比为:S∶100g∶(100g+S)。所以,20℃时200g硝酸钾饱和溶液中溶质、溶剂与溶液的质量比为3∶10∶13。4.D 点拨:由溶解度曲线图可看出,当温度高于20℃时,甲物质的溶解度大于乙物质的溶解度,当温度低于20℃时,甲物质的溶解度小于乙物质的溶解度,故A错误;由溶解度曲线不难看出,甲物质的溶解度随温度的升高而逐渐增大,所以要将其不饱和溶液变为饱和溶液应该降低温度,故B错误; 20℃时乙物质的溶解度为30g,即30g乙溶于100g水中所得溶液为饱和溶液,所得饱和溶液的质量是130g,故C错误;观溶解度曲线可知:40℃时,甲物质的溶解度大于乙物质的溶解度;所以用100g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量,故D正确;故选D。5. (1)A (2)易溶 (3)C (4)C点拨:本题考查溶解度曲线的意义及应用。由图可知:通过t1℃垂直于横坐标的垂线与曲线A的交点最低,故t1℃时,A的溶解度最小。物质的溶解性是根据20℃时物质在水里的溶解度区分的,20℃时,A的溶解度为25g>10g,因此A属于易溶物质。C的溶解度随温度的升高而减小,通过升温可将其由不饱和溶液变为饱和溶液,加溶质、蒸发溶剂也可达到此目的。同理,C的饱和溶液升温后,由于溶解度减小,所以必将有晶体析出。A、B升温后,溶解度增大,原来的饱和溶液会变成不饱和溶液而没有晶体析出。6.(1)减小 (2)大于t1℃ (3)25 点拨:(1)由物质c的溶解度曲线可知,物质c的溶解度随温度的升高而减小;(2)由物质a、c的溶解度曲线进行对比可知,物质a的溶解度大于物质c的溶解度的温度范围是:大于t1℃;(3)由物质a的溶解度曲线可知,t2℃时物质a的溶解度是50g,t2℃时,用50g水配制物质a的饱和度溶液,至少需要 25g物质a。7.(1)小 (2)b当堂达标8.D9.B 点拨:溶解度曲线能定量地表示出溶解度变化的规律,因而从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同。由图像可知,在t2℃时,甲、乙两物质的溶解度曲线有一个交叉点,所以甲、乙的溶解度相等,则t2℃时,甲、乙两种饱和溶液中溶质的质量分数相等,但溶质的质量未必相等,只有溶剂质量相等时,溶质质量才相等。达到饱和时,由曲线图像提供的信息可知:甲的溶解度受温度的影响较大,乙的溶解度受温度影响不大,在相同质量的溶液中,两溶质的质量相等,故溶剂水的质量也相等。但在t2℃时,乙的溶解度小于60g,所以t3℃时,将60g乙加入100g水中不可能可得到l60g溶液。10.B11.D 点拨:向接近饱和的溶液中增加溶质或蒸发溶剂都可以使溶液变成饱和溶液,故把一瓶接近饱和的石灰水变成饱和,可以采取:①加入氢氧化钙、⑤蒸发水的方法;由于氢氧化钙的溶解度随温度升高而减小,升高温度后氢氧化钙的溶解度变小,故把一瓶接近饱和的石灰水变成饱和,还可以采取②升高温度的方法,故①②⑤符合题意,故选D。12.(1)t2℃时,A、B两种固体物质的溶解度相同 (2)B﹥A (3)90 13.(1)30℃ (2)< (3)B (4)②14.(1)NaCl (2)136 (3)②④课后提高1.D 点拨:加入水溶剂增多,但一开始溶液饱和,加入一定量的水,仅有部分晶体溶解,说明溶液仍然饱和,饱和溶液的质量分数与溶解度有关,因为温度不变所以溶解度不变,溶质质量分数也不变,所以溶液颜色不变,故A错;溶解度受温度影响,温度不变溶解度就不变,加入水溶剂增多,但一开始溶液饱和,加入一定量的水,仅有部分晶体溶解,说明溶液仍然饱和,饱和溶液的质量分数与溶解度有关,因为温度不变所以溶解度不变,溶质质量分数也不变,所以溶液颜色不变,故B错;加入一定量的水变成不饱和又溶解了一部分溶质,所以溶质质量增加,但溶液颜色是不变的,故C错;溶解度受温度影响,温度不变溶解度就不变,加入水溶剂增多,但一开始溶液饱和,加入一定量的水,仅有部分晶体溶解,说明溶液仍然饱和,饱和溶液的质量分数与溶解度有关,因为温度不变所以溶解度不变,溶质质量分数也不变,所以溶液颜色不变,故D正确。故选D。2. B 点拨:根据溶解度曲线知30℃时,M的溶解度大于N,故A错误;P点表示M和N在t℃时溶解度相等,故B正确;在20℃时M、N的溶解度都大于10g,故都是易溶物质,故C错误;阴影处各点对应的溶液是M的饱和溶液,是N的不饱和溶液,故D错误。3. D 点拨:根据图像可以看出,升温后该物质溶解度变大,M点向右平移,再蒸发水,会逐渐接近饱和或达到饱和,故不可能到N点,故D不正确。4. (1)20℃时,KNO3的溶解度是31.6g (2)固体部分溶解 A、C、D5.(1)C、B、A C (2)100 (3)K+ Cl-
相关课件
这是一份初中化学人教版九年级下册课题2 溶解度试讲课ppt课件,文件包含92-2溶解度第2课时教学课件pptx、92-2教学设计溶解度第2课时docx、92-2练习·基础巩固溶解度第2课时docx、92-2练习·能力提升溶解度第2课时docx、92-2练习·素能拓展溶解度第2课时docx、92-2预习导学溶解度第2课时docx等6份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
这是一份初中化学人教版九年级下册课题2 溶解度教课内容ppt课件,共29页。PPT课件主要包含了条件一定温度,溶解度的表示方法,答案C,课堂小结,溶解度,影响因素,固体溶解度,TT↗S↘,PP↗S↗,溶解度曲线等内容,欢迎下载使用。
这是一份初中化学人教版九年级下册第九单元 溶液课题2 溶解度集体备课课件ppt,共20页。









