




人教版九年级下册课题2 酸和碱的中和反应示范课ppt课件
展开1.认识中和反应的概念及实质;2.了解酸和碱对生命活动和农作物的影响,以及中和反应在实际中的应用。
浓硫酸泄漏,为什么可以用熟石灰抢险?
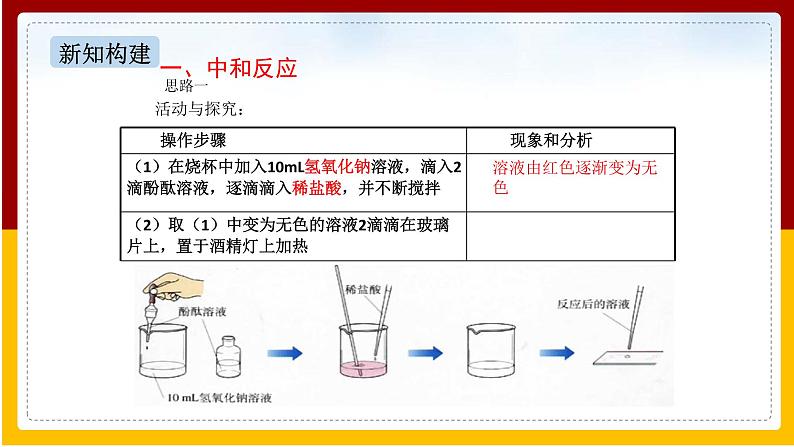
溶液由红色逐渐变为无色
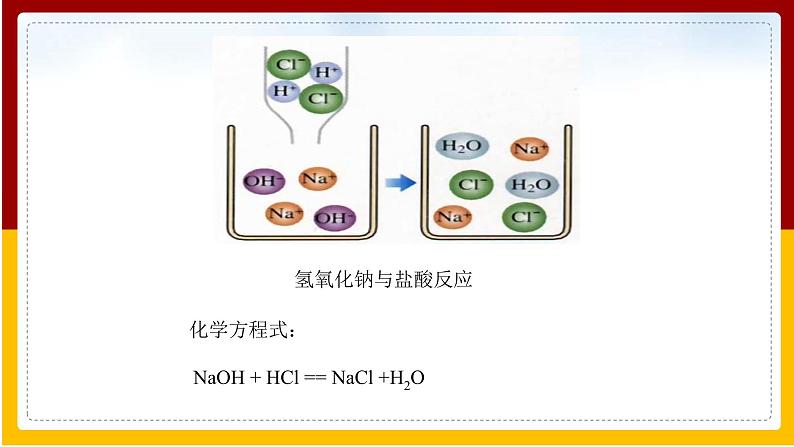
氢氧化钠与盐酸反应
NaOH + HCl == NaCl +H2O
例 其他的酸和碱也能发生类似的反应。
Ca(OH)2 + 2HCl == CaCl2 +2 H2O
2NaOH +H2SO4 == Na2SO4 +2H2O
上述三个反应的特点: 三个反应都生成水,另一种产物(氯化钠、氯化钙、硫酸钠)都是由金属离子和相应的酸根离子构成的,我们把这类化合物叫做盐,我们把这类化学反应叫做中和反应。
盐:由金属离子和酸根离子 构成的化合物
中和反应:酸和碱作用生成盐和水的反应。
酸 + 碱 → 盐 + 水
【演示实验】 在一支试管中先后倒入少量NaOH和稀HCl溶液,振荡。
【设疑】 我们可以用什么方法证明这个反应是否发生了?
方案1:取一支试管,往试管里倒入5 mL NaOH溶液,滴入几滴酚酞溶液,再用滴管慢慢滴入稀盐酸,不断振荡溶液,至溶液颜色由红色变为无色。
【现象】方案1:溶液由无色变为红色,最后又由红色变为无色。
现象:溶液由无色变为蓝色,最后又由蓝色变为紫色。
方案2:取一支试管,往试管里倒入5 mL NaOH溶液,滴入几滴石蕊溶液,再用滴管慢慢滴入稀盐酸,不断振荡溶液,至溶液颜色由蓝色变为紫色。
方案3:取一支试管,往试管里倒入5 mL稀盐酸,滴入几滴石蕊溶液,再用滴管慢慢滴入NaOH溶液,不断振荡溶液,至溶液颜色由红色变为紫色。
现象:溶液由无色变为红色,最后又由红色变为紫色。
【学生练习】 书写化学方程式:(1)Cu(OH)2+H2SO4
(2)Fe(OH)3+HCl
【实验探究1】 探究酸与碱之间能否发生化学反应。【实验步骤】 (1)取一支试管,先加入适量氢氧化钠溶液。(2)再用胶头滴管慢慢向试管中滴加盐酸。
【展示】 实验1:将紫色石蕊溶液滴入盐酸中,再慢慢滴入氢氧化钠溶液;实验2:将紫色石蕊溶液滴入氢氧化钠溶液中,再慢慢滴入盐酸;实验3:将无色酚酞溶液滴入盐酸中,再慢慢滴入氢氧化钠溶液;实验4:将无色酚酞溶液滴入氢氧化钠溶液中,再慢慢滴入盐酸。
【总结】 用无色酚酞溶液作指示剂,现象便于观察。
【实验探究2】 在烧杯中先加入10 mL氢氧化钠溶液,滴入几滴无色酚酞溶液,再用胶头滴管慢慢滴入稀盐酸,边滴边用玻璃棒不断搅拌溶液,至溶液颜色恰好变为无色为止,停止加入盐酸。
【讨论】 在实验过程中,溶液为什么先变红?当滴加适量盐酸后,溶液由红色变成无色时,说明了什么?为何要逐滴滴加稀盐酸?
氢氧化钠溶液是碱性溶液,它能使酚酞试液变红;加入盐酸后,溶液变为无色,说明原溶液中的氢氧化钠不存在了,变成了其他物质;说明氢氧化钠溶液可以与稀盐酸反应;逐滴滴加稀盐酸,能更清楚地观察酚酞溶液的颜色变化,并能控制氢氧化钠溶液可以与稀盐酸恰好完全反应。
HCl→H+ + Cl—
NaOH→Na+ + OH—
HCl和NaOH在水中解离出离子
NaOH+HCl== NaCl+H2O
【讨论】 蒸发后玻璃片上的白色物质是氢氧化钠吗?为什么?【分析】 氢氧化钠是碱,其溶液能使酚酞溶液显示红色,随着盐酸的加入,红色逐渐消失变成无色,所以此时的溶液肯定不是碱性溶液。根据质量守恒定律也可以说明玻璃片上的白色物质不是氢氧化钠,而是反应生成的新物质——氯化钠。
【实验探究3】 取2滴上述反应后的无色溶液滴在玻璃片上,加热,使水分蒸发,观察有什么现象。【学生】 现象:玻璃片上出现白色物质。
知识点2、中和反应在实际中的应用
在酸性土壤中加入熟石灰,中和土壤的酸性
硫酸厂的污水中含有硫酸等物质,可以用熟石灰进行中和处理
若工厂的废水呈碱性,可加入废硫酸进行中和
被蚊虫叮咬后可涂稀氨水止痒,碱性物质能与蚊虫分泌的蚁酸中和
3HCl + Al(OH)3 AlCl3 + 3H2O
胃酸过多的病人可服用含有碱性物质(如氢氧化铝)的药物
生活中的中和反应1.食用松花蛋时加入食醋可以将其中的碱性物质中和,从而消除其涩味,使松花蛋变得可口。2.洗发时先使用弱碱性的洗发剂,再用弱酸性的护发素,可以保护头发。
(2019·新乡模拟)下列应用与中和反应原理无关的是( )
A.配制农药波尔多液B.用氢氧化钠溶液洗涤石油产品中残留的硫酸C.用熟石灰改良酸性土壤 D.服用含氢氧化镁的药物治疗胃酸过多症
中和反应:酸+碱 盐+水
1.如图是氢氧化钠与盐酸反应示意图。
(1)反应前后没有发生变化的离子有哪些?(2)用实际参加反应的离子符号来表示反应的式子叫做离子方程式。请写出氢氧化钠与盐酸反应的离子方程式。
答案:(1)由反应示意图得,反应前后没有发生变化的离子是钠离子和氯离子。(2)氢氧化钠与盐酸反应生成氯化钠和水,实际参加反应的离子是氢离子和氢氧根离子,生成水分子,反应的离子方程式为:H++OH- H2O。
2.中和反应在生活生产中有广泛的应用,下列做法不是利用中和反应原理的是( )
A.用熟石灰改良酸性土壤B.用含氢氧化镁的药物治疗胃酸过多C.用盐酸除去铁锈D.用氨水(NH3·H2O)处理工厂的硫酸
解析:用盐酸除去铁锈,发生的反应为Fe2O3+6HCl 2FeCl3+3H2O,不属于中和反应。
3.下列方法可以解决生活中的一些问题。(1)服用含氢氧化铝的药物可以治疗胃酸过多症,反应的化学方程式为_________________________________。(2)用熟石灰可以处理硫酸厂污水中含有的硫酸,反应的化学方程式为__________________________________。
Al(OH)3+3HCl AlCl3+3H2O
Ca(OH)2+H2SO4 CaSO4+2H2O
4. 某化学兴趣小组用实验室常用药品(或溶液)对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。[知识卡片] 氯化钠溶液显中性。[实验探究] (1)方案Ⅰ:某同学先向试管中加入约2 mL NaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①实验结论: 。②从微观的角度分析,该反应的实质是 。
NaOH溶液与稀盐酸恰好完全反应
氢离子和氢氧根离子结合生成水分子
初中化学人教版九年级下册课题2 酸和碱的中和反应多媒体教学课件ppt: 这是一份初中化学人教版九年级下册课题2 酸和碱的中和反应多媒体教学课件ppt,共28页。PPT课件主要包含了活动与探究,中和反应,思路一,播放中和反应实验,化学方程式,归纳并板书,思路二,思路三,氢氧化钠与盐酸反应,改良酸性土壤等内容,欢迎下载使用。
2022年人教版化学中考专题训练 第10单元 酸和碱 第2课时 酸和碱的中和反应课件PPT: 这是一份2022年人教版化学中考专题训练 第10单元 酸和碱 第2课时 酸和碱的中和反应课件PPT,共24页。PPT课件主要包含了生石灰,不一定,OH-,t2到t3,CaCl2和HCl,足量的,碳酸钠溶液,先有气泡产生后,有白色沉淀生成,石蕊试液合理即可等内容,欢迎下载使用。
九年级下册课题2 酸和碱的中和反应示范课ppt课件: 这是一份九年级下册课题2 酸和碱的中和反应示范课ppt课件,共27页。PPT课件主要包含了新知导入,新知探究,溶液的酸碱度,酸碱度,酸碱性,pH的测定方法,pH计,pH试纸,读数为整数,特别提醒等内容,欢迎下载使用。













