
仁爱湘教版九年级下册专题八 金属和金属材料综合与测试课后复习题
展开专题8《金属和金属材料》检测题
一、单选题
1.运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是
A.金刚石、石墨、C60都是由碳元素组成的,也都是由碳原子构成的物质
B.钢铁、硬铝和黄铜都是合金,则合金中至少含有一种金属单质
C.二氧化碳气体能使紫色石蕊试剂变红色,则一氧化碳气体也能使紫色石蕊试剂变红色
D.铝的金属活动性比铁强,则铝制品比铁制品更容易生锈
2.铜锌合金若干克经粉碎后与足量的稀硫酸充分反应,过滤后,得到的滤渣在空气中充分灼烧,结果灼烧后的生成物质量与原合金质量相等,则原合金中锌的质量分数为
A.40% B.20% C.50% D.80%
3.下列物质的用途与性质之间的关系错误的是
A.金刚石裁玻璃——硬度大 B.氮气充入食品袋防腐——化学性质不活泼
C.石墨作电极——导电性 D.钨制灯泡里的灯丝——熔点低
4.目前应用最广泛的金属材料是铁和铁的合金,图甲是铁元素在周期表中的相关信息,图乙是铁原子结构示意图,下列说法正确的是
A.人体缺铁容易患贫血病,这里的“铁”是指铁原子
B.铁元素的原子序数为26,图乙中x的值为2
C.足量的铁钉与硫酸铜溶液反应生成红色固体和黄色溶液
D.铁丝在氧气中燃烧生成的黑色固体是氧化铁
5.中华优秀传统文化博大精深。下列成语的本意主要涉及化学变化的是
A.披荆斩棘 B.刻舟求剑 C.大浪淘沙 D.百炼成钢
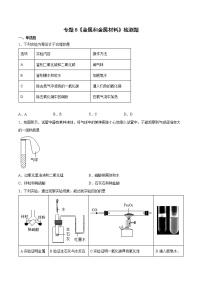
6.如图打开止水夹,将液体A滴入试管②中与固体B接触。若试管①中的导管口有较多气泡产生,则液体A和固体B的组合不可能是
A.双氧水和二氧化锰
B.稀盐酸和镁条
C.水和氢氧化钠
D.水和硝酸铵
7.我们生活在不断变化的物质世界中,下列变化中,属于物理变化的是
A.植物的光合作用 B.海水晒盐 C.钢铁生锈 D.食物变质
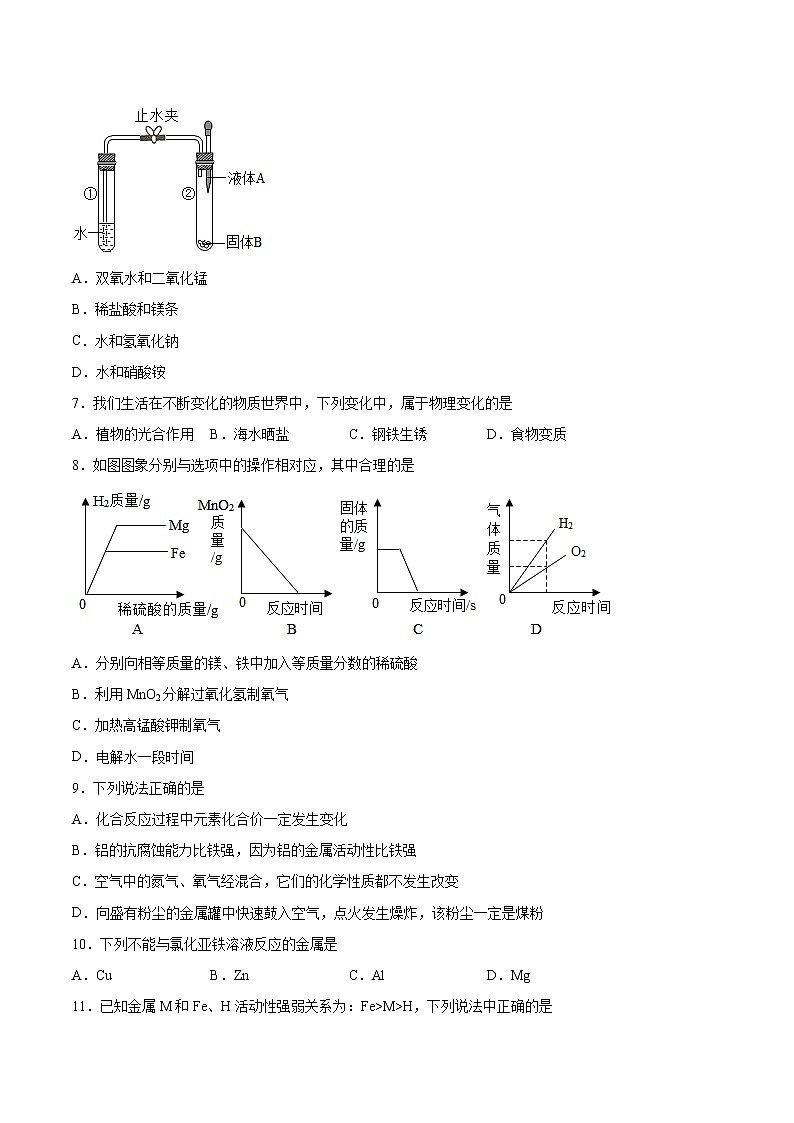
8.如图图象分别与选项中的操作相对应,其中合理的是
A.分别向相等质量的镁、铁中加入等质量分数的稀硫酸
B.利用MnO2分解过氧化氢制氧气
C.加热高锰酸钾制氧气
D.电解水一段时间
9.下列说法正确的是
A.化合反应过程中元素化合价一定发生变化
B.铝的抗腐蚀能力比铁强,因为铝的金属活动性比铁强
C.空气中的氮气、氧气经混合,它们的化学性质都不发生改变
D.向盛有粉尘的金属罐中快速鼓入空气,点火发生燥炸,该粉尘一定是煤粉
10.下列不能与氯化亚铁溶液反应的金属是
A.Cu B.Zn C.Al D.Mg
11.已知金属M和Fe、H活动性强弱关系为:Fe>M>H,下列说法中正确的是
A.将金属M放入Zn(NO3)2溶液中,有锌析出
B.将金属M放入CuSO4溶液中,没有明显现象
C.将金属铁放入AgNO3溶液中,一段时间后溶液质量变大
D.将金属铁(足量)放入M(NO3)2溶液中,溶液变为浅绿色
12.如图所示,试管中盛有某种液体,将气球中的某种固体小心地倒入试管中,不能观察到气球逐渐变大的一组物质是
A.过氧化氢溶液和二氧化锰 B.硝酸铵固体和水
C.锌粒和稀硫酸 D.石灰石和稀盐酸
二、简答题
13.生活中处处有化学。请用所学化学知识解释下列问题。
(1)为什么灯泡里的灯丝用钨制不用锡制?
(2)为什么电线用铜不用银?
(3)为什么在天然气中掺入微量具有难闻气味的气体?
14.佩戴口罩是预防感染新冠病毒的有效手段之一。
(1)某同学佩戴口罩仍能闻到阵阵花香,请从分子的角度解释该现象。
(2)口罩鼻梁上的金属条通常采用铝条,请用化学方程式解释铝条耐腐蚀的原因。
三、推断题
15.甲、乙、丙是初中化学常见的物质,物质间的转化关系如图所示(“→”表示两种物质间的转化关系,部分反应物、生成物及反应条件已略去)。请回答下列问题。
(1)若甲发生分解反应生成乙和丙,则:
甲发生反应的化学方程式为______;乙→丙的化学方程式为______。
(2)若甲→乙发生的化学反应为化合反应,则:
甲→丙发生置换反应的化学方程式为______;丙→乙的化学方程式为______。
16.下图中的A~I表示几种初中化学常见的物质,其中A、D、I是氧化物,I是一种有毒气体,B单质中的元素在地壳中的含量位居第三,C由三种元素组成,G为紫红色。图中“一”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物或反应条件已略去。
(1)写出G的化学式:_________。
(2)写出B→A反应的化学方程式:_________。
(3)写出E→G反应的化学方程式:_________。
(4)写出H→I反应的化学方程式:_________,此反应为_________。反应(填“吸热”或“放热”)。
17.爱好化学的体育老师在体育课上请7名同学做排队游戏,A ~ G 7名同学分别代表氧气、木炭、一氧化碳、二氧化碳、铜、氧化铁、硝酸银7种初中化学常见物质中的一种物质。
【游戏规则】
规则①:相对分子质量最大的A排在最前面。
规则②:A、B、C、D、E、F、G相邻之间能发生化学反应。
(1)写出以下物质的化学式:A_________;E___________。
(2)写出符合要求的化学方程式:
①A + B____________;
②C + D_____________;
③E→G______________。
(3)B与C反应的现象___________。
(4)D的一种用途是 ____________。
四、实验题
18.某校化学兴趣小组同学学习了金属活动性后,在实验室用下图装置进行实验,发现了一个有趣的实验现象:锌粉产生的气体比铝片的快。同学们依照金属活动性顺序,应该是铝片的快,究竟什么原因呢?请你与小组同学一起进行探究。
【讨论交流】
(1)按题中兴趣小组同学设计的实验方案比较金属铝、锌的活动性是否合理?______(填“是”或“否”),原因是______(回答出一个原因即可)。
(2)请写出铝与稀盐酸反应的化学方程式______。
【反思评价】
(3)某同学按题(1)中所提到的影响产生气体快慢的原因改进了实验方案,发现依然是锌反应产生气体快,铝刚开始时反应还是比锌慢的多,后来才慢慢快起来,原因是______。
(4)为了进一步确认铝、锌的活动性顺序,学习小组同学将打磨过的铝片插入盛有乙试管反应的溶液的烧杯中,通过______(填字母)的变化来证明铝、锌的活动性。
A.观察反应前后溶液颜色的变化
B.称量铝片(已进行干燥处理)反应前后质量是否明显增加
C.称量反应前后烧杯中溶液的质量是否明显减少
【拓展迁移】
(5)某学生在老师的指导下,将铅片加入到硫酸锌和硫酸铜的混合液中,充分反应一段时间后,混合液中离子数目一定增加的是______(用离子符号回答)。
19.铁是应用最广泛的金属,通过冶炼铁矿可以得到铁。
(1)高炉是工业炼铁的主要设备(如图1)。
①高炉炼铁中,焦炭的作用是_______(用化学方程式表示)。
②写出高炉中以赤铁矿为原料得到铁的化学方程式:_______。
(2)实验室用氧化铁粉末模拟炼铁(如图2),并探究产物成分。
①实验中观察到硬质玻璃管内固体全部变为黑色,澄清石灰水变浑浊:实验结束时,硬质玻璃管内物质冷却后才停止通一氧化碳的主要原因是________;该装置的一个明显缺陷是________。
②查阅资料发现:
一氧化碳还原氧化铁后剩余固体可能由四氧化三铁、氧化亚铁、铁粉和未反应的氧化铁中的一种或几种组成;进一步查得三种铁的氧化物的某些性质如下表:
| 氧化亚铁 | 氧化铁 | 四氧化三铁 |
颜色 | 黑色 | 红棕色 | 黑色 |
磁性 | 无 | 无 | 有 |
与硫酸铜溶液 | 不反应 | ||
与稀盐酸 | 反应生成可溶性物质,无气体放出 | ||
由实验中_________的现象,确认剩余固体中已无氧化铁。
③继续探究剩余固体的组成:
步骤 | 实验操作 | 实验现象 | 实验结论 |
1 | 用磁铁吸引剩余固体 | a_________ | 剩余固体中没有氧化亚铁 |
2 | b_________ | c_________ | 剩余固体中只有铁粉 |
五、计算题
20.将13克的锌粒放入87.4克的稀盐酸中,当锌粒完全反应后:
(1)最多可以放出多少克的氢气?
(2)盐酸溶液中溶质的质量分数是多少?
21.回答下列问题
(1)工厂中的废液含有硝酸银和硝酸铜。取用一定量的废液,加入镁粉和铜粉,反应过滤后得到滤液和滤渣。若滤渣中含有铜粉,则滤液中溶质一定含有_____。
(2)将等质量的镁、铁、锌,分别放入三份溶质质量分数相同的稀盐酸中,生成的H2质量与反应时间的关系如图所示。其中金属Z为_____。一定没有反应完的金属是_____。
(3)现有一块铁铜合金15g,将其置于298.6g的稀硫酸中恰好完全反应。过滤可得到9.4g的滤渣。此时滤液中溶质质量分数为_____。
参考答案:
1.B 2.B 3.D 4.B 5.D 6.D 7.B 8.A 9.C 10.A 11.D 12.B
13.(1)钨的熔点比锡高
(2)银的价格比铜贵
(3)一旦天然气泄漏,人们能及早察觉
14.(1)分子体积小且分子在不断运动
(2)4Al + 3O2=2Al2O3
15.(1) 2H2O22H2O+O2↑ 2H2O2H2↑+O2↑(合理即可)
(2) C+2CuO2Cu+CO2↑(合理即可) C+CO22CO
16.(1)Cu
(2)
(3)
(4)
吸热
17.(1)
(2)
(3)红色固体变黑
(4)作燃料、冶炼金属等
18.(1) 否 所用酸的种类不同或浓度未知或金属形状不同
(2)
(3)铝表面有一层氧化铝薄膜
(4)BC
(5)Al3+
19.(1) 和
(2) 防止生成的铁在高温条件下再次被氧化 没有尾气处理装置 红棕色粉末完全转化为黑色 黑色固体被全部吸引 往剩余固体中加足量硝酸铜 黑色固体全部变成红色
20.(1)设最多可以放出的氢气的质量为x
故最多可以放出0.4克的氢气。
(2)设参加反应的盐酸的质量为y
故盐酸溶液中溶质的质量分数是。
21.(1)硝酸镁
(2) 铁 镁
(3)5%
初中化学仁爱湘教版九年级下册专题七 初识酸、碱和盐综合与测试同步达标检测题: 这是一份初中化学仁爱湘教版九年级下册专题七 初识酸、碱和盐综合与测试同步达标检测题,共11页。试卷主要包含了单选题,简答题,推断题,实验题,计算题等内容,欢迎下载使用。
仁爱湘教版九年级下册专题八 金属和金属材料综合与测试课时练习: 这是一份仁爱湘教版九年级下册专题八 金属和金属材料综合与测试课时练习,共9页。试卷主要包含了单选题,简答题,推断题,实验题,计算题等内容,欢迎下载使用。
初中化学仁爱湘教版九年级下册专题八 金属和金属材料综合与测试练习: 这是一份初中化学仁爱湘教版九年级下册专题八 金属和金属材料综合与测试练习