
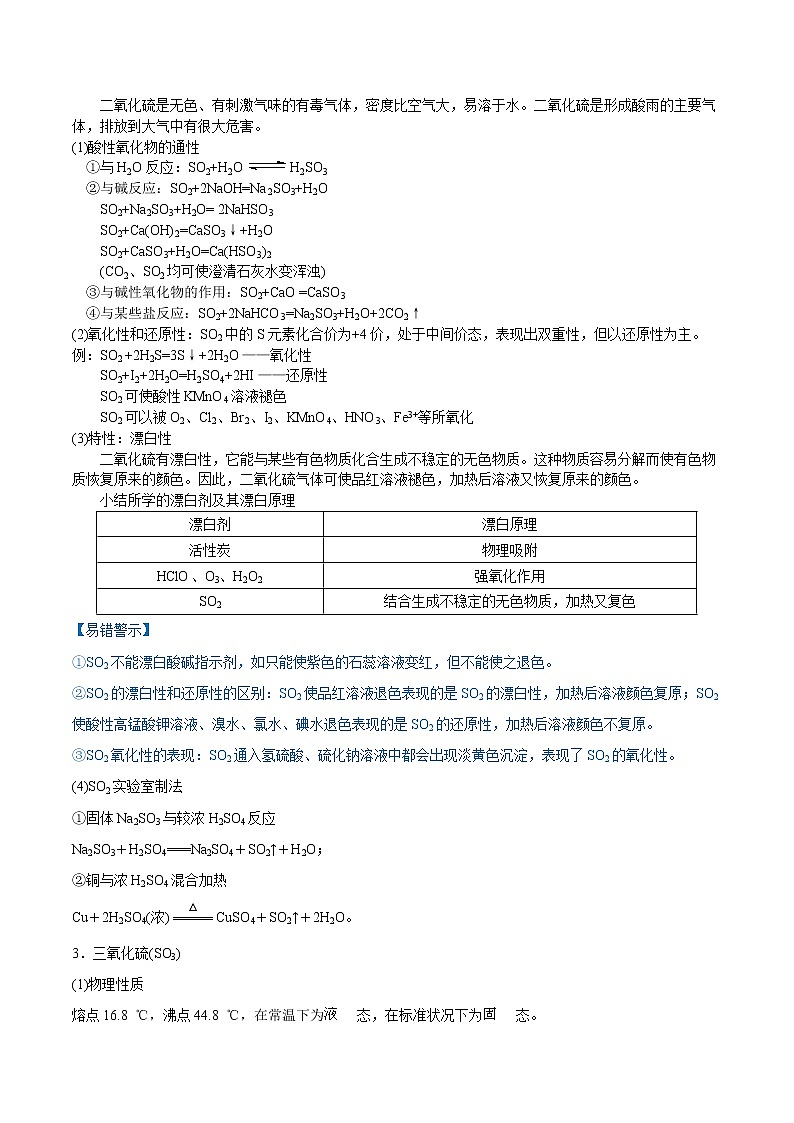




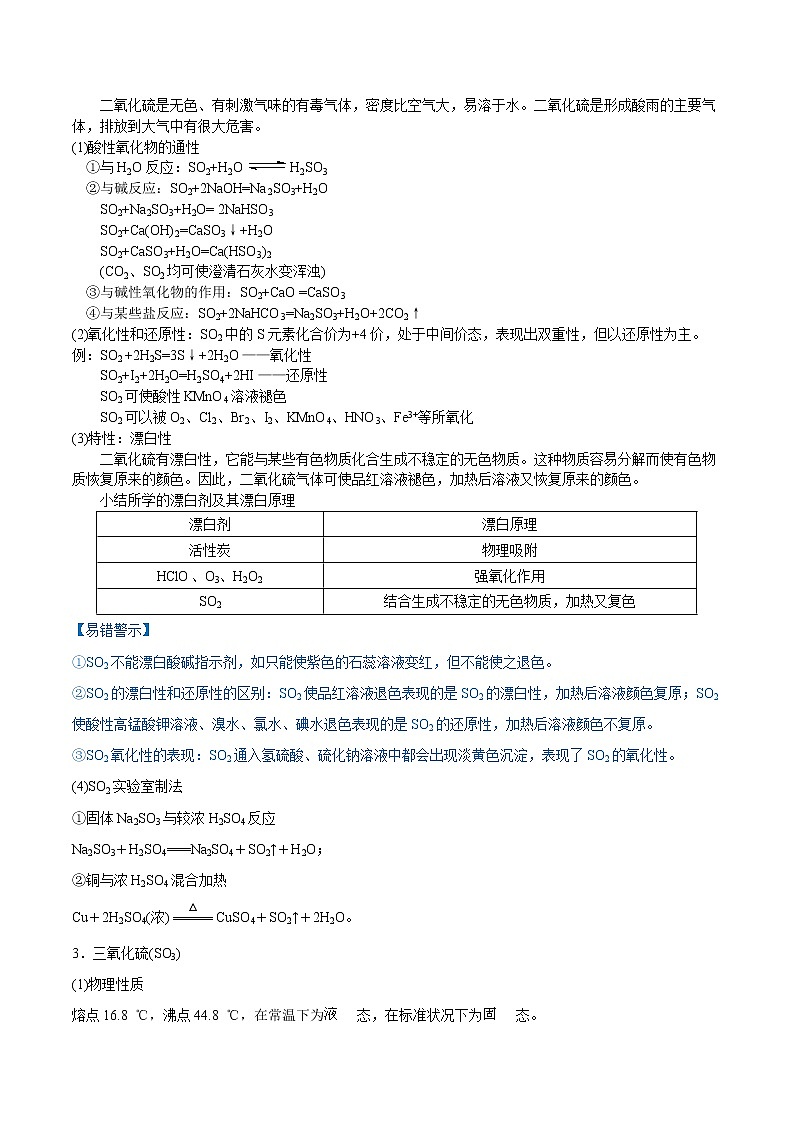




第五章-化工生产中的重要的非金属元素-知识串讲和检测试题(有答案)2021-2022学年高一化学下学期期末复习(人教版必修第二册)
展开
这是一份第五章-化工生产中的重要的非金属元素-知识串讲和检测试题(有答案)2021-2022学年高一化学下学期期末复习(人教版必修第二册),文件包含第五章知识串讲-2021-2022学年高一化学下学期期末复习大串讲人教版必修第二册解析版doc、第五章知识串讲-2021-2022学年高一化学下学期期末复习大串讲人教版必修第二册原卷版doc、第五章检测试题-2021-2022学年高一化学下学期期末复习测试卷人教版必修第二册解析版doc、第五章检测试题-2021-2022学年高一化学下学期期末复习测试卷人教版必修第二册原卷版doc等4份试卷配套教学资源,其中试卷共51页, 欢迎下载使用。
第五章 化工生产中的重要非金属元素测试卷一、选择题(第小题只有一个正确选项,共16*3分)1.下列物质能用于制造光导纤维的是A.钢 B.陶瓷 C.二氧化硅 D.聚乙烯2.下列物品或设备的成分中含有二氧化硅的是①门窗玻璃②计算机芯片③石英钟表④玛瑙首饰⑤硅太阳能电池⑥光导纤维A.①③④⑥ B.全部 C.②⑤ D.①⑥3.起固氮作用的转化是A.N2→NH3 B.NO→NO2 C.NH3→NO D.HNO3→NH4NO34.下列溶液由于久置空气中,被氧气氧化而变黄色的是A.浓硝酸 B.硫酸亚铁 C.碘水溶液 D.工业盐酸5.如图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴定管内盛放某种液体。挤压滴管的胶头,下列与实验事实不相符的是A.SO2(H2O含石蕊)/蓝色喷泉 B.NH3(H2O含酚酞)/红色喷泉C.H2S(NaOH溶液)/无色喷泉 D.HCl(AgNO3溶液)/白色喷泉6.下列关于氨与铵盐的叙述中不正确的是A.碳酸氢铵受热分解有氨气产生B.干燥NH3时,不可以用酸性干燥剂,也不可以用中性干燥剂CaCl2C.铵盐作氮肥时,与生石灰混用的效果更好D.铵盐的物理共性是铵盐都是晶体,都能溶于水7.下列实验设计正确的是A.将SO2通入溴水中证明SO2具有漂白性B.将亚硫酸钠与硫酸反应产生的气体通入品红溶液,品红褪色证明SO2具有还原性C.SO2和SO3混合气体通入Ba(NO3)2溶液可得到BaSO3和BaSO4D.二氧化硫能使碘水褪色,说明二氧化硫具有还原性8.区分二氧化硫和二氧化碳可以采用通过A.澄清石灰水 B.品红溶液 C.石蕊试液 D.NaOH溶液9.下列陈述Ⅰ、Ⅱ正确并且有因果关系的是选项陈述Ⅰ陈述ⅡANH3的水溶液可以导电NH3是电解质B浓硫酸有吸水性浓硫酸可用于干燥H2和COCSiO2有导电性SiO2可用于制备光导纤维DSO2通入硝酸钡溶液出现白色沉淀BaSO3不溶于强酸A.A B.B C.C D.D10.向50mL 18mol/L的浓硫酸中加入足量的铜并加热,充分反应后,被还原的H2SO4的物质的量A.大于0.9mol B.等于0.45molC.在0.45mol与0.9mol之间 D.小于0.45mol11.下列有关实验方法正确的是A.用铜片和浓硝酸反应制NO B.用浓硫酸干燥NH3C.加热NH4Cl和Ca(OH)2固体混合物制取NH3 D.用排水法收集NO212.下列说法正确的是A.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在B.NO可用于某些疾病的治疗C.NO2通入FeSO4溶液中始终无明显现象D.可用湿润的淀粉-KI试纸鉴别NO2和Br2(g)13.下列叙述不正确的是A.浓硫酸、浓硝酸露置于空气中,溶液质量均增加B.常温下,浓硝酸能在铁质容器中盛放C.浓硝酸见光或受热易分解,必须保存在棕色瓶中D.将蘸有浓盐酸的玻璃棒与蘸有浓氨水的玻璃棒靠近产生大量白烟14.在一定条件下,将8体积NO2和NO的混合气体置于试管中,并将试管倒置于水中,当通入4体积的O2充分反应后,剩余1体积气体,则原NO体积可能为①2体积②3体积③4体积④5体积⑤5.5体积A.② B.③或④ C.①或⑤ D.②或⑤15.将44.8gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4 、NO2)的混合物共0.9mol,这些气体恰好能被500mL2mol/LNaOH溶液完全吸收,生成只含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量为A.0.5mol B.0.4mol C.0.3mol D.0.2mol16.将一定量硫酸、硝酸和KNO3溶液混合成100ml溶液,其中H2SO4、HNO3和KNO3的物质的量浓度分别是6mol/L,2mol/L和1mol/L,向其中加入过量的铜粉,可产生标准状况下的混合气体体积为A.11.2L B.6.72L C.8.96L D.4.48L二、主观题(共5小题,共52分)17.(10分)按要求填空(1)浓硫酸具有如下的性质:A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。①浓硫酸使蔗糖变黑___________②碳投入热的浓硫酸中溶解___________③浓硫酸与氧化铜反应___________④浓硫酸干燥氢气___________(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。①浓硝酸需避光保存___________②常温下可用铝或者铁遇浓硝酸钝化___________(3)二氧化硫气体在下列反应中表现的性质填写在横线上。A.氧化性B.漂白性C.还原性D.酸性氧化物的性质①SO2+2OH-=+H2O___________②SO2+2H2S=3S↓+2H2O___________③SO2+Ca(OH)2=CaSO3↓+H2O___________④SO2+Cl2+2H2O=2HCl+H2SO4___________18.(10分)氮元素是地球大气中含量最多的元素,请完成下列有关问题:(1)写出氮元素的原子结构示意图:___________。(2)通常情况下,氮气性质不活泼,其原因是___________。A.氮分子是双原子分子B.氮元素的非金属性很强C.氮原子的半径较小D.破坏氮分子中的化学键很难(3)N2的电子式:___________。(4)氨是一种重要的化工原料,请写出工业合成氨的化学方程式:___________。(5)NH4NO3是常用的铵态氮肥,在施用时若受热会释放出___________而降低肥效。检验的方法是___________。19.(12分)Si是现代社会半导体工业发展的基石。(1)硅元素在自然界中的存在形式有_______A、游离态 B、化合态 C、游离态和化合态都有硅的氧化物属于_______氧化物(填“酸性”、 “两性”或“碱性" )。(2)SiO2是玻璃的主要成分之一,故SiO2可以用作_______,SiO2与氢氧化钠溶液反应的化学方程式为_______,工艺师常用_______(填物质名称)来雕刻玻璃。(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可用作_______。Na2SiO3可通过SiO2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是_______。A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚(4)制备硅半导体材料必须先得到高纯硅,三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如图:石英砂粗硅SiHCl3(粗) SiHCl3(纯)高纯硅①写出由纯SiHCl3制备高纯硅的化学反应方程式_______;②整个制备过程必须严格控制无水无氧,SiHCl3遇水剧烈反应生成H2SiO3,HCl和另一种物质,写出配平的化学反应方程式_______20.(8分)(1)氮氧化物进入大气后,不仅会形成硝酸型酸雨,还能对臭氧层破坏,还可能形成___________,因此必须对含有氮氧化物的废气进行处理。用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:NO2+NO+2NaOH =2NaNO2+H2O①2NO2+2NaOH =NaNO3+ NaNO2+H2O②在反应①中,氧化剂是___________,在反应②中,还原剂是___________。(2)汽车尾气中含有氮的氧化物(用NOx表示)和CO,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成N2和CO2,则该反应的化学方程式为___________ 。(3)某校化学研究性学习小组的同学,按下列流程探究不同催化剂对NH3还原NO反应的催化性能。若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通入滴有酚酞的稀硫酸溶液,通过测量并记录稀硫酸溶液显色所需要时间的不同,可比较不同催化剂的催化性能,则实验时对每次使用的硫酸溶液的要求是___________。21.(12分)甲、乙、丙三位同学分别用下图所示实验装置制取氨气。请你根据实验探究的过程,回答下列有关问题。(1)三位同学制取氨气的化学方程式是___________。(2)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(实验操作都正确),你认为没有收集到氨气的同学是___________(填“甲”、“乙”或“丙”)。(3)为确定试管内是否已收集满氨气,将蘸有浓盐酸的玻璃棒接近试管口,观察的现象是___________,该反应的化学方程式是___________。(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的同学是___________(填“甲”、“乙”或“丙”)。(5)氨是一种重要的化工产品,经过一系列反应可以得到硝酸,其中氨被氧化生成一氧化氨的化学方程式为___________。
相关试卷
这是一份第5章 化工生产中的重要非金属元素——【期末复习】高一化学单元复习知识点梳理(人教版2019必修第二册),共14页。
这是一份第五章 化工生产中的重要非金属元素【过知识】-2022-2023学年高一化学单元复习(人教版2019必修第二册),共60页。PPT课件主要包含了考点一硫和二氧化硫,知识复习,硫酸的性质,硫酸根离子的检验,一氮气,氮的固定和循环,考点五氨和铵盐,一氨的物理性质,二氨气的化学性质,三氨的实验室制法等内容,欢迎下载使用。
这是一份第五章 化工生产中的重要非金属元素【知识清单】-2022-2023学年高一化学单元复习(人教版2019必修第二册),共17页。试卷主要包含了硫的存在,物理性质,化学性质,氨气的还原性,氨的用途等内容,欢迎下载使用。








