

还剩4页未读,
继续阅读
初中化学第5章 金属的冶炼与利用综合与测试测试题
展开这是一份初中化学第5章 金属的冶炼与利用综合与测试测试题,共7页。试卷主要包含了单选题,简答题,推断题,实验题,计算题等内容,欢迎下载使用。
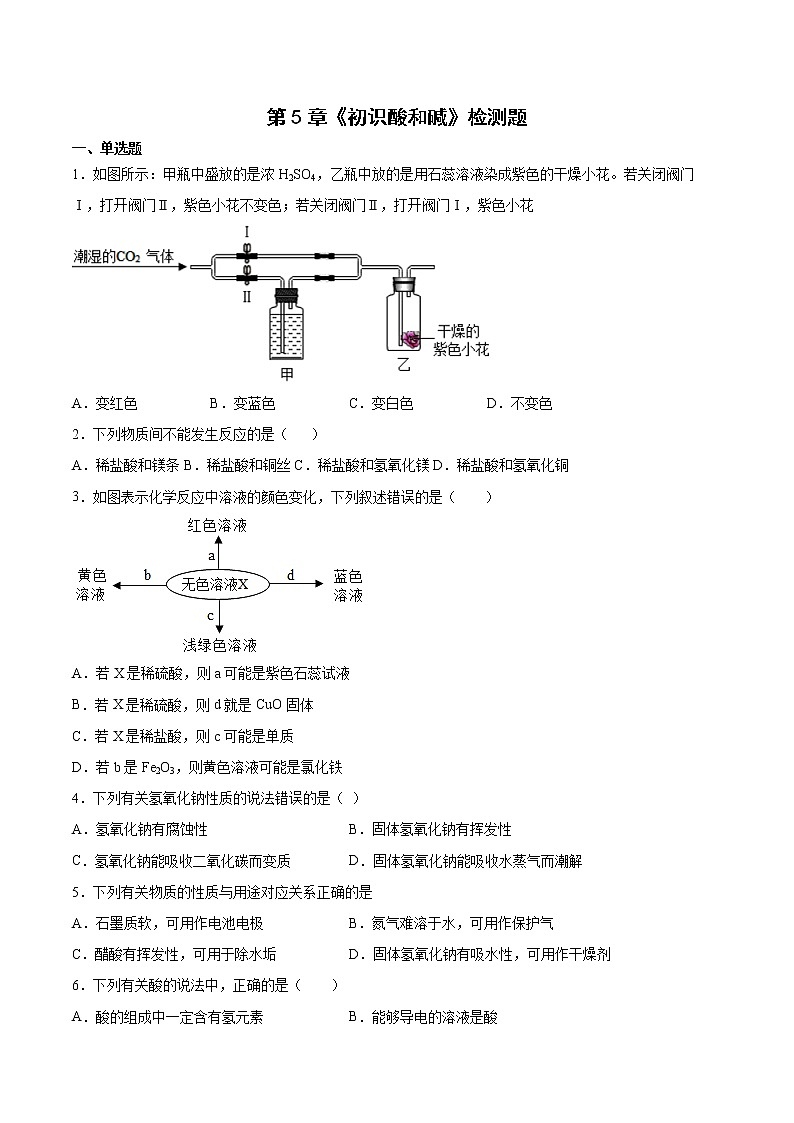
1.如图所示:甲瓶中盛放的是浓H2SO4,乙瓶中放的是用石蕊溶液染成紫色的干燥小花。若关闭阀门Ⅰ,打开阀门Ⅱ,紫色小花不变色;若关闭阀门Ⅱ,打开阀门Ⅰ,紫色小花
A.变红色B.变蓝色C.变白色D.不变色
2.下列物质间不能发生反应的是( )
A.稀盐酸和镁条B.稀盐酸和铜丝C.稀盐酸和氢氧化镁D.稀盐酸和氢氧化铜
3.如图表示化学反应中溶液的颜色变化,下列叙述错误的是( )
A.若X是稀硫酸,则a可能是紫色石蕊试液
B.若X是稀硫酸,则d就是CuO固体
C.若X是稀盐酸,则c可能是单质
D.若b是Fe2O3,则黄色溶液可能是氯化铁
4.下列有关氢氧化钠性质的说法错误的是( )
A.氢氧化钠有腐蚀性B.固体氢氧化钠有挥发性
C.氢氧化钠能吸收二氧化碳而变质D.固体氢氧化钠能吸收水蒸气而潮解
5.下列有关物质的性质与用途对应关系正确的是
A.石墨质软,可用作电池电极B.氮气难溶于水,可用作保护气
C.醋酸有挥发性,可用于除水垢D.固体氢氧化钠有吸水性,可用作干燥剂
6.下列有关酸的说法中,正确的是( )
A.酸的组成中一定含有氢元素B.能够导电的溶液是酸
C.滴加无色酚酞不变色的溶液是酸D.能与碱发生反应的物质是酸
7.下列关于盐酸用途的叙述中错误的是
A.用于金属表面除锈
B.在实验室用作干燥剂
C.人体胃液中含有盐酸,可帮助消化
D.实验室用稀盐酸与石灰石反应来制取二氧化碳
8.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如下。由此分析下列说法正确的是
A.反应前后阴、阳离子的总数目不变
B.反应前后溶剂质量不变
C.反应后溶液呈中性
D.反应前后元素种类发生了变化
9.下列关于氢氧化钠的描述中不正确的是
A.曝露在空气中易潮解B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红D.对皮肤有强烈的腐蚀作用
10.下列描述正确的是( )
A.“H”既可以表示宏观的氢元素,也可以表示微观的一个氢原子
B.烧碱、熟石灰、纯碱按物质分类均属于碱
C.金刚石、均为碳单质,所以物理性质、化学性质完全相同
D.泡沫灭火器灭火的原理是提高了可燃物质的着火点
11.下列化学方程式与事实相符且正确的是( )
A.甲烷在空气中完全燃烧:
B.用含氢氧化铝的药物治疗胃酸过多:2Al(OH)3+3H2SO4═Al2(SO4)3+6H2O
C.三氧化硫与氢氧化钠溶液的反应:SO3+2NaOH═Na2SO4+H2O
D.赤铁矿溶于盐酸:Fe2O3+2HCl═FeCl3+H2O
12.下列物质的性质与其用途不匹配的是
A.石墨质软——用作电池的电极材料
B.不锈钢耐腐蚀——制造医疗器械
C.熟石灰显碱性——用来改良酸性土壤
D.干冰易升华——用于人工降雨
13.下列有关溶液的说法正确的是( )
A.均一、稳定的液体一定是溶液
B.稀释浓硫酸时,会放出大量的热
C.降低温度,不饱和溶液一定能变成饱和溶液
D.实验室利用氯化钠固体和水配制50g质量分数为6%的氯化钠溶液的步骤是:计算、量取、溶解、贮存
二、简答题
14.硫酸和盐酸是实验室常用的试剂,它们具有相似的化学性质。小华同学在复习有关酸的化学性质时,归纳出以下几点,但并不完整,请你和他一起完成。
(1)酸的化学性质,化学方程式举例
①与多种活泼金属反应,Mg+H2SO4===MgSO4+H2↑
②与某些金属氧化物反应_______________________________
(2)生活中的食醋含有醋酸,用铁锅炒菜时放点食醋,可补充人体需要的微量元素铁,该反应的原理体现了酸的化学性质________(填上表中的序号)。
(3)盐酸、硫酸、醋酸具有相似的化学性质是因为它们的水溶液中都含有________。
15.请用微观角度解释下列现象。
(1)春季花开,香飘满园。____________
(2)稀盐酸和稀硫酸具有相似化学性质的原因是什么?____________
三、推断题
16.如图所示,是初中化学常见的物质,和可发生中和反应,常用作食品干燥剂,为单质.根据图示回答下列问题.
(1)的俗称为______.
(2)的化学式为______.
(3)反应②的化学方程式为______.
17.如图是某同学学习了氢氧化钠的化学性质后绘制的知识网络图,其中A、B、C分别表示不同类别的化合物,已知A是一种硫酸盐,其溶液呈蓝色,B能用于灭火,“﹣”表示相连两物质之间能相互 反应。
(1)按物质分类,C属于______(填“氧化物”、“酸”、“碱”或“盐”);
(2)写出A、B的化学式:A_____;B ______;
(3)写出C的一种物质与NaOH反应的化学方程式______
(4)NaOH与A反应的实验现象是______。
18.A、B、C、D、E是初中化学常见的五种不同类别的物质。其中B的固体可用于人工降雨,C的组成元素在地壳中含量居第四位,D常用于清洗油污。图中“﹣”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略)。请回答下列问题。
(1)B的化学式是_____。
(2)B与D反应的化学方程式是_____。
(3)A与D反应的微观本质是_____,该反应属于反应类型中的_____。
(4)C与E反应的化学方程式是_____,反应现象是_____。
四、实验题
19.不同实验对反应速率有不同要求。某同学探究CO2制取实验,请按要求答题。
限选控制反应速率的方法:①反应物的浓度 ②反应物的状态
限选试剂:A.稀盐酸 B.浓盐酸 C.块状石灰石 D.碳酸钠溶液 E.粉末状石灰石
用上述字母或数字填写下表并回答相关问题[温馨提示:碳酸钠与碳酸钙的化学性质相似]。
写出灭火器反应原理的化学方程式_____。
五、计算题
20.已知CuO被C还原的产物是 Cu2O(红色)。现有 CuO 和木炭粉组成的混合物4.36g,在高温下充分反应后,得到红色固体产物。反应后产生的气体能全部被过量的澄清的石灰水吸收,得沉淀3.00g。试计算所得红色固体产物质量。
21.称取5g含杂质的氢氧化钙固体样品放入烧杯中,向烧杯中加入50g溶质的质量分数为7.3%的稀盐酸(假设杂质不与稀盐酸反应),二者恰好完全反应。请计算:固体样品中氢氧化钙的质量分数。
实验名称
控制速率的方法
所选用的最佳试剂
灭火器反应原理
①
_____和D
CO2的实验室制法
_____
A和C
参考答案:
1.A 2.B 3.B 4.B 5.D 6.A 7.B 8.C 9.C 10.A 11.C 12.A 13.B 14. Fe2O3+6HCl===2FeCl3+3H2O ② 氢离子(或H+)
15. 分子是在不断运动的 稀盐酸和稀硫酸中都含有氢离子
16. 熟石灰(或消石灰)
17. 酸 CuSO4 CO2 产生蓝色沉淀
18. CO2 2NaOH+CO2=Na2CO3+H2O 氢离子和氢氧根离子反应生成水 复分解反应 Fe+CuCl2=FeCl2+Cu 铁表面有红色物质析出,溶液由蓝色变成浅绿色
19. B ② 2HCl+Na2CO3=2NaCl+H2O+CO2
20.设要生成3.00g沉淀需要二氧化碳的质量为
根据质量守恒定律可知:CuO和木炭粉组成的混合物4.36g,最后质量减少的原因是生成了二氧化碳,所以用4.36g减去二氧化碳的质量就是最后生成的红色固体的质量,所以所得红色固体产物质量为4.36g-1.32g=3.04g;
答:所得红色固体产物质量3.04g。
21.74%
相关试卷
沪教版 (上海)九年级第二学期5.2 酸和碱的性质研究第一课时综合训练题:
这是一份沪教版 (上海)九年级第二学期5.2 酸和碱的性质研究第一课时综合训练题,共8页。试卷主要包含了能使紫色石蕊试液变红的是,下列关于浓盐酸的说法错误的是,下列家庭常用物质中,含有酸的是等内容,欢迎下载使用。
初中化学沪教版 (上海)九年级第二学期第五单元 初识酸和碱5.2 酸和碱的性质研究第二课时同步练习题:
这是一份初中化学沪教版 (上海)九年级第二学期第五单元 初识酸和碱5.2 酸和碱的性质研究第二课时同步练习题,共8页。试卷主要包含了下列物质不能与氢氧化钠反应的是,下列物质放在空气中易潮解的是,下列四种常见液体中,呈碱性的是,氢氧化钠和酚酞反应的现象,氢氧化钠固体要密封保存等内容,欢迎下载使用。
沪教版 (上海)九年级第二学期5.1 生活中的酸和碱课后作业题:
这是一份沪教版 (上海)九年级第二学期5.1 生活中的酸和碱课后作业题,共9页。试卷主要包含了酸的组成中一定含有,物质的组成中一定不含氢元素的是,下列物质分类,属于二元酸的是,下列物质,属于盐类的一组是,下列属于中和反应的是等内容,欢迎下载使用。









