

2021-2022学年重庆市巴蜀中学九年级(下)开学化学试卷
展开一、选择题(本大题共16小题,每小题2分,共32分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.(2分)生活中的下列操作,不涉及化学变化的是( )
A.干冰人工降雨 B.酿制葡萄酒
C.漂白粉消毒自来水D.点燃煤气
2.(2分)如图所示的化学实验基本操作中,正确的是( )
3.(2分)下列实验现象正确的是( )
A.细铁丝在空气中剧烈燃烧,火星四射,有黑色固体生成
B.红磷在空气中燃烧,发出红色的火焰,产生大量白色烟雾
C.碳还原氧化铜,黑色的氧化铜变成红色的铜,生成二氧化碳
D.向装有紫色石蕊溶液的试管中通入二氧化碳,溶液变成红色
4.(2分)下列有关水的说法正确的是( )
A.用过滤的方法可以使硬水软化
B.水在通电条件下可分解为氢气和氧气,说明水是由氢气和氧气组成的
C.明矾是净水的絮凝剂
D.蒸馏水不能养鱼,是因为蒸馏水中没有氧元素
5.(2分)“吃出营养、吃出健康”是人们普遍的饮食追求,下列说法不正确的是( )
A.人体缺乏维生素A会引起夜盲症
B.食用甲醛浸泡的食物会危害人体健康
C.不吃霉变或超过保质期的食物
D.微量元素钙对人体十分重要,必须大量服用
6.(2分)将一定量的下列固体放入适量水中,能形成溶液且温度明显升高的是( )
A.CaCO3B.NaOHC.NaClD.NH4NO3
7.(2分)下列化学用语书写正确的是( )
A.三个二氧化硫分子:2SO3
B.钙离子:Ca+2
D.硫酸铁:FeSO4
8.(2分)镍在元素周期表中的信息如图所示,下列有关镍元素的说法不正确的是( )
9.(2分)冬季是感冒的高发季节,对乙酰氨基苯酚(C8H9NO2)是速效感冒胶囊的有效成分之一,下列有关对乙酰氨基苯酚说法正确的是( )
A.对乙酰氨基苯酚中含有氧分子
B.对乙酰氨基苯酚中含有8个碳原子、9个氢原子、1个氮原子、2个氧原子
C.对乙酰氨基苯酚的相对分子质量为151g
D.对乙酰氨基苯酚中碳、氧元素的质量比为3:1
10.(2分)下列有关溶液的说法错误的是( )
A.溶液是均一、稳定的混合物
B.溶液中的溶质可以是固体、液体或气体
C.某种溶液中溶质和溶剂都只能是一种
D.洗涤剂能洗去衣服上的油污,原因是洗涤剂具有乳化作用
11.(2分)下列实验设计,不能达到实验目的的是( )
A.AB.BC.CD.D
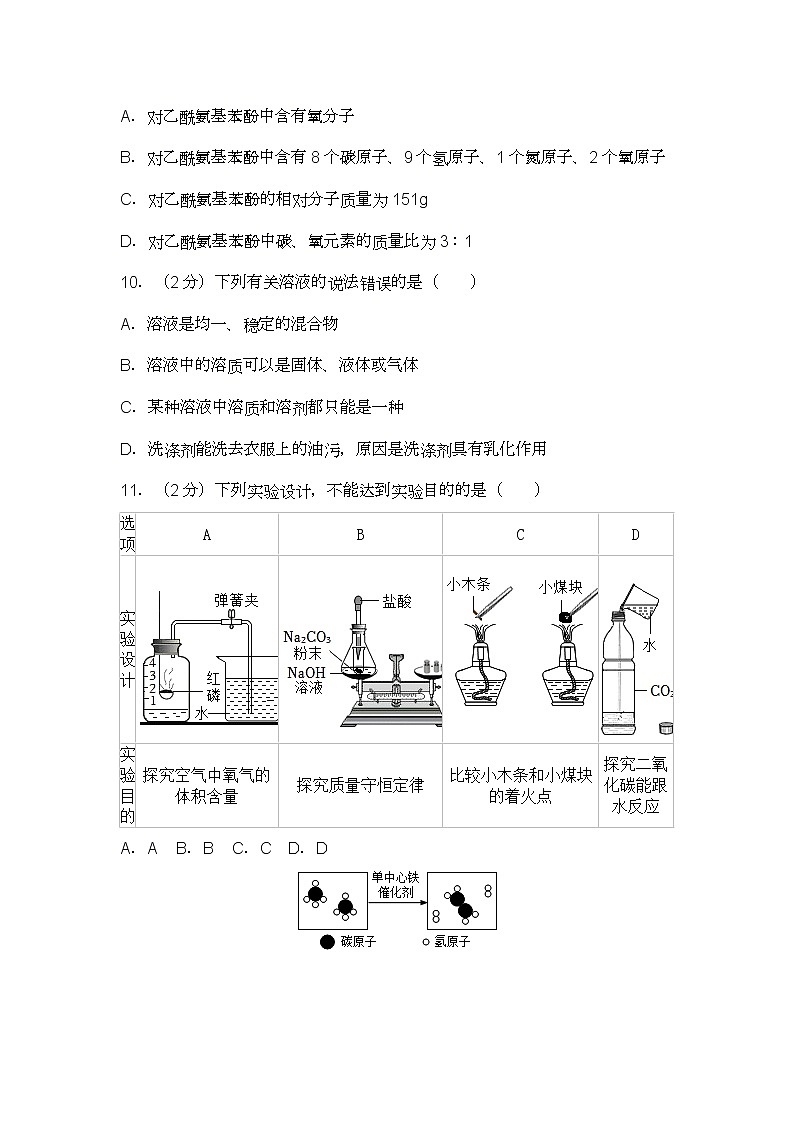
12.(2分)我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破。如图为该转化的微观示意图,下列有关转化的说法错误的是( )
A.反应前后分子的种类发生了变化
B.生成物之一为C2H4
C.反应前后分子的个数没有变化
D.催化剂改变了反应速率
13.(2分)下列实验操作中,不能达到实验目的的是( )
A.AB.BC.CD.D
14.(2分)一定质量M、N两种金属,分别与相同质量和相同质量分数的稀硫酸反应,生成氢气的质量与反应时间的关系如图所示。分析图象得到的以下结论中,不正确的是( )
15.(2分)工业炼铁的部分反应如下所示,则( )
A.X可以是木炭
B.X与CO都具有氧化性
C.③反应后的尾气可直接排放
D.Y中铁元素的化合价一定是+3
16.(2分)为验证铁、铜、银的金属活动性顺序,某同学设计了如图四组实验。下列说法错误的是( )
A.通过实验①、②,能验证金属活动性:Fe>Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu
D.实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag
二、填空题(共21分)
17.(4分)化学就在我们身边,人类的生活离不开化学。
(1)从下列选项中选择一种适当的物质填空,并将字母序号填写在横线上。
A.水果
B.钛合金
C.医用酒精
D.碳酸钙
①健康:食用_____以补钙。
②医疗:可用______制造人造骨骼。
(2)“杂交水稻之父”袁隆平“一稻济天下”,在不断培育高产杂交水稻的同时,还成功培育出了适宜在盐碱地上种植的“海水稻”。
①“杂交水稻”富含淀粉,淀粉属于六大基本营养素中的______。
②“海水稻”富含硒,硒是人体必需的______(选填“微量”或“常量”)元素。
18.(4分)中国探月工程“绕”“落”“回”三步走规划如期完成。回答下列问题:
(1)嫦娥二号由长征三号丙火箭送入既定轨道。长征三号丙火箭的三级推进剂为液氢和液氧,构成它们的微粒为______(用化学用语填空)。
(2)嫦娥三号着陆地球表面,对可能存在的He-3等进行探测。He-3原子的原子核内有2个质子和1个中子,其原子结构示意图为_________。
(3)嫦娥四号的月球车靠太阳能从月夜中唤醒,已完成25个月昼的探测工作。下列能源中,与太阳能一样属于新能源的是_______(填序号)。
A.风能
B.潮汐能
C.化石燃料
(4)2020年12月17日,嫦娥五号携带月壤样品成功返回地球。月球岩石中的长石以钙长石(CaO•Al2O3•2SiO2)为主,钙长石中共含有____种金属元素。
19.(4分)H2O2溶液常用作的消毒剂。
(1)H2O2溶液的溶剂是水,写出电解水的化学方程式______。
(2)H2O2中含有一种带负电的原子团——过氧根离子,请写出过氧化钡的化学式__________。
(3)H2O2不稳定,易分解。H2O2分解的化学方程式为_______。
(4)用3%的H2O2溶液对不同金属进行腐蚀性实验,结果如表:
下列金属制品用该溶液浸泡消毒时,最易被腐蚀的是_______(填序号)。
A.不锈钢锅
B.铝盆
C.铜火锅
20.(5分)大量实验证明,化学反应符合质量守恒定律。
(1)如图是铁钉与硫酸铜溶液反应的实验。
①反应一段时间,观察到的现象是_____________________。
②该反应的化学方程式是____________________。
③有关该反应的说法正确的是_______________。
A.溶液减少的质量等于生成的铜和参加反应的铁的质量之差
B.固体质量增加了,所以不符合质量守恒定律
C.反应前后溶液中金属阳离子数目没变化
(2)由质量守恒定律可知,化学反应前后一定不变的是______________(填序号)。
①原子种类
②原子数目
③分子种类
④分子数目
⑤元素种类
⑥物质种类
(3)经计算3g镁和100g含氯化氢7.3g的稀盐酸充分反应可生成氢气0.2g,但经实验测得生成氢气的质量大于0.2g,则可能的原因是过量的镁与_____发生反应。
21.(4分)2022年1月,世界气象组织公布:2020年全球CO2含量创人类历史新高,2021年仍在上升。采用物理或化学方法捕集CO2并将其资源化利用,正成为控制排放的有效措施。
(1)煅烧炉内反应的化学方程式为____________________。
(2)温度对CO2的转化率影响较大,由图2可知,捕集器内温度应控制在_____℃为宜。
(3)“催化Ⅰ室”生成CO和H2O,该反应中充当还原剂的物质是_______(填物质名称)。
(4)乙烯(C2H4)是“催化Ⅱ室”的生成物之一,写出一氧化碳和氢气在一定条件下生成乙烯和水的反应的化学方程式:_________________________。
三、实验题(共11分)
22.(5分)下列实验仪器常用于实验室制取气体,回答下列问题:
(1)写出仪器的名称:A______。
(2)用大理石和稀盐酸反应制取CO2,并用向上排空气法收集。
①组装制取装置时,可选用图中的A、H、I、J、L、P和_______;
②检验CO2是否收集满的操作是________。
(3)用高锰酸钾制取氧气,并用排水法收集,该反应的化学方程式是______________________________________________________________________。
(4)氢化钙(CaH2)常温下能与水反应生成氢氧化钙和H2,是野外工作人员便携燃料的来源。请写出氢化钙(CaH2)与水反应的化学方程式________。
23.(6分)因发现青蒿素而获诺贝尔奖的科学家屠呦呦还发现了双青蒿素,查阅资料可知,双青蒿素由碳、氢、氧三种元素组成。为测定双青蒿素中碳、氢、氧三种元素的质量比。兴趣小组进行了以下探究。
【设计实验】兴趣小组设计并进行了如图一所示的实验。(装置气密性良好)
将7.1g双青蒿素放在装置C的玻璃管中,燃烧至无固体灰分残留。
(1)装置A、B中盛放的试剂分别是______(填序号)。
①足量NaOH溶液、足量浓硫酸
②足量浓硫酸、足量NaOH溶液
(2)装置F可吸收从装置E的气流中带出来的少量水蒸气,生石灰与水蒸气发生反应的化学方程式是__________。
【记录数据】加热前,先通入空气一段时间,再称量装置D的质量、装置E和F的总质量(反应前的质量)。双青蒿素完全反应后,停止加热,继续通入空气一段时间,再次称量装置D的质量、装置E和F的总质量(反应后的质量),实验数据如表所示。
【实验结论】(3)根据表中数据分析,双青蒿素中碳、氢、氧三种元素的质量比是___________。
【拓展分析】(4)双青蒿素分子中碳、氢、氧三种原子的个数比是___________________。
【实验反思】(5)实验过程中,加热前要先通入空气一段时间,该操作的作用是___________。
(6)有同学建议,为使实验结果更准确,需要在装置C和D之间增加图二所示的装置,其目的是____________________。
四.计算题(共6分)
24.(6分)孔雀石主要成分是碱式碳酸铜[Cu2(OH)2CO3],另外还含有少量的SiO2等杂质(杂质不与硫酸发生反应)。某化学兴趣小组为测定孔雀石中Cu2(OH)2CO3的含量进行如下实验:取30g孔雀石样品,粉碎后放入烧杯中,将200g稀硫酸分成四等份,分四次加入烧杯中,测出每次完全反应后烧杯内物质的总质量,实验数据记录如表:
请完成:
(1)Cu2(OH)2CO3+2H2SO4═2CuSO4+CO2↑+3______。
(2)该反应中生成气体的总质量是________g。
(3)200g稀硫酸中溶质硫酸的质量是多少?(写出计算过程)
(4)求孔雀石中碱式碳酸铜的质量分数?(写出计算过程)A.
倾倒液体
B.
称量固体
C.
闻气体气味
D.
加热液体
A.原子序数是28
B.属于金属元素
C.元素符号是Ni
D.一个原子的实际质量是58.69g
选项
A
B
C
D
实验设计
实验目的
探究空气中氧气的体积含量
探究质量守恒定律
比较小木条和小煤块的着火点
探究二氧化碳能跟水反应
选项
实验目的
操作方法
A
除去氧化钙中少量的碳酸钙
高温煅烧
B
区别氧气和二氧化碳
分别通入紫色石蕊溶液
C
区别铜粉和木炭粉
分别加水溶解
D
除去氧化铜中的炭粉
在空气中灼烧
A.两种金属的活动性:M>N
B.两种金属生成氢气的质量:M=N
C.两种金属消耗稀硫酸的质量:M=N
D.充分反应后,得到溶液的质量:M=N
金属种类
不锈钢片
铝片
铜片
腐蚀速度(mg/h)
0.001
0.010
0.404
装置
反应前的质量/g
反应后的质量/g
D
74.7
80.1
E和F
80.3
96.8
次数
加稀硫酸前
1
2
3
4
加入稀硫酸的质量(g)
0
50
50
50
50
烧杯内物质的总质量(g)
30
77.8
125.6
174.5
224.5
24,2024年重庆市巴蜀中学中考三诊化学试卷: 这是一份24,2024年重庆市巴蜀中学中考三诊化学试卷,共8页。
重庆市鲁能巴蜀中学校2024届九年级下学期开学考试化学试卷(含答案): 这是一份重庆市鲁能巴蜀中学校2024届九年级下学期开学考试化学试卷(含答案),共22页。试卷主要包含了单选题,填空题,实验题,计算题等内容,欢迎下载使用。
83,重庆市鲁能巴蜀中学2023-2024学年九年级下学期开学考试化学试题: 这是一份83,重庆市鲁能巴蜀中学2023-2024学年九年级下学期开学考试化学试题,共19页。试卷主要包含了填空题,实验题,计算题等内容,欢迎下载使用。












