

所属成套资源:新鲁科版化学必修第一册学案全套
- 2021_2022年新教材高中化学第三章物质的性质与转化第3节第2课时氨的转化与生成学案鲁科版必修第一册 学案 1 次下载
- 2021_2022年新教材高中化学第三章物质的性质与转化第2节第1课时自然界中的硫二氧化硫学案鲁科版必修第一册 学案 1 次下载
- 2021_2022年新教材高中化学第三章物质的性质与转化第3节第3课时硝酸的性质人类活动对氮循环和环境的影响学案鲁科版必修第一册 学案 1 次下载
- 2021_2022年新教材高中化学第三章物质的性质与转化第1节第2课时铁及其化合物之间的转化关系学案鲁科版必修第一册 学案 1 次下载
- 2021_2022年新教材高中化学第三章物质的性质与转化第2节第2课时硫酸酸雨及其防治学案鲁科版必修第一册 学案 1 次下载
高中鲁科版 (2019)第3节 氮的循环第1课时学案
展开
这是一份高中鲁科版 (2019)第3节 氮的循环第1课时学案,共7页。
1.通过自然界中的氮循环,了解氮循环的基本过程,能列举自然固氮与人工固氮的过程,知道人工固氮对社会发展的重要意义,培养科学态度与社会责任的化学学科核心素养。
2.认识氮循环过程中重要的含有氮元素的物质,能够对含有氮元素的物质进行分类,形成宏观辨识与微观探析的化学学科核心素养。
3.建立从物质类别、元素价态角度研究物质性质和实现含有氮元素的物质之间转化的思路和方法,培养科学探究与创新意识的化学学科核心素养。
eq \a\vs4\al(自然界中的氮循环 氮气)
1.自然界中的氮循环
(1)氮元素的存在
在自然界中的存在形式有游离态和化合态。
(2)自然界中氮的循环
(3)人类活动对自然界中的氮循环的影响
①氮气eq \(――――→,\s\up7(化学方法))eq \a\vs4\al(氨)―→氮肥、硝酸等含氮化合物;
②eq \x(\a\al(森林、农作物、,化石燃料))eq \(――→,\s\up7(燃烧))氮氧化物参与氮的循环。
2.氮的固定
(1)含义:将空气中游离态的氮转化为含氮化合物的过程叫作氮的固定。
(2)分类
eq \a\vs4\al(氮的,固定)eq \b\lc\{\rc\ (\a\vs4\al\c1(\a\vs4\al(自然,固氮)\b\lc\{\rc\ (\a\vs4\al\c1(高能固氮N2+O2\(=====,\s\up7(放电))2NO,生物固氮豆科植物的根瘤菌固氮)),\a\vs4\al(人工,固氮)\b\lc\{\rc\ (\a\vs4\al\c1(合成氨\b\lc\(\rc\)(\a\vs4\al\c1(N2+3H2\(,\s\up7(高温、高压),\s\d5(催化剂))2NH3)),仿生固氮))))
3.氮气
(1)物理性质
(2)化学性质
①稳定性
通常状况下,氮气的化学性质不活泼,它很难与其他物质发生反应。
②N2与O2的反应(表现出还原性)
闪电时或汽车引擎中发生的反应为N2+O2eq \(=====,\s\up7(放电))2NO。
③N2与H2的反应(表现出氧化性)
化学方程式为N2+3H2eq \(,\s\up7(高温、高压),\s\d5(催化剂))2NH3。
④N2与Mg的反应(表现出氧化性)
化学方程式为N2+3Mgeq \(=====,\s\up7(点燃))Mg3N2。
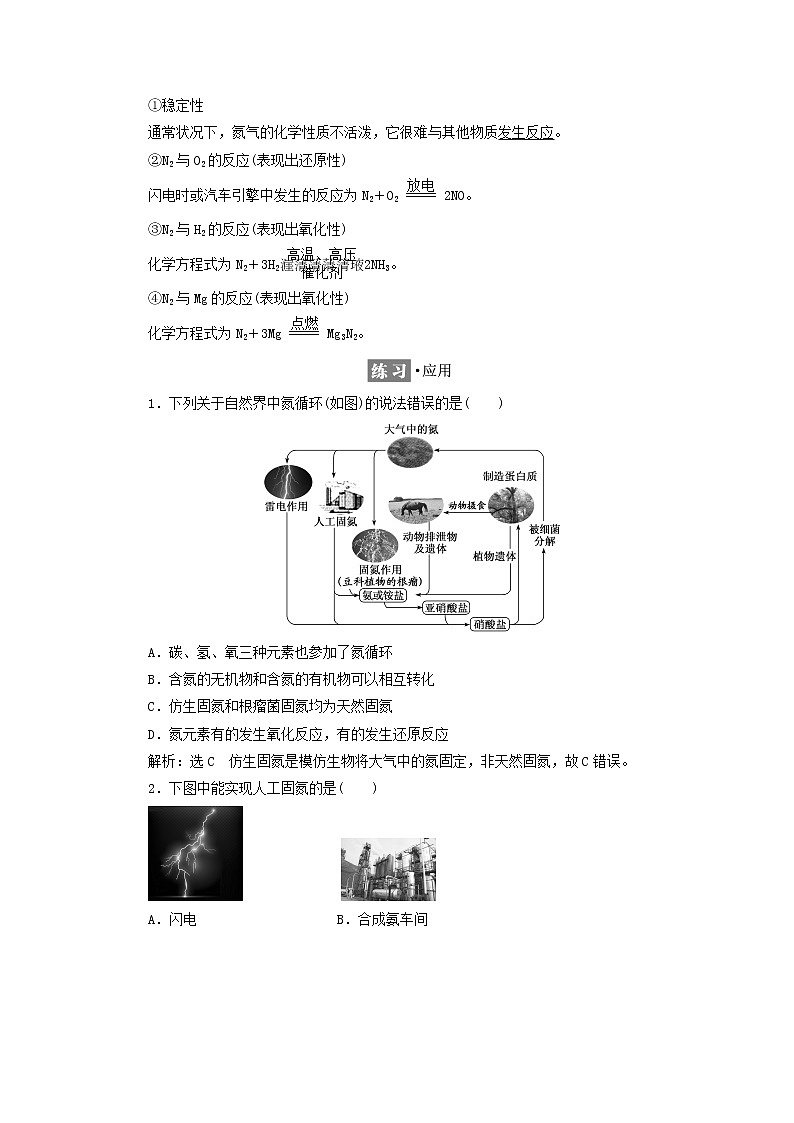
1.下列关于自然界中氮循环(如图)的说法错误的是( )
A.碳、氢、氧三种元素也参加了氮循环
B.含氮的无机物和含氮的有机物可以相互转化
C.仿生固氮和根瘤菌固氮均为天然固氮
D.氮元素有的发生氧化反应,有的发生还原反应
解析:选C 仿生固氮是模仿生物将大气中的氮固定,非天然固氮,故C错误。
2.下图中能实现人工固氮的是( )
A.闪电 B.合成氨车间
C.豆科植物根瘤 D.绿色植物光合作用
解析:选B 闪电时,氮气和氧气反应生成NO,属于自然固氮,A错误;合成氨车间N2与H2在一定条件下反应生成NH3,属于人工固氮,B正确;豆科植物的根瘤菌将空气中的氮气通过生物化学过程转化为含氮化合物,属于生物固氮,C错误;光合作用是将二氧化碳和水转化为有机物和氧气,不属于固氮,D错误。
3.下列关于N2的说法中错误的是( )
A.通常情况下,N2的化学性质很稳定,所以N2可在电焊时做保护气
B.N2+O2高温,2NO,该反应是汽车尾气造成污染的主要原因之一
C.N2在空气中约占空气总质量的eq \f(4,5)
D.在反应3Mg+N2点燃,Mg3N2中,N2做氧化剂
解析:选C N2在空气中约占空气总体积的eq \f(4,5),C项错误。
eq \a\vs4\al(氮的氧化物)
1.NO和NO2性质的比较
[名师点拨]
NO易与O2反应,难溶于水,不与水反应,因此收集NO用排水法,不能用排空气法。NO2易与水反应,很难被O2氧化,因此收集NO2用向上排空气法,不能用排水法。
2.氮的氧化物溶于水的计算
(1)计算依据
3NO2+H2O===2HNO3+NO①
2NO+O2===2NO2②
①×2+②⇒4NO2+O2+2H2O===4HNO3③
①×2+②×3⇒4NO+3O2+2H2O===4HNO3④
(2)氮的氧化物与氧气混合后溶于水的情况分析
①NO2和O2的混合气体溶于水(足量)时,情况分析见下表:
②NO和O2同时通入水(足量)中时,情况分析见下表:
③判断有关NO、NO2、O2的混合气体与足量H2O反应后剩余气体时,因NO2能与H2O反应,NO能与O2反应,所以剩余的气体只可能为NO、O2中的一种,绝对不会剩余NO2。
[名师点拨]
氮的氧化物与O2、H2O反应的计算方法
1.电子守恒法
当NOx转化为硝酸时要失去电子,如果是NOx与O2混合,则反应中O2得到的电子数与NOx失去的电子数相等。
2.原子守恒法
4NO2+O2和4NO+3O2从组成上均相当于2N2O5的组成,4NO2+O2+2H2O===4HNO3、4NO+3O2+2H2O===4HNO3都与N2O5+H2O===2HNO3等效。当NO、NO2、O2的混合气体通入水中时利用混合气体中N、O原子个数比进行分析判断:
N(N)∶N(O)eq \b\lc\{\rc\ (\a\vs4\al\c1(<2∶5 剩余O2,=2∶5 恰好完全反应,>2∶5 剩余NO))
1.将一支盛满NO2气体的试管倒置在水槽中,最终试管内液面的变化是( )
解析:选A 由反应3NO2+H2O===2HNO3+NO可知,反应后V(NO)是反应前V(NO2)的eq \f(1,3),则液面上升到试管的eq \f(2,3)处。
2.下列对NO、NO2的描述,正确的是( )
A.NO是红棕色气体,易溶于水,是酸性氧化物
B.NO2可用排水法收集,且可由N2和O2化合而得到
C.NO、NO2在一定条件下可相互转化,且二者都是大气污染物
D.NO密度比空气大,可用排空气法收集
解析:选C NO是无色难溶于水的气体,不与碱反应,不是酸性氧化物,A项错误;NO2能与水反应:3NO2+H2O===2HNO3+NO,N2和O2反应生成NO,B项错误;NO和O2发生反应:2NO+O2===2NO2,NO2与H2O反应生成NO,NO、NO2都是大气污染物,C项正确;NO易与O2反应,不能用排空气法收集,D项错误。
3.将10 mL NO和NO2的混合气体通入装满水倒立在水槽中的量筒内,一段时间后,最后剩余4 mL气体,原混合气体中含NO的体积为( )
A.1 mL B.3 mL
C.5 mLD.7 mL
解析:选A 若NO2的体积为x,则NO的体积为(10 mL-x),NO2气体与水反应的化学方程式为3NO2+H2O===2HNO3+NO,由此可知,eq \f(1,3)x+(10 mL-x)=4 mL,解得x=9 mL,则原混合气体中含NO的体积为10 mL-x=1 mL。
[分级训练·课课过关]
1.下列说法不正确的是( )
A.豆科植物通过根瘤菌吸收空气中的氮是化学变化
B.汽车尾气中的氮氧化物是由游离态氮转化来的
C.化石燃料燃烧通常不释放出氮氧化物
D.植物秸秆燃烧时产生氮氧化物,参与了氮的循环
解析:选C 氮的固定是将游离态的氮转变成化合态的氮,是化学变化;汽车尾气中的氮氧化物是由氮气和氧气反应生成的;化石燃料中含有氮元素,燃烧时会释放出氮氧化物;植物秸秆燃烧时产生氮氧化物,参与了氮的循环。
2.实验室收集NO、NO2两种气体,下列收集方法正确的是( )
A.均可用排水法
B.均可用向上排空气法
C.NO用向上排空气法,NO2用排水法
D.NO用排水法,NO2用向上排空气法
解析:选D NO2气体能与水反应生成硝酸和NO,不能用排水法收集,A错误;NO与O2反应生成NO2,所以NO不能用排空气法收集,B错误;根据以上分析,C错误;NO难溶于水,因此可以用排水法收集;NO2与空气不反应,其密度比空气密度大,所以可用向上排空气法收集,D正确。
3.NO对于心脑血管系统功能的改善具有重要作用。下列关于NO的描述不正确的是( )
A.难溶于水
B.可由氮气和氧气在放电条件下反应生成
C.常温下能与氧气化合
D.红棕色气体
解析:选D NO为无色难溶于水的气体,D项错误。
4.如图将充满二氧化氮的试管倒扣在水槽中,下列叙述错误的是( )
A.试管内液面上升
B.试管内气体颜色逐渐变浅,直至消失
C.堵住管口将试管取出,管口向上,观察到试管口有红棕色出现
D.取少量试管内液体,滴加石蕊试液后褪色
解析:选D 二氧化氮溶于水后,发生如下反应:3NO2+H2O===2HNO3+NO,NO2气体为红棕色,NO气体无色。从反应的化学方程式可以看出,3体积的NO2与水反应后,只生成1体积的NO,随着反应的进行,试管内气压会减小,所以试管内液面上升,A正确;试管内气体由NO2转化为NO,所以气体的颜色逐渐变浅,直至消失,B正确;试管内的NO与空气接触,生成NO2,试管口有红棕色出现,C正确;反应后,试管内液体为稀硝酸,滴加石蕊试液,溶液只变红不褪色,D错误。
5.目前,汽车尾气已成为许多大城市空气的主要污染源之一。汽车尾气中含有CO、NO等多种污染物。
(1)汽车燃料中一般不含氮,尾气中所含的NO产生的原因是________________________________________________________________________,
化学方程式为____________________________________________________。
(2)治理汽车尾气中NO和CO的一种方法是在汽车的排气管上装上一个催化转化装置,使NO和CO反应,生成CO2和N2,反应的化学方程式为________________________________________________________________________。
(3)下列措施中,能有效减少或控制汽车尾气污染且可行的是________(填标号)。
①制定严格的尾气排放标准,并严格执行。
②开发清洁能源,如氢能汽车、太阳能汽车等。
③市民出行戴防毒面具。
④市民大量移居城市郊区。
解析:(1)空气中的N2和O2在电火花作用下或内燃机燃烧产生的高温条件下反应生成NO,其化学方程式为N2+O2eq \(========,\s\up7(放电或高温),\s\d5( ))2NO。
(2)NO和CO反应生成CO2和N2,其化学方程式为2NO+2COeq \(=====,\s\up7(催化剂))2CO2+N2。
(3)①有利于减少污染;②有利于减少污染;③不现实,是污染后再防护的做法,不可取;④不现实,大量移居成本较高,不可取。
答案:(1)空气中的N2和O2在电火花作用下或内燃机燃烧产生的高温条件下反应产生NO N2+O2eq \(========,\s\up7(放电或高温),\s\d5( ))2NO (2)2NO+2COeq \(=====,\s\up7(催化剂))N2+2CO2
(3)①②
颜色
状态
气味
在水中的溶解性
eq \a\vs4\al(无)色
eq \a\vs4\al(气)体
无味
难溶
NO
NO2
物理性质
无色、难溶于水的气体
红棕色、有刺激性气味、易溶于水的气体
化学性质
与水反应
不反应
3NO2+H2O===2HNO3+NO
(工业上利用这一原理制取HNO3)
与O2反应
2NO+O2===2NO2
不反应
与碱反应
不反应
2NO2+2NaOH===NaNO3+NaNO2+H2O
氧化性
弱氧化性:6NO+4NH3eq \(=====,\s\up7(催化剂))5N2+6H2O;
2NO+2COeq \(=====,\s\up7(催化剂))N2+2CO2
强氧化性:NO2+SO2===NO+SO3;可使湿润的淀粉KI试纸变蓝
毒性
有毒,结合血红蛋白的能力比CO还强
有毒
气体比例
剩余气体情况
V(NO2)∶V(O2)=4∶1时
恰好反应,无气体剩余
V(NO2)∶V(O2)<4∶1时
剩余氧气
V(NO2)∶V(O2)>4∶1时
NO2过量,剩余气体为NO,且其体积为过量NO2体积的eq \f(1,3)
气体比例
剩余气体情况
V(NO)∶V(O2)=4∶3时
恰好反应,无气体剩余
V(NO)∶V(O2)<4∶3时
剩余氧气
V(NO)∶V(O2)>4∶3时
剩余NO
相关学案
这是一份高中化学鲁科版 (2019)必修 第一册第3节 氮的循环第1课时导学案,共15页。
这是一份化学必修 第一册第3章 物质的性质与转化第3节 氮的循环学案,共13页。学案主要包含了自然界中的氮循环,氮的固定,氮氧化物等内容,欢迎下载使用。
这是一份高中化学鲁科版 (2019)必修 第一册第1节 铁的多样性第2课时学案设计,共8页。










