





2022中考一轮单元复习 05.第五单元 化学方程式课件PPT
展开第五单元 化学方程式
1. (2015河南19题2分)为验证质量守恒定律,某同学设计了如图实验。该实验能否达到实验目的?请说明理由。
质量守恒定律的验证(10年4考)
答:不能。因为稀盐酸和硫酸钠溶液不能发生化学反应(或不能发生复分解反应)。
质量守恒定律的应用之定性推断(10年8考)
2. (2017河南11题1分)硝酸铜受热分解会产生一种污染空气的有毒气体,该气体可能是( )A. N2 B. NO2 C. NH3 D. SO23. (2018河南备用卷11题1分)氢化钙与水反应的化学方程式为CaH2+2H2O=== X+2H2↑。下列说法不正确的是( )A. 氢化钙需要密封保存 B. 氢化钙是一种燃料提供剂C. X的化学式为Ca(OH)2 D. 氢化钙可用于干燥多种气体
【链接】更多试题详见微专题1
质量守恒定律的应用之定量计算(10年7考)
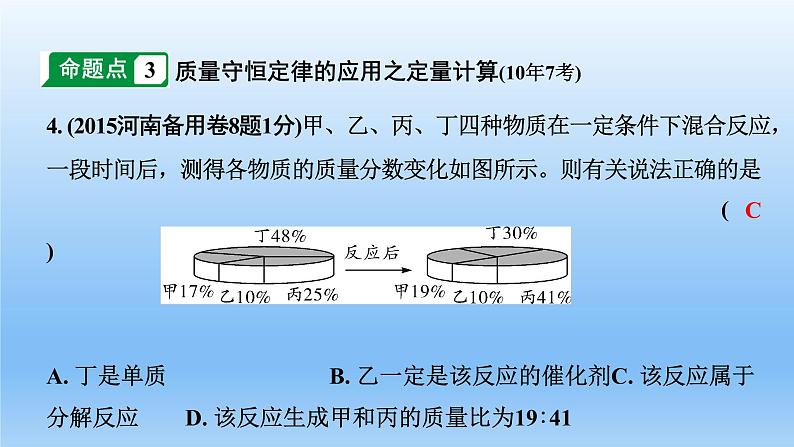
4. (2015河南备用卷8题1分)甲、乙、丙、丁四种物质在一定条件下混合反应,一段时间后,测得各物质的质量分数变化如图所示。则有关说法正确的是 ( )A. 丁是单质 B. 乙一定是该反应的催化剂C. 该反应属于分解反应 D. 该反应生成甲和丙的质量比为19∶41
5. (2016河南17题1分)2015年诺贝尔奖获得者屠呦呦发现的青蒿素是一种抗疟疾药,若14.1 g青蒿素燃烧生成33.0 g CO2和9.9 g H2O,则青蒿素中氧的质量与其燃烧消耗氧气的质量之比为________________。【链接】更多试题详见微专题2
5∶36(或4∶28.8)
微观反应示意图(10年10考)
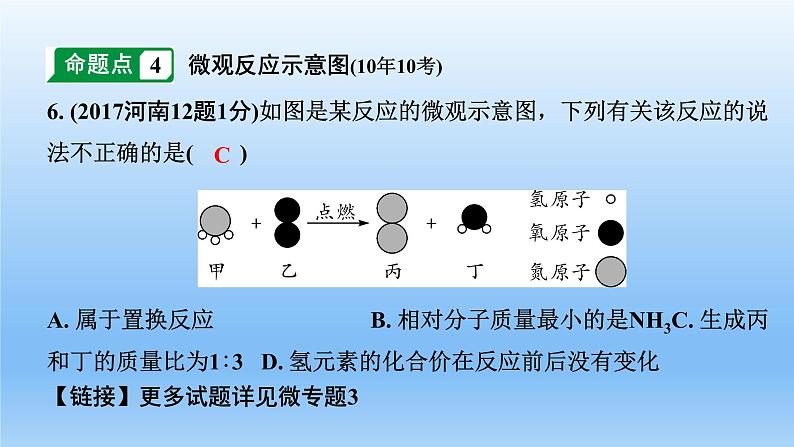
6. (2017河南12题1分)如图是某反应的微观示意图,下列有关该反应的说法不正确的是( )A. 属于置换反应 B. 相对分子质量最小的是NH3C. 生成丙和丁的质量比为1∶3 D. 氢元素的化合价在反应前后没有变化
【链接】更多试题详见微专题3
基本反应类型的判断(10年9考)
9. (2021河南6题1分)古籍记载“曾青得铁则化为铜”,指可溶性的铜的化合物与铁反应得到铜,该反应为( )A. 化合反应 B. 分解反应C. 置换反应 D. 复分解反应10. (2015河南9题1分)工业制镁的方法为:将含碳酸钙的贝壳制成石灰乳;在海水中加入石灰乳,过滤;在氢氧化镁中加入盐酸,结晶;电解熔融氯化镁。该方法中的化学反应不包括( )A. 化合反应 B. 置换反应C. 分解反应 D. 复分解反应
11. (2013河南8题1分)有化合价升降的反应是氧化还原反应。下列一定不是氧化还原反应的是( )A. 化合反应 B. 分解反应C. 置换反应 D. 复分解反应
12. (2018河南备用卷13题1分)有元素化合价升降的反应属于氧化还原反应。下列反应中属于氧化还原反应的是( )A. ①② B. ①③ C. ②④ D. ④⑤
化学方程式的书写(10年10考)
14. (2019河南备用卷17题1分)氢化镁(MgH2)可用来储氢,氢化镁与水反应生成一种单质和一种碱,该反应的化学方程式为________________________________。15. [2014河南备用卷17(2)题1分]液氨有望成为新一代绿色能源。氨气在纯氧中燃烧生成空气中含量最多的气体和一种氧化物,且释放大量热量。该反应的化学方程式_____________________________。
MgH2+2H2O === Mg(OH)2+2H2↑
16. (2018河南20题1分)碱式碳酸铜[Cu2(OH)2CO3]受热分解生成氧化铜、水和二氧化碳,反应的化学方程式为____________________________________。17. 电解食盐水可得到烧碱、氯气(Cl2)和一种可燃气体,反应的化学方程式为________________________________________。[2017河南20题、2013河南15(3)题]
18. [2015河南23(2)题2分]钠与水反应生成氢氧化钠和氢气,化学方程式为____________________________;小苏打受热分解成碳酸钠、二氧化碳和水,化学方程式为______________________________________。
2Na+2H2O === 2NaOH+H2↑
19. (2016河南备用卷17题2分)已知:Cl2+2NaOH === NaCl+NaClO+H2O。氯气和熟石灰反应可以制得漂白粉,该反应的化学方程式为__________________________________________;Ca(ClO)2在空气中会转化为CaCO3和HClO,该反应的化学方程式为_________________________________________。
2Cl2+2Ca(OH)2 === CaCl2+Ca(ClO)2+2H2O
Ca(ClO)2+H2O+CO2=== CaCO3↓+2HClO
20. (2014河南20题3分)用化学方程式表示下列反应原理。(1)用电解水的方法制取氢气。
(2)用磁铁矿石(含Fe3O4)炼铁。
(3)实验室制取氧气。(写出一个即可)
化学方程式的计算(10年10考)
考向1 直接给出代入化学方程式中纯净物的质量(10年4考)21. [2021河南25(5)题3分]某温室大棚需用到440 L CO2(按标准状况计算,CO2密度为1.964 g/L),用足量盐酸与含CaCO3 80%的石灰石反应制取,需要这种石灰石的质量是多少?
22. [2019河南25(7)题3分]已知:2Na2O2+2CO2===2Na2CO3+O2,某潜水艇上有100人,如果每人每分钟消耗氧气为0.001 kg,假如所需要的氧气全部由Na2O2与CO2反应来提供,则该潜水艇一天所需要Na2O2的质量是多少?
考向2 根据反应前后质量差计算代入化学方程式中纯净物的质量(10年3考)23. [2018河南25(4)题3分]为测定某石灰石样品中碳酸钙的质量分数,称取10 g石灰石(杂质不参加反应)放入烧杯中,加入100 g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7 g(气体的溶解忽略不计)。请计算该样品中碳酸钙的质量分数。
考向3 根据质量分数计算代入化学方程式中纯净物的质量(10年3考)24. [2020河南备用卷25(4)题3分]某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000 t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?
解:设该厂理论上可日产含铁96%的生铁的质量为xFe2O3+3CO 2Fe+3CO2 160 1126000 t×80% x×96%x=3500 t答:理论上可日产含铁96%的生铁的质量为3500 t。
26. [2014河南备用卷23(4)题3分]取已变质的氢氧化钠溶液100 g,向其中加入溶质质量分数为7.3%的稀盐酸100 g,恰好完全反应得到中性溶液。试计算蒸干该溶液可得到固体的质量。
27. [新科技](2021安徽)科学家设计了“人造树叶”模拟光合作用,其装置和反应的微观示意图如下。下列说法错误的是( )A. 反应最终生成两种分子 B. 该过程实现了能量的转化C. 反应前后催化剂的化学性质不变 D. 该设计为缓解温室效应提供了新途径
28. [真实教学情境](2021山西改编)在一次作业批改中,王老师发现4位同学在同一题中出现了不同的错误,为帮大家理清思路,老师将错误的解题过程写在黑板上,请同学们仔细观察,发现问题,纠正错误。(1)仔细观察:你发现解题过程中的错误有____处。(2)纠正错误:老师点拨后,请写出正确的解题过程。
内容:_____________的各物质的_________等于反应后_____的各物质的 _________,适用范围:只适用于所有的_____变化;只适用于_____守恒,不包括体积、分子数 目等的守恒
微观:原子的_____、_____、_____不变。宏观:物质的_________、_________、元素质量不变。
微观:___________一定改变。宏观:___________一定改变。
_________可能改变 。 ___________可能改变。
a. 推断物质的元素组成——依据化学反应前后元素_____不变b. 确定化学反应中某物质的化学式——依据化学反应前后原子种类、数目不变。c. 确定反应中的化学计量数——依据化学反应前后各原子_____不变。d. 解释反应前后物质的质量变化及用质量差确定反应中某一物质的质量—— 依据化学反应前后, 物质的总质量不变。
验证(10年4考)(详见实验突破栏目)
二、基本反应类型(10年4考)
概念:用化学式表示化学反应的式子。
“质”:表示化学反应的_______、_______和_________。“量”:
宏观:表示反应物、生成物之间的_______。微观:表示反应物、生成物之间的微粒_______。
原则:一是以_________为基础;二是遵守_____________,即等号两边各原 子的______和_____必须相同书写完成后检查:一查化学式是否正确,二查是否配平,三查生成物状态是 否标注,标注是否恰当,, 四查反应条件是否标明
a.反应前无气体,反应后的气体生成物需标“↑”b.溶液中的反应如果反应前无固体,反应后的固体需标“↓”
计算:依据质量守恒定律
下列说法正确的是_____。①化学反应前后分子的总数目一定相等②化学反应前后原子种类不变,因此元素种类也不变③根据质量守恒定律可知100 g水受热蒸发变为水蒸气后,质量仍为100 g④某纯净物在氧气中燃烧生成二氧化碳和水,则该物质中一定含有碳、氢、氧三种元素⑤镁燃烧后生成氧化镁的质量大于镁的质量,所以不符合质量守恒定律⑥置换反应中一定有元素化合价发生变化,复分解反应中各元素化合价一定不变
质量守恒定律的验证(10年4考)
1. 药品选择:药品之间必须能发生化学反应。2. 方案设计
温馨提示:若因软件问题视频无法打开,请在实验视频文件夹打开原视频
3. 实验原理实验A:______________________(用化学方程式表示,下同)。实验B:__________________________。实验C:_____________________________________。
Fe+CuSO4=== FeSO4+Cu
Na2CO3+2HCl=== 2NaCl+H2O+CO2↑
4. 实验现象实验A:红磷燃烧_____________,反应前后天平保持平衡。实验B:铁钉表面覆盖一层____色固体,溶液由____色变为_____色,反应前后天平保持平衡。实验C:产生大量气泡,天平指针向右偏转。5. 实验结论(根据实验A、B)参加反应的各物质的质量总和等于生成物的质量总和。
6. 实验反思(针对实验A中左盘装置)(1)锥形瓶底要铺一层细沙,目的是_________________________。(2)气球的作用:________________________、调节压强。
7. 装置评价与改进实验C中左盘装置由于碳酸钠与稀盐酸反应生成的_____逸散到空气中,导致天平不平衡,所以在用有气体生成或参与的反应来验证质量守恒定律时,应将实验在_________中进行。
防止锥形瓶受热不均而炸裂
防止气体逸出、起密封作用
例 某兴趣小组设计如下实验探究质量守恒定律(1)如图1,反应前,托盘天平的指针指向刻度盘的中间,两种物质反应后,托盘天平的指针向右偏转,原因是___________________________________________________________________,该反应______(填“遵循”或“不遵循”)质量守恒定律。
稀盐酸和碳酸钙反应生成的二氧化碳气体逸散到空气中,烧杯内质量减少
(2)如图2,实验中玻璃管的作用是_________,实验时,气球变化的情况是__________________________。
先膨胀,后变得比之前更瘪
(3)如图3,某同学将装有硫酸铜溶液的锥形瓶和铁钉放在天平左盘,调节天平平衡。然后取下锥形瓶把铁钉放入锥形瓶中,一段时间后,再把锥形瓶放回天平左盘,最后天平_____(填“平衡”或“不平衡”)。反应后锥形瓶内溶液的质量_____(填“增大”“减小”或“不变”)。
(4)请判断图4装置能否用于验证质量守恒定律,并说明原因。
答:不能,因为稀硫酸和氯化钠溶液不发生化学反应。
2024长沙中考化学一轮复习 第五单元 化学方程式(课件): 这是一份2024长沙中考化学一轮复习 第五单元 化学方程式(课件),共57页。PPT课件主要包含了质量总和,原子的种类,原子的数目,原子的质量,六个“不变”,两个“一定改变”,两个“可能改变”,元素种类,物质的质量总和不变,密闭容器等内容,欢迎下载使用。
中考化学一轮单元总复习课件 第五单元 化学方程式 (含答案): 这是一份中考化学一轮单元总复习课件 第五单元 化学方程式 (含答案),共43页。PPT课件主要包含了核心知识·建构脉络图,主干回顾·厚积知识力,参加化学反应,质量总和,化学式,反应物,生成物,反应条件,碳和氧气,二氧化碳等内容,欢迎下载使用。
2023年中考化学一轮复习:第五单元化学方程式课件PPT: 这是一份2023年中考化学一轮复习:第五单元化学方程式课件PPT,共24页。












