





- 1.1 物质的分类及转化(第一课时)课件+教案+练习 课件 91 次下载
- 1.1 物质的分类及转化(第二课时)课件+教案+练习 课件 84 次下载
- 1.2离子反应(第二课时)课件+教案+练习 课件 89 次下载
- 1.2离子反应(第三课时)课件+教案+练习 课件 86 次下载
- 1.3氧化还原反应(第一课时)课件+教案+练习 课件 84 次下载
人教版 (2019)必修 第一册第二节 离子反应获奖ppt课件
展开一、新课导入二、研究NaCl溶液导电的原因三、电解质四、电离
因为手上有水时,人双手间电阻由干燥时的1000-5000欧降至200-800欧。 在电压不变的情况下,通过人体的电流会增大。大到一定程度就有危险了。
物体能导电是因为有电流
由带电荷的粒子按一定方向自由移动而形成的。
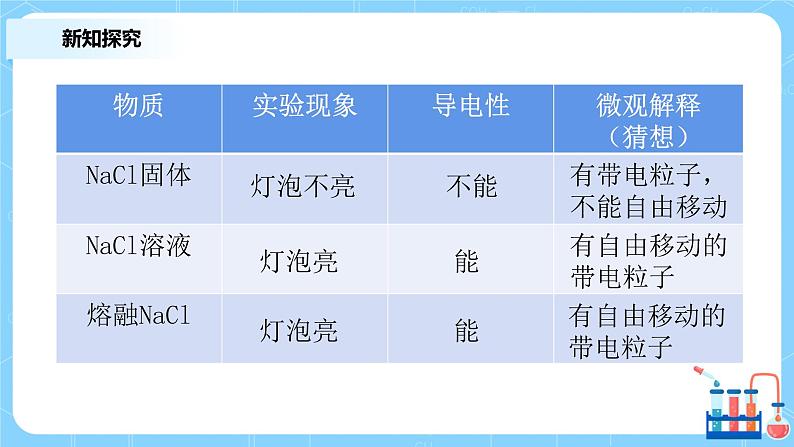
活动1 研究NaCl(aq)导电的原因
猜想 :NaCl(aq)中有自由移动的带电粒子
有带电粒子,不能自由移动
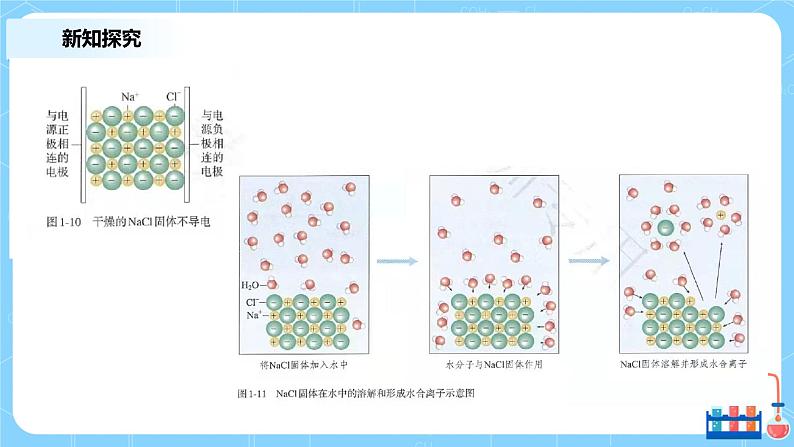
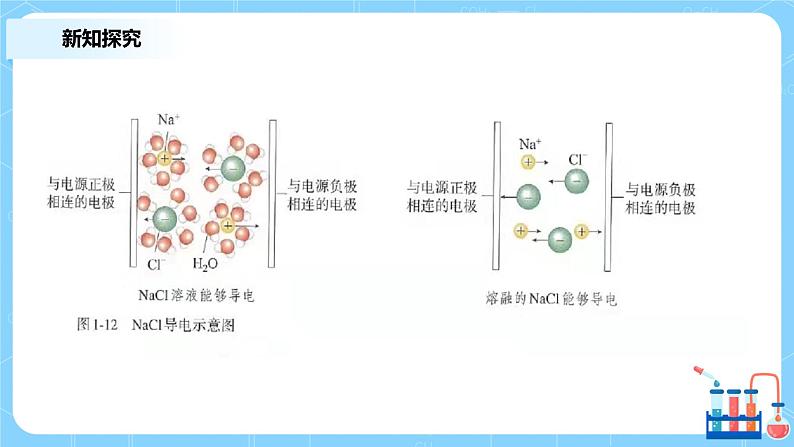
在水溶液里或者在熔融状态下能够导电的化合物叫做电解质。
活动2 电解质、非电解质
请判断对错:(1)不是电解质的物质,就一定是非电解质。( )(2)CO2、SO2、NH3的水溶液能够导电,它们是电解质( )(3)能导电的物质不一定是电解质。( )(4)不导电的物质不一定不是电解质。( )(5)CaO等金属氧化物是电解质是因为它们在熔融状态下导 电,它们在水溶液中与水反应生成了其他物质。( )
它们溶于水后能电离出离子的物质是H2CO3、H2SO3、NH3·H2O,而这些物质才是电解质。
活动3 强电解质和弱电解质
活动4 影响电解质溶液导电性强弱的因素
(1)影响因素:自由移动离子的浓度越大,所带电荷越多, 溶液导电性越强。(2)电解质溶液导电性与强弱电解质的关系: ①相同浓度的强、弱电解质溶液,强电解质溶液导电性强。 ②不同浓度时,强电解质溶液导电性不一定强。
活动5 电离概念、强、弱电解质的电离
活动6 从电离角度理解酸、碱、盐
请书写以下三组的电离方程式:
总 结一、判断物质是否是电解质二、强电解质和弱电解质三、电解:宏观 → 微观 → 符号(电离方程式)
1、2、从电离角度分析NaHSO4的物质属性。
人教版 (2019)必修 第一册第二节 离子反应教学课件ppt: 这是一份人教版 (2019)必修 第一册第二节 离子反应教学课件ppt,共1页。
高中化学人教版 (2019)必修 第一册第二节 离子反应精品ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二节 离子反应精品ppt课件,共25页。PPT课件主要包含了物质及其变化,学习目标,离子方程式,写出正确的化学方程式,Ca2+,Cl-,Na+,CO32-,CaCO3↓,检查二守恒等内容,欢迎下载使用。
化学必修 第一册第二节 离子反应精品课件ppt: 这是一份化学必修 第一册第二节 离子反应精品课件ppt,文件包含12《离子反应》第三课时课件pptx、12《离子反应》第三课时练习docx、常见阳离子和阴离子的检验知识点docx、12《离子反应》第三课时教案docx等4份课件配套教学资源,其中PPT共24页, 欢迎下载使用。














