

2020-2021学年四川省西昌市高二下学期期中检测化学试题含答案
展开
西昌市2020—2021学年度下期期中检测
高 二 化 学
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,试题卷6页,答题卡2页。全卷满分为100分,考试时间90分钟。
答题前考生务必将自己的姓名、准考证号用0.5毫米的黑色签字笔填写在答题卡上,并将条形码粘贴在答题卡的指定位置;选择题使用2B铅笔填涂在答题卡对应题目标号的位置上,其他试题用0.5毫米签字笔书写在答题卡对应题框内,不得超越题框区域。考试结束后将答题卡收回。
可能用到的相对原子质量 H-1 O-16 C-12 Si-28 P-31 Ni-59
第Ⅰ卷(选择题 共48分)
一、选择题(在下列给出的选项中只有一个选项符合题意。有16个小题,每小题3分,共48分)
1.元素性质随着原子序数的递增呈现周期性变化的原因是( )
A.原子半径的周期性变化 B.电负性的周期性变化
C.第一电离能的周期性变化 D.原子核外电子排布的周期性变化
2.电子由3d能级跃迁至4p能级时,可通过光谱仪直接摄取( )
A.电子的运动轨迹图象 B.原子的吸收光谱
C.电子体积大小的图象 D.原子的发射光谱
3.下列无机含氧酸分子中酸性最强的是( )
A.HNO2 B.H2SO3 C.HClO3 D.HClO4
4. 类推的思维方法在化学学习与研究中可能会产生错误的结论,因此类推出的结论需经过实践的检验才能确定其正确与否。下列几种类推结论正确的是( )
A.从CH4、NH、SO为正四面体结构,可推测PH、PO也为正四面体结构
B.H2O常温下为液态,H2S常温下也为液态
C.金刚石中C—C键的键长为154.45 pm,C60中C—C键的键长为140~145 pm,所以C60的熔点高于金刚石
D.CO2与SiO2化学式相似,可推测出CO2与SiO2的结构也相似
5.下列物质呈固态时,一定属于分子晶体的是( )
A.非金属单质 B.非金属氧化物
C.含氧酸 D.金属氧化物
6.下列物质的变化过程中,化学键没有被破坏的是( )
A.碘升华 B.氯化钠受热熔化
C.金属汞汽化 D.氯化氢溶于水
7. 下列分子中不存在键的是 ( )
A. C2H2 B. C2H4 C. CH4 D. C6H6
8. 设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.28 g晶体硅中含有Si—Si键的个数为2NA
B.124 g白磷(P4)晶体中含有P—P键的个数为4NA
C.12 g石墨中含有C—C键的个数为4NA
D.SiO2晶体中每摩尔硅原子可与氧原子形成2NA个共价键(Si—O键)
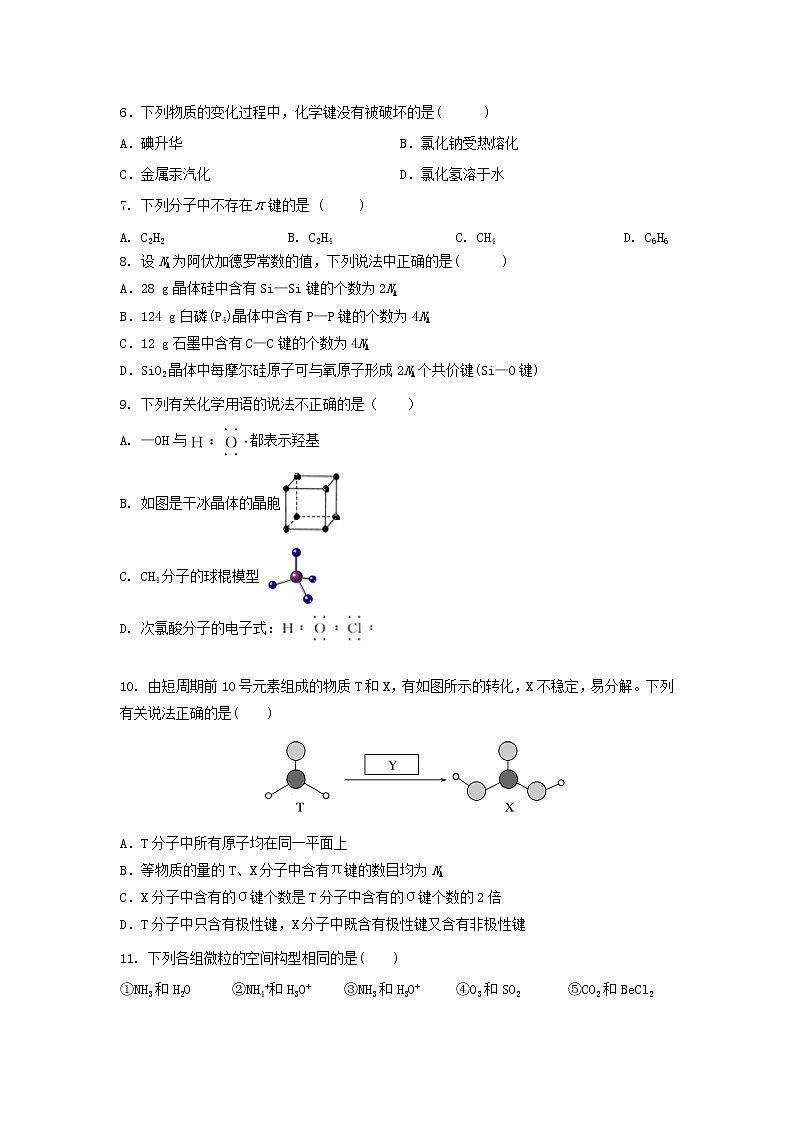
9. 下列有关化学用语的说法不正确的是( )
A. —OH与都表示羟基
B. 如图是干冰晶体的晶胞
C. CH4分子的球棍模型
D. 次氯酸分子的电子式:
- 由短周期前10号元素组成的物质T和X,有如图所示的转化,X不稳定,易分解。下列有关说法正确的是( )
A.T分子中所有原子均在同一平面上
B.等物质的量的T、X分子中含有π键的数目均为NA
C.X分子中含有的σ键个数是T分子中含有的σ键个数的2倍
D.T分子中只含有极性键,X分子中既含有极性键又含有非极性键
11. 下列各组微粒的空间构型相同的是( )
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2
⑥SiO44-和SO42- ⑦BF3和Al2Cl6
A. 全部 B. 除④⑥⑦以外 C. ③④⑤⑥ D. ②⑤⑥
12. 有X、Y、Z、Q、T五种元素,X原子M层上有2个未成对电子且无空轨道;Y原子的价层电子排布式为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )
A. 元素Y和Q可形成化合物Y2Q3
B. T和Z各有一种单质的空间构型为正四面体形
C. 元素X和Z形成的化合物不可能是分子晶体
D. ZQ2是极性键构成的非极性分子
13.中国科学家团队成功合成了五氮阴离子盐(N5)6(H3O)3(NH4)4Cl,五氮阴离子(N5-)是制备全氮类物质N5+N5-的中间体。下列说法正确的是( )
A.键角:NH4+>H3O+ B.电负性:N>O>H
C.N5+N5-属于离子化合物 D.基态Cl-的价电子排布图为
14.下列各项叙述中正确的是( )
A.电子层序数越大,s原子轨道的形状相同,半径越大
B.在同一电子层上运动的电子,其自旋方向肯定不同
C.镁原子由1s22s22p63s2→1s22s22p63p2时,释放能量,由基态转化成激发态
D.杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对
15.下列分子或离子中,VSEPR模型名称与分子的立体构型名称不一致的是( )
A.CO2 B.H2O C.CO D.CCl4
16. Co(Ⅲ)的八面体配合物CoClm·nNH3,若1 mol配合物与AgNO3作用生成1 mol AgCl沉淀,则m、n的值是( )
A.m=1 n=5 B.m=3 n=4
C.m=5 n=1 D.m=4 n=5
第Ⅱ卷(非选择题 共52分)
二、填空题(共52分)
17.(12分)X、Y、Z三种元素的结构信息如表所示。请根据信息回答下列问题:
元素 | 结构信息 |
X | 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2 |
Y | 基态原子的3p轨道上有4个电子 |
Z | 元素Z的原子最外层电子数是其内层的3倍 |
(1)基态X原子中,核外电子占据最高能层的符号是_______,占据该能层电子的电子云轮廓图形状为_______。
(2)元素W与X处于同一周期,其基态原子中未成对电子数是核外电子总数的 ,W的元素符号为_______。
(3)在第三周期中,第一电离能比Y大的主族元素有_______(填元素符号).
(4)YZ3分子中,Y原子的杂化轨道类型是_______,其分子的立体构型为_______。
(5)Z的氢化物(H2Z)的稳定性高于Y的氢化物(H2Y),其原因是
_____________________________________________________________________________。
(6)H2Z在特定条件下得到一个H+形成H3Z+,从结构角度对上述过程分析错误的是_______
A.中心原子的杂化轨道类型发生了改变
B.中心原子的价层电子对数发生了改变
C.微粒的立体结构发生了改变
D.微粒中键角发生了改变
18.(14分)下表为周期表的一部分,其中的编号代表所对应的元素。
请回答下列问题:
(1)表中属于d区的元素是 (填编号)。
(2)元素⑨的基态原子有________种运动状态不相同的电子。
(3)科学研究发现,②、④、⑧三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图所示,则该化合物的化学式为________(用对应的元素符号表示),1个④与________个⑧等距离且最近。
(4)①、②两种元素能形成多种平面形分子,其中有一种相对分子质量最小,有关该分子的说法中正确的是________。
a.该分子属于含有极性键的非极性分子
b.该分子含有4个σ键和1个π键
c.该分子中的②原子采取sp2杂化
(5)某元素的价电子排布式为nsnnpn+1,该元素可与元素①形成含有10个电子的分子X,将过量的X通入盛有硫酸铜溶液的试管里,产生的现象为_____________________________,写出该过程中沉淀溶解的离子方程式_____________________________________________。
(6)第一电离能④_______⑤(填“>”、“<”或“=”),其原因是_____________________________。
19.(13分)许多元素及它们的化合物在科学研究和工业生产中具有许多用途,请回答下列有关问题:
(1)某同学画出基态碳原子的核外电子排布图:,该电子排布图违背了_____________;CH3+、-CH3、CH3-都是重要的有机反应中间体,CH3- 的VSEPR模型为__________。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为__________________________。
(3)基态溴原子的价层电子排布图为________________,用价层电子对互斥理论推断SnBr2分子中Sn—Br的键角__________120°(填“>”、“<”或“=”)。
(4)能与多种金属离子形成配合物,例如,工业冶炼金的原理:。与互为等电子体的分子有________只写一种,中含________键。
(5)类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是_______________。
20.(13分)中国科学技术大学俞书宏教授团队和高敏锐教授课题组通过室温过饱和溶液共沉积法,实现了无定形NiFeMo氧化物纳米材料的宏量制备,该方法简便快捷,反应几分钟即可一次性生产多达515克的产物,制备的无定形NiFeMo氧化物在碱性条件下展示出优异的OER催化活性,明显优于结晶型NiFeMo氧化物。根据所学知识回答下列问题:
(1)区别结晶型NiFeMo氧化物和无定形NiFeMo氧化物最可靠的科学方法为______________,结晶型NiFeMo氧化物能自发呈现多面体外形,这种性质称为晶体的_________。
(2)Mo为第五周期元素与Cr同族,则Mo的价层电子排布式为_______________
(3)配合物Ni(CO)4常温下为液态,易溶于CCl4 ,苯等有机溶剂,是获得高纯度纳米镍的原料,Ni(CO)4是_______________(填“极性”或“非极性”)分子。
(4)下列状态的铁中,电离最外层的一个电子所需能量最大的是 (填编号)。
(5)FeCl3中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的FeCl3的结构式为________,其中Fe的配位数为_________.
(6)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为a pm,列式表示NiO晶体的密度为_______________g/cm3(不必计算出结果,阿伏加德罗常数的值为NA)。
西昌市2020—2021学年度下期期中检测
高二化学期中试题参考答案
一、选择题(包括16个小题,每小题3分,共48分.每小题只有一个选项符合题意.)
1.D 2.B 3.D 4.A 5.C 6.A 7.C 8.A 9.B 10.A 11.C 12.C 13.A 14.A 15.B 16.B
二、填空题(除标注外,其余每空2分,共52分)
17.(12分)
(1) N (1分); 球形 (1分) (2) Mn (3) P、Cl
(4) sp2(1分) ; 平面正三角形(或平面三角形)(1分)
(5) 水分子中O-H的键能大于硫化氢中S-H的键能 (6) A、B
18.(14分)
(1)⑧(1分) (2)29(1分) (3)MgNi3C或Ni3MgC 12 (4)ac (5)先产生蓝色沉淀,后沉淀消失,溶液变成深蓝色
(6) >(1分), Mg的3s电子排布处于全满状态,较稳定(1分) 。
19.(13分)
(1)洪特规则(1分);四面体形(1分);
(2)C>H>Si
(3) (1分) ; <
(4)或CO,或其他合理答案; 8
(5)异硫氰酸分子间存在氢键,而硫氰酸分子间只存在范德华力。
20.(13分)
(1)X-射线衍射实验(1分) 自范性(1分) (2) 4d55s1
(3) 非极性 (4)A
(5)
(或 ) 4(1分)
(6)
四川省凉山州西昌市2023-2024学年高二上学期期末检测化学试题(word含答案): 这是一份四川省凉山州西昌市2023-2024学年高二上学期期末检测化学试题(word含答案),共10页。试卷主要包含了一定条件,水煤气发生变换反应,设为阿伏加德罗常数的值等内容,欢迎下载使用。
四川省凉山州西昌市2023-2024学年高二上学期期末检测化学试题(PDF版含答案): 这是一份四川省凉山州西昌市2023-2024学年高二上学期期末检测化学试题(PDF版含答案),共10页。
四川省凉山州西昌市2023-2024学年高二上学期期中考试化学试题含答案: 这是一份四川省凉山州西昌市2023-2024学年高二上学期期中考试化学试题含答案,共11页。试卷主要包含了3 kJ,1~4,4),溶液中,5倍,其目的是,2%,9%,8%等内容,欢迎下载使用。












