



所属成套资源:高考化学三轮复习专项冲刺
2021届高考化学三轮复习专项冲刺:化学工艺流程综合(第二课时)课件PPT
展开
这是一份2021届高考化学三轮复习专项冲刺:化学工艺流程综合(第二课时)课件PPT,共14页。PPT课件主要包含了考点1,典例呈现,考点2,归纳总结等内容,欢迎下载使用。
【例1】四水合磷酸锌 [Zn3(PO4)2·4H2O,摩尔质量为457 g· ml-1,难溶于水] 是一种性能优良的绿色环保防锈颜料。实验室以锌灰(含ZnO、PbO、CuO、FeO、Fe2O3、SiO2等)为原料制备Zn3(PO4)2·4H2O的流程如下,回答下列问题:
以金属元素为主角的流程
已知:6NH4HCO3+3ZnSO4 ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2↑;ZnCO3·2Zn(OH)2·H2O+2H3PO4 Zn3(PO4)2·4H2O+2H2O+CO2↑。
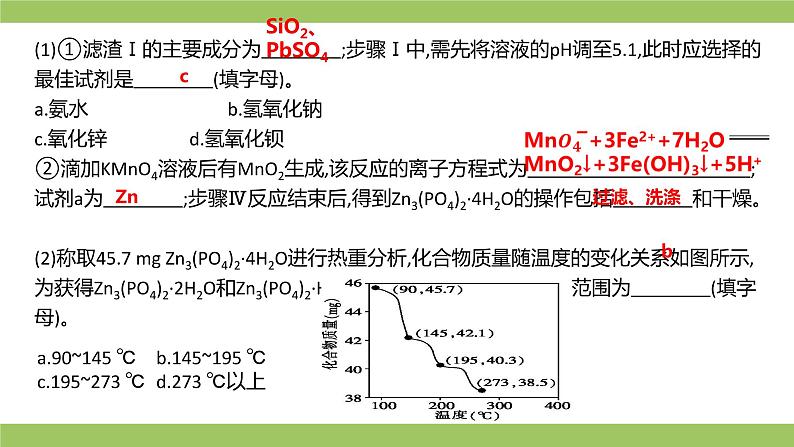
(1)①滤渣Ⅰ的主要成分为 ;步骤Ⅰ中,需先将溶液的pH调至5.1,此时应选择的最佳试剂是 (填字母)。 a.氨水 b.氢氧化钠c.氧化锌 d.氢氧化钡②滴加KMnO4溶液后有MnO2生成,该反应的离子方程式为 ;试剂a为 ;步骤Ⅳ反应结束后,得到Zn3(PO4)2·4H2O的操作包括 和干燥。 (2)称取45.7 mg Zn3(PO4)2·4H2O进行热重分析,化合物质量随温度的变化关系如图所示,为获得Zn3(PO4)2·2H2O和Zn3(PO4)2·H2O的混合产品,烘干时的温度范围为 (填字母)。
a.90~145 ℃b.145~195 ℃c.195~273 ℃d.273 ℃以上
(3)为测定产品中Zn3(PO4)2·4H2O的含量,进行如下实验,已知滴定过程中Zn2+与H2Y2-按1∶1反应。步骤Ⅰ:准确称取0.4570 g产品于烧杯中,加入适量盐酸使其溶解,将溶液转移至100 mL容量瓶,定容。步骤Ⅱ:移取20.00 mL上述溶液于锥形瓶中,加入指示剂,在pH=5~6的缓冲溶液中用0.02000 ml·L-1 Na2H2Y标准溶液滴定至终点,测得Na2H2Y标准溶液的用量为27.60 mL。步骤Ⅱ中移取溶液时所使用的玻璃仪器为 ;产品中Zn3(PO4)2·4H2O的质量分数为 。下列操作中,导致产品中Zn3(PO4)2·4H2O含量测定值偏小的是 (填字母)。 a.步骤Ⅰ中定容时俯视刻度线b.步骤Ⅰ中转移溶液时未洗涤烧杯c.步骤Ⅱ中滴定管未用Na2H2Y标准溶液润洗d.步骤Ⅱ中滴定前滴定管内无气泡,滴定结束后有气泡
移液管(或酸式滴定管)
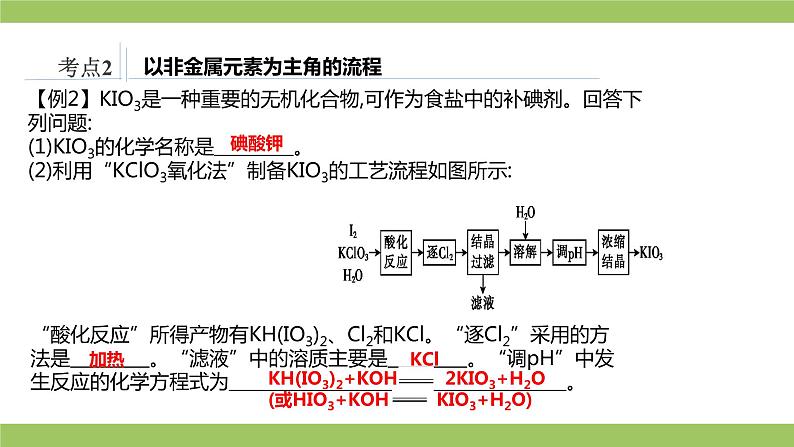
【例2】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:(1)KIO3的化学名称是 。 (2)利用“KClO3氧化法”制备KIO3的工艺流程如图所示:
以非金属元素为主角的流程
“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是 。“滤液”中的溶质主要是 。“调pH”中发生反应的化学方程式为 。
KH(IO3)2+KOH 2KIO3+H2O(或HIO3+KOH KIO3+H2O)
2H2O+2e- 2OH-+H2↑
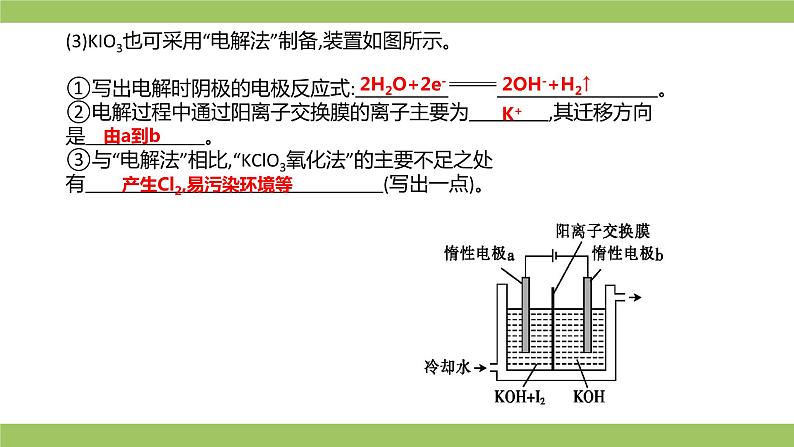
(3)KIO3也可采用“电解法”制备,装置如图所示。 ①写出电解时阴极的电极反应式: 。 ②电解过程中通过阳离子交换膜的离子主要为 ,其迁移方向是 。 ③与“电解法”相比,“KClO3氧化法”的主要不足之处有 (写出一点)。
产生Cl2,易污染环境等
解析▶ (2)将溶解在溶液中的气体排出的方法一般是将溶液加热,原因是气体的溶解度随温度升高而减小。第一步反应得到的产品中氯气在“逐Cl2”时除去,根据图示,碘酸钾在最后得到,所以过滤时KH(IO3)2应该在滤渣中,所以滤液中的溶质主要为KCl。“调pH”的主要目的是将KH(IO3)2转化为KIO3,所以化学方程式为KH(IO3)2+KOH 2KIO3+H2O。(3)①由图示可知,阴极为氢氧化钾溶液,所以反应为水电离出的氢离子得电子,反应为2H2O+2e- 2OH-+H2↑。②隔膜是阳离子交换膜,其主要交换的离子是K+,电解时,阳离子向阴极迁移,所以K+的迁移方向为由a到b。③KClO3氧化法的主要不足之处在于生产中会产生污染环境的氯气。
近几年高考工艺流程题易错的热点提问1.分析循环利用的物质和可回收的物质循环利用和回收利用是工业生产提高经济效益、降低污染、提高物质的利用率等的必要手段。(1)理解物质循环利用的目的:节能减排、“绿色化学”、降低成本等。提炼出:一定不会用于循环的物质可能是目标产物、杂质;可以用于循环的物质可能是辅助试剂、母液。(2)可回收的物质:副产品(非目标产品)。应对策略:弄清楚每一步的反应物和产物,对比“投入”和“输出”,既消耗又生成的物质即为循环利用物质。
近几年高考工艺流程题易错的热点提问2.分析调节溶液的pH(1)目的:使溶液中的某金属阳离子形成氢氧化物完全沉淀下来而除去。(2)需要的物质:含主要阳离子的难溶性氧化物或氢氧化物或碳酸盐,即能与H+反应,是使pH增大的物质,如MgO、Mg(OH)2等。(3)原理:加入的物质能与溶液中的H+反应,降低了H+的浓度,增大pH。④pH控制的范围:大于除去离子的完全沉淀的pH,小于所需离子的开始沉淀的pH。
4.分析控制温度温度的控制,实际生产过程中主要基于反应速率、物质的溶解度(溶解度曲线)、物质的热分解与挥发(物质的性质分析)、弱离子的水解(平衡)、能源的利用(耗能)、副反应的发生、催化剂的活性、生产安全性等方面的思考。一般需要考虑温度过高、过低会有怎样的效果。具体如下:(1)加热:加快反应速率或溶解速率;促进平衡向吸热方向移动;除杂,除去热稳定性弱的杂质,如NaHCO3、Ca(HCO3)2、KMnO4、NH4Cl等;使沸点相对较低的原料气化。
(2)降温:防止某物质在高温时溶解(或分解);使化学平衡向着题目要求的方向移动(放热方向);使某个沸点较高的产物液化,使其与其他物质分离;降低晶体的溶解度,减少损失,尤其是减压蒸发、减压烘干,通过降低温度需求,防止目标物质的分解。(3)控温(用水浴或油浴控温):防止某种物质温度过高时会分解或挥发,为了使某物质达到沸点挥发出来;使催化剂的活性达到最好;防止副反应的发生;降温或减压可以减少能源成本、降低对设备的要求,达到绿色化学的要求。
相关课件
这是一份2021届高考化学三轮复习专项冲刺:综合实验探究(第二课时)课件PPT,共25页。PPT课件主要包含了考点3,典例分析,考点4,能力提升等内容,欢迎下载使用。
这是一份2021届高考化学三轮复习专项冲刺:综合实验(一)课件PPT,共26页。PPT课件主要包含了实验综合题特点,考情预测,常见的量气装置,实验综合题常见考查点等内容,欢迎下载使用。
这是一份2021届高考化学三轮复习专项冲刺:综合实验(三)课件PPT,共35页。PPT课件主要包含了实验综合题常见考查点,分析模型,明确题型,了解原理,物质制备分离型,性质原理探究型,定量分析型,装置功能各步骤分目的,实验目的方法,物质结构性质等内容,欢迎下载使用。









