

2022年中考化学专题复习——常见的碱及性质
展开
这是一份2022年中考化学专题复习——常见的碱及性质,共15页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
2022年中考化学专题复习——常见的碱及性质
一、选择题
1.氢氧化钙可用于改良酸性土壤,其俗称是( )
A.熟石灰 B.石灰石 C.生石灰 D.碱石灰
2.下列物质间能够发生反应,但没有出现明显现象的是( )
A.将稀盐酸滴入盛石灰石的试管中
B.将CO2通入NaOH溶液中
C.将碳酸钠溶液滴入澄清石灰水中
D.将稀硫酸滴入NaCl溶液中
3.对于碱,下列说法正确的是( )
A.碱一定含有 H 元素 B.可使酚酞变红的都是碱溶液
C.所有非金属氧化物都可与碱溶液反应 D.酸与碱反应一定不产生沉淀
4.若利用碱的性质进行下列实验,不能达到相应目的的是( )
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
5.下列物质不能与NaOH溶液反应的是( )
A.二氧化碳 B.硝酸 C.硫酸铜 D.氢氧化铁
6.下列做法利用了酸碱中和反应原理的是( )
A.用食醋腌木瓜放入食盐进行调味 B.用稀盐酸除去铁钉上的铁锈
C.焙制蛋糕时加入碳酸氢钠使蛋糕膨松 D.服用含氢氧化铝的药物治疗胃酸过多症
7.能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是( )
A.HCl B.KNO3 C.Na2CO3 D.FeCl3
8.物质的性质决定它的用途还决定了它的保存方法。固体氢氧化钠具有以下性质:①白色片状固体②有强腐蚀性③易吸收水分而潮解④易溶于水,且溶解放热⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )
A.①② B.①②③ C.②③④ D.③⑤
9.碱溶液中都含有OH﹣,因此不同的碱表现出一些共同的性质.下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A.能使紫色石蕊溶液变蓝色 B.能与盐酸反应生成水
C.能与CO2反应生成水 D.能与Na2SO4溶液反应生成BaSO4沉淀
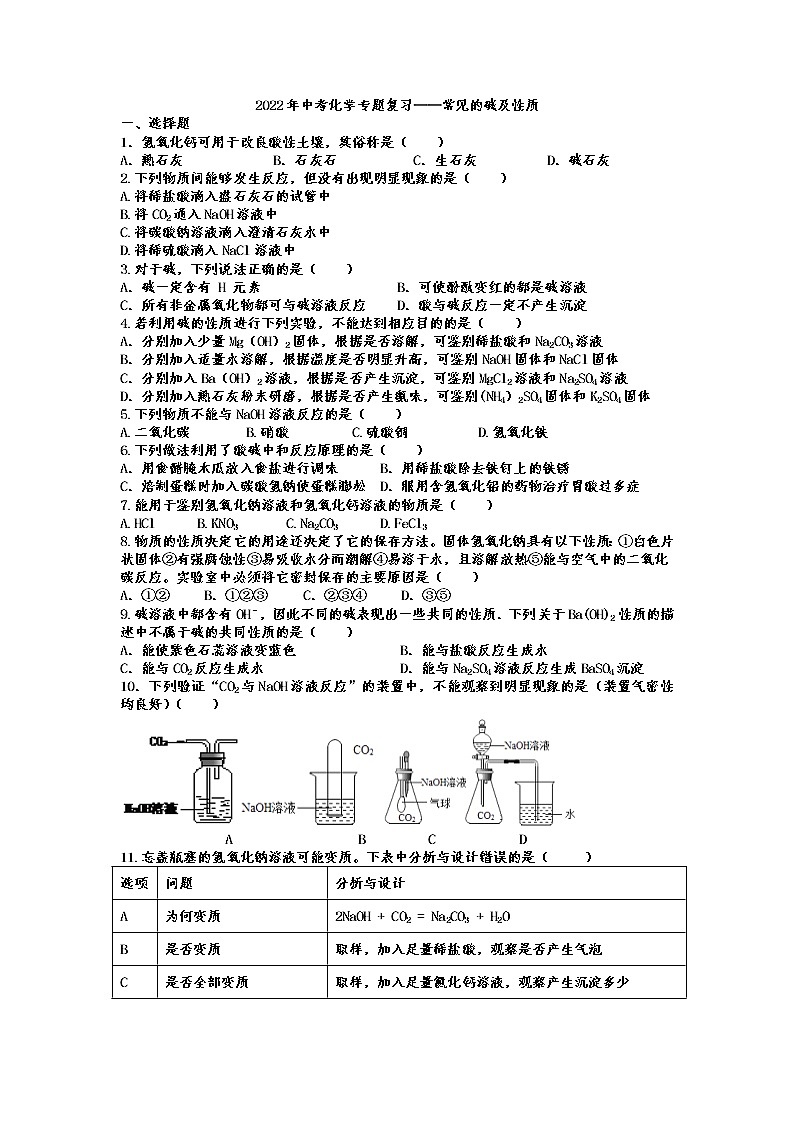
10.下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)( )
A B C D
11.忘盖瓶塞的氢氧化钠溶液可能变质。下表中分析与设计错误的是( )
选项
问题
分析与设计
A
为何变质
2NaOH + CO2 = Na2CO3 + H2O
B
是否变质
取样,加入足量稀盐酸,观察是否产生气泡
C
是否全部变质
取样,加入足量氯化钙溶液,观察产生沉淀多少
D
如何除去杂质
取样,加入适量氢氧化钙溶液,过滤
12.下列能使紫色石蕊试液和无色酚酞试液均变色的是( )
A.pH=1的盐酸 B.pH=3的硫酸
C.pH=7的氯化钠溶液 D.pH=14的氢氧化钾溶液
13.下列物质的用途错误的是( )
A、氢氧化铝用于治疗胃酸过多
B、铁质水龙头上镀铬延长使用寿命
C、氢氧化钠用于生产肥皂
D、用炉具清洁剂
清洗餐具
A.A B.B C.C D.D
14.某同学将一定量的Na2CO3与Ba(OH)2溶液混合,要想检验反应后Ba(OH)2是否过量,应选用的试剂是( )
A. 酚酞 B. CuCl2溶液 C. Na2CO3溶液 D. NaCl溶液
15.1839年虎门销烟采用的方法是:在海边挖池,放入烟土,引入海水浸泡,投入石灰,石灰遇水沸腾,烟土溶解。该过程发生的反应有CaO+H2O==Ca(OH)2。下列说法不正确的是
A. 该反应属于化合反应
B. 该反应会放出热量
C. 由此反应推测氧化钙可干燥氯化氢气体
D. 此反应可制备氢氧化钙
16.氢氧化钴[Co(OH)2]能与酸性溶液反应,可作涂料和清漆的干燥剂.制备方法为:①Co+2HCl═CoCl2+H2↑;②CoCl2+2NaOH═Co(OH)2↓+2NaCl。下列判断错误的是( )
A.①为置换反应
B.氢氧化钴可以干燥氯化氢气体
C.②为复分解反应
D.钴的金属活动性比铜的弱
17.如图是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
18.工业用煤燃烧产生二氧化硫,在排放前需经处理,如图是两种除硫工艺中主要物质的转化路径(部分产物已略)。
若每1000g Ca(OH)2和NaOH的市场价格分别按0.36元、2.90元计算,下列说法不正确的是( )
A. 煤是不能再生的化石燃料
B. 反应Ⅰ的化学反应方程式为:SO2+2NaOH=Na2SO3+H2O
C. “双碱法”中的NaOH可以循环使用,节约成本
D. 处理相同的SO2,“钠碱法”所需的原料成本更低
19.向一定质量的CuSO4溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列有关说法不正确的是( )
A.b点时所加试剂一定是稀盐酸
B.加入试剂总体积为V1时,溶液中不存在NaOH
C.c点时溶液中的溶质都是盐
D.a点时溶液中一定不存在Cu2+
20某兴趣小组进行了化学探究活动。
实验一:相同条件下,将10.00g下列物质分别置于相同规格的烧杯中,敞口放置在空气中,烧杯中物质质量随时间变化如下表。
时间
水
饱和石灰水
稀盐酸
浓硫酸
氢氧化钠溶液
n小时
8.14g
8.32g
8.62g
11.16g
9.36g
2n小时
5.74g
5.93g
6.67g
12.53g
8.45g
实验二:
下列说法不正确的是
A. 浓硫酸敞口久置后浓度会变小
B. 实验二的溶液①中溶质只有Na2CO3
C. 稀盐酸敞口久置后浓度可能会变大
D. 饱和石灰水的质量变化小于水的质量变化,原因之一是饱和石灰水吸收了空气中的CO2
二、非选择题
21.根据碱的四条化学性质回答下列问题:
(1)碱溶液能使酚酞溶液变______色;
(2)图中的X代表一类物质,则X为____________(填物质类别),请写出符合性质③的一个化学反应方程式_____________________________________;
(3)碱溶液有相似化学性质的原因是都含有__________。
22.请回答下列有关问题:
(1)小江同学取5mL氢氧化钠溶液于试管中,滴入几滴酚酞溶液,可观察到的现象为 。
(2)小东同学走进实验室时,看到氢氧化钠溶液的试剂瓶敞口放置,这样会使氢氧化钠溶液变质.若溶液部分变质,溶质是 (填化学式),氢氧化钠溶液变质的化学方程式是 。
(3)要配制50g溶质质量分数为5%的氯化钠溶液,需要氯化钠固体 克;量取水时俯视读数,导致配制的氯化钠溶液的溶质质量分数 (填“偏大”或“偏小”)。
23.图1是关于氢氧化钠化学性质的思维导图,请据图回答问题。
(1)性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈______色。
(2)性质②,将氢氧化钠溶液滴入稀盐酸中、图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是______(填化学式)。
(3)依据性质③,除去硫酸厂在生产过程中产生的二氧化硫气体,化学方程式为______。
(4)性质④,将氢氧化钠固体和某种盐混合研磨,能放出有刺激性气味的气体。推测这种盐可能是______。
24.用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。
(1)先推入的溶液是 。
(2)bc段压强不变,原因是 。
(3)cd段压强变大,用化学方程式解释: 。
25.在《探究酸、碱的化学性质》实验课上,某同学向盛有约2mL氢氧化钠溶液的试管中滴加稀硫酸,没有观察到现象。请教老师后,他发现自己在滴加稀硫酸前忘了加入酸碱指示剂,导致无法判断反应情况,于是他对试管中溶液的中和程度进行探究。
(探究目的)探究试管中溶液的中和程度。
(实验原理)试管中发生反应的化学方程式为_____。
(做出猜想)
猜想l:氢氧化钠未完全反应,溶液呈碱性。
猜想2:氢氧化钠和硫酸恰好完全反应,溶液呈中性。
猜想3:氢氧化钠完全反应、硫酸过量,溶液呈酸性。
(进行实验)
实验操作
实验现象
实验结论
另用试管取该溶液1~2mL,滴入1~2滴无色酚酞溶液,振荡
溶液变_____
溶液呈碱性
溶液不变色
溶液呈酸性或中性
(分析思考)(1)若溶液呈碱性,向试管里的溶液中逐滴加入FeCl3溶液,将产生红褐色沉淀,反应的化学方程式为_____。
(2)若滴入酚酞后溶液不变色,为进一步确定溶液的酸碱性,该同学提出了以下方案:
方案1
用pH试纸测其酸碱度,若pH_____7(选填“>”“<”或“=”),则溶液呈酸性
方案2
加入金属锌,若有气泡产生,则溶液呈酸性,该反应的化学方程式为_____。
26.某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,同学们进行了以下探究:
(1)(提出问题)氢氧化钠溶液是否变质?变质程度如何?
(做出猜想)猜想一:氢氧化钠溶液未变质
猜想二:氢氧化钠溶液完全变质
猜想三:________。
(2)(设计实验)请完成实验报告
实验步骤
实验现象
实验结论
①取少量溶液于试管中,加入________,充分反应。
________
猜想二成立
②将步骤①试管中的物质过滤,向滤液中加入________。
无明显现象
(3)(反思拓展)
①氢氧化钠溶液变质的原因________(用化学方程式表示),氢氧化钠溶液应________保存。
②分别取两份完全变质的氢氧化钠溶液样品于试管中,向其中一份加入盐酸有气泡产生,另一份加入氢氧化钙溶液有白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,所得溶液中溶质一定有________。
27.实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物。同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究。
查阅资料:(1)Ca(OH)2、Na2CO3溶于水无明显的温度变化。
(2)CaCl2+Na2CO32NaCl+CaCO3↓。
(3)CaCl2溶液呈中性。
(1)滤渣B中一定含有_____________,产生该物质的化学方程式可能是___________________________________(写出一个即可)。
(2)滤液C成分的探究。
【猜想】滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④____________。
【设计方案并进行实验】甲、乙、丙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3。
乙同学:取滤液C少许放入试管中,滴加足量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH。
丙同学:取滤液C少许放入试管中,滴加Ca(OH)2溶液,有白色沉淀产生。向上层清液中滴加无色酚酞,无色酚酞变成红色,则滤液C中的溶质是NaOH和Na2CO3。
【反思与评价】丁同学认真分析上述三位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断。他认为滤液C中的溶质一定含有__________________,可能含有NaOH。为进一步确认滤液C中是否含有NaOH,请你帮助他设计实验进行验证。
实验操作
实验现象
实验结论及解释
______________________________
______________________
猜想④正确
(3)实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热。综合对滤液和滤渣成分的探究,下列对样品成分的分析正确的是__________(填序号)。
①样品中一定含NaOH ②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种
28.学习化学开启了我们认识物质之旅。某实验小组的同学对氢氧化钠的性质及应用进行了如下的探究。
探究一:溶解过程中的能量变化如图所示,同学们设计了不同的实验方案进行探究:
(1)实验一中的硝酸铵溶解后,溶液温度______(填“升高”、“降低”或“不变”)。
(2)实验二所加试剂及用量如图,将分液漏斗中的水全部加入试管后,立即关闭分液漏斗的活塞,此时观察到U形管的液面左低右高,由此小明得出“氢氧化钠溶于水时放出热量”的结论,你是否同意小明的结论并写出你的理由______。
探究二:氢氧化钠的化学性质如图,同学们用氢氧化钠溶液进行了下列实验,请分析并回答下列问题:
(3)A试管中观察到的现象是_____。
(4)C、D试管中均无明显现象。
①为了证明D中已发生化学反应,向该试管中再加入足量的_____,观察到有气泡产生。
②为了证明氢氧化钠溶液和稀盐酸能发生化学反应,同学们设计并进行了如图实验:(所用稀盐酸经估算确保过量)整个实验过程中无明显现象,证明氢氧化钠溶液和稀盐酸能发生化学反应。请写出步骤Ⅱ中所加试剂_____。
探究三:工业中的应用
氢氧化钠常用于制造人造丝、造纸、炼油、纺织、印染与橡胶工业。某造纸厂废水中NaOH的质量分数1.6%,现有废硫酸4.9t(H2SO4的质量分数为20%),可以处理的废水质量是______t。结合化学方程式中的数据分析:若将等质量、等溶质质量分数的稀硫酸和氢氧化钠溶液混合,充分反应后,请判断溶液中一定含有的溶质,并简述你的判断理由:______。
2022年中考化学专题复习——常见的碱及性质参考答案
一、选择题
1.氢氧化钙可用于改良酸性土壤,其俗称是( )
A.熟石灰 B.石灰石 C.生石灰 D.碱石灰
【答案】A。
2.下列物质间能够发生反应,但没有出现明显现象的是( )
A.将稀盐酸滴入盛石灰石的试管中
B.将CO2通入NaOH溶液中
C.将碳酸钠溶液滴入澄清石灰水中
D.将稀硫酸滴入NaCl溶液中
【答案】B
3.对于碱,下列说法正确的是( )
A.碱一定含有 H 元素 B.可使酚酞变红的都是碱溶液
C.所有非金属氧化物都可与碱溶液反应 D.酸与碱反应一定不产生沉淀
【答案】A
4.若利用碱的性质进行下列实验,不能达到相应目的的是( )
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
【答案】C
5.下列物质不能与NaOH溶液反应的是( )
A.二氧化碳 B.硝酸 C.硫酸铜 D.氢氧化铁
【答案】D
6.下列做法利用了酸碱中和反应原理的是( )
A.用食醋腌木瓜放入食盐进行调味 B.用稀盐酸除去铁钉上的铁锈
C.焙制蛋糕时加入碳酸氢钠使蛋糕膨松 D.服用含氢氧化铝的药物治疗胃酸过多症
【答案】D
7.能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是( )
A.HCl B.KNO3 C.Na2CO3 D.FeCl3
【答案】C
8.物质的性质决定它的用途还决定了它的保存方法。固体氢氧化钠具有以下性质:①白色片状固体②有强腐蚀性③易吸收水分而潮解④易溶于水,且溶解放热⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )
A.①② B.①②③ C.②③④ D.③⑤
【答案】D
9.碱溶液中都含有OH﹣,因此不同的碱表现出一些共同的性质.下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A.能使紫色石蕊溶液变蓝色 B.能与盐酸反应生成水
C.能与CO2反应生成水 D.能与Na2SO4溶液反应生成BaSO4沉淀
【答案】D
10.下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)( )
A B C D
【答案】A
11.忘盖瓶塞的氢氧化钠溶液可能变质。下表中分析与设计错误的是( )
选项
问题
分析与设计
A
为何变质
2NaOH + CO2 = Na2CO3 + H2O
B
是否变质
取样,加入足量稀盐酸,观察是否产生气泡
C
是否全部变质
取样,加入足量氯化钙溶液,观察产生沉淀多少
D
如何除去杂质
取样,加入适量氢氧化钙溶液,过滤
【答案】C
12.下列能使紫色石蕊试液和无色酚酞试液均变色的是( )
A.pH=1的盐酸 B.pH=3的硫酸
C.pH=7的氯化钠溶液 D.pH=14的氢氧化钾溶液
【答案】D
13.下列物质的用途错误的是( )
A、氢氧化铝用于治疗胃酸过多
B、铁质水龙头上镀铬延长使用寿命
C、氢氧化钠用于生产肥皂
D、用炉具清洁剂
清洗餐具
A.A B.B C.C D.D
【答案】D。
14.某同学将一定量的Na2CO3与Ba(OH)2溶液混合,要想检验反应后Ba(OH)2是否过量,应选用的试剂是( )
A. 酚酞 B. CuCl2溶液 C. Na2CO3溶液 D. NaCl溶液
【答案】C
15.1839年虎门销烟采用的方法是:在海边挖池,放入烟土,引入海水浸泡,投入石灰,石灰遇水沸腾,烟土溶解。该过程发生的反应有CaO+H2O==Ca(OH)2。下列说法不正确的是
A. 该反应属于化合反应
B. 该反应会放出热量
C. 由此反应推测氧化钙可干燥氯化氢气体
D. 此反应可制备氢氧化钙
【答案】C
16.氢氧化钴[Co(OH)2]能与酸性溶液反应,可作涂料和清漆的干燥剂.制备方法为:①Co+2HCl═CoCl2+H2↑;②CoCl2+2NaOH═Co(OH)2↓+2NaCl。下列判断错误的是( )
A.①为置换反应
B.氢氧化钴可以干燥氯化氢气体
C.②为复分解反应
D.钴的金属活动性比铜的弱
【答案】B
17.如图是室温下稀硫酸和氢氧化钠反应过程中的pH变化曲线。下列有关说法正确的是( )
A.图中X是氢氧化钠
B.图中a点的阴离子是OH-
C.向图中c点所示溶液中加入铁粉后,溶液中有气泡产生
D.稀硫酸与氢氧化钠溶液反应的化学方程式为:H2SO4+2NaOH═Na2SO4+H2O
【答案】C
18.工业用煤燃烧产生二氧化硫,在排放前需经处理,如图是两种除硫工艺中主要物质的转化路径(部分产物已略)。
若每1000g Ca(OH)2和NaOH的市场价格分别按0.36元、2.90元计算,下列说法不正确的是( )
A. 煤是不能再生的化石燃料
B. 反应Ⅰ的化学反应方程式为:SO2+2NaOH=Na2SO3+H2O
C. “双碱法”中的NaOH可以循环使用,节约成本
D. 处理相同的SO2,“钠碱法”所需的原料成本更低
【答案】D
19.向一定质量的CuSO4溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所得沉淀质量随加入试剂总体积的变化趋势如图所示。下列有关说法不正确的是( )
A.b点时所加试剂一定是稀盐酸
B.加入试剂总体积为V1时,溶液中不存在NaOH
C.c点时溶液中的溶质都是盐
D.a点时溶液中一定不存在Cu2+
【答案】D
20某兴趣小组进行了化学探究活动。
实验一:相同条件下,将10.00g下列物质分别置于相同规格的烧杯中,敞口放置在空气中,烧杯中物质质量随时间变化如下表。
时间
水
饱和石灰水
稀盐酸
浓硫酸
氢氧化钠溶液
n小时
8.14g
8.32g
8.62g
11.16g
9.36g
2n小时
5.74g
5.93g
6.67g
12.53g
8.45g
实验二:
下列说法不正确的是
A. 浓硫酸敞口久置后浓度会变小
B. 实验二的溶液①中溶质只有Na2CO3
C. 稀盐酸敞口久置后浓度可能会变大
D. 饱和石灰水的质量变化小于水的质量变化,原因之一是饱和石灰水吸收了空气中的CO2
【答案】B
二、非选择题
21.根据碱的四条化学性质回答下列问题:
(1)碱溶液能使酚酞溶液变______色;
(2)图中的X代表一类物质,则X为____________(填物质类别),请写出符合性质③的一个化学反应方程式_____________________________________;
(3)碱溶液有相似化学性质的原因是都含有__________。
【答案】(1)红;
(2)酸,NaOH+HCl=NaCl+H2O;
(3)氢氧根离子
22.请回答下列有关问题:
(1)小江同学取5mL氢氧化钠溶液于试管中,滴入几滴酚酞溶液,可观察到的现象为 。
(2)小东同学走进实验室时,看到氢氧化钠溶液的试剂瓶敞口放置,这样会使氢氧化钠溶液变质.若溶液部分变质,溶质是 (填化学式),氢氧化钠溶液变质的化学方程式是 。
(3)要配制50g溶质质量分数为5%的氯化钠溶液,需要氯化钠固体 克;量取水时俯视读数,导致配制的氯化钠溶液的溶质质量分数 (填“偏大”或“偏小”)。
【答案】(1)无色溶液变红色;
(2)NaOH、Na2CO3,2NaOH+CO2=Na2CO3+H2O;
(3)50g×5%=2.5g,偏大
23.图1是关于氢氧化钠化学性质的思维导图,请据图回答问题。
(1)性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈______色。
(2)性质②,将氢氧化钠溶液滴入稀盐酸中、图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是______(填化学式)。
(3)依据性质③,除去硫酸厂在生产过程中产生的二氧化硫气体,化学方程式为______。
(4)性质④,将氢氧化钠固体和某种盐混合研磨,能放出有刺激性气味的气体。推测这种盐可能是______。
【答案】红 NaCl、NaOH 铵盐
24.用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。
(1)先推入的溶液是 。
(2)bc段压强不变,原因是 。
(3)cd段压强变大,用化学方程式解释: 。
【答案】(1)氢氧化钠溶液;
(2)盐酸先和过量的氢氧化钠反应生成氯化钠和水;
(3)Na2CO3+2HCl═2NaCl+H2O+CO2↑。
25.在《探究酸、碱的化学性质》实验课上,某同学向盛有约2mL氢氧化钠溶液的试管中滴加稀硫酸,没有观察到现象。请教老师后,他发现自己在滴加稀硫酸前忘了加入酸碱指示剂,导致无法判断反应情况,于是他对试管中溶液的中和程度进行探究。
(探究目的)探究试管中溶液的中和程度。
(实验原理)试管中发生反应的化学方程式为_____。
(做出猜想)
猜想l:氢氧化钠未完全反应,溶液呈碱性。
猜想2:氢氧化钠和硫酸恰好完全反应,溶液呈中性。
猜想3:氢氧化钠完全反应、硫酸过量,溶液呈酸性。
(进行实验)
实验操作
实验现象
实验结论
另用试管取该溶液1~2mL,滴入1~2滴无色酚酞溶液,振荡
溶液变_____
溶液呈碱性
溶液不变色
溶液呈酸性或中性
(分析思考)(1)若溶液呈碱性,向试管里的溶液中逐滴加入FeCl3溶液,将产生红褐色沉淀,反应的化学方程式为_____。
(2)若滴入酚酞后溶液不变色,为进一步确定溶液的酸碱性,该同学提出了以下方案:
方案1
用pH试纸测其酸碱度,若pH_____7(选填“>”“<”或“=”),则溶液呈酸性
方案2
加入金属锌,若有气泡产生,则溶液呈酸性,该反应的化学方程式为_____。
【答案】2NaOH+H2SO4=Na2SO4+2H2O 红色 3NaOH+FeCl3=Fe(OH)3↓+3NaCl < Zn+H2SO4=ZnSO4+H2↑
26.某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,同学们进行了以下探究:
(1)(提出问题)氢氧化钠溶液是否变质?变质程度如何?
(做出猜想)猜想一:氢氧化钠溶液未变质
猜想二:氢氧化钠溶液完全变质
猜想三:________。
(2)(设计实验)请完成实验报告
实验步骤
实验现象
实验结论
①取少量溶液于试管中,加入________,充分反应。
________
猜想二成立
②将步骤①试管中的物质过滤,向滤液中加入________。
无明显现象
(3)(反思拓展)
①氢氧化钠溶液变质的原因________(用化学方程式表示),氢氧化钠溶液应________保存。
②分别取两份完全变质的氢氧化钠溶液样品于试管中,向其中一份加入盐酸有气泡产生,另一份加入氢氧化钙溶液有白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,所得溶液中溶质一定有________。
【答案】 (1)氢氧化钠溶液部分变质
(2)加入足量(或过量)的氯化钙溶液(或可溶性钙盐、钡盐溶液)(合理即可);产生白色沉淀(或产生白色浑浊);酚酞溶液(或可溶性铜盐、铁盐、镁盐溶液、石蕊溶液)(合理即可)
(3)2NaOH+CO2 ==Na2CO3+H2O;密封;氯化钠、氯化钙(或NaCl、CaC12)
27.实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物。同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究。
查阅资料:(1)Ca(OH)2、Na2CO3溶于水无明显的温度变化。
(2)CaCl2+Na2CO32NaCl+CaCO3↓。
(3)CaCl2溶液呈中性。
(1)滤渣B中一定含有_____________,产生该物质的化学方程式可能是___________________________________(写出一个即可)。
(2)滤液C成分的探究。
【猜想】滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④____________。
【设计方案并进行实验】甲、乙、丙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3。
乙同学:取滤液C少许放入试管中,滴加足量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH。
丙同学:取滤液C少许放入试管中,滴加Ca(OH)2溶液,有白色沉淀产生。向上层清液中滴加无色酚酞,无色酚酞变成红色,则滤液C中的溶质是NaOH和Na2CO3。
【反思与评价】丁同学认真分析上述三位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断。他认为滤液C中的溶质一定含有__________________,可能含有NaOH。为进一步确认滤液C中是否含有NaOH,请你帮助他设计实验进行验证。
实验操作
实验现象
实验结论及解释
______________________________
______________________
猜想④正确
(3)实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热。综合对滤液和滤渣成分的探究,下列对样品成分的分析正确的是__________(填序号)。
①样品中一定含NaOH ②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种
【答案】(1)CaCO3 Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
(2)【猜想】NaOH和Na2CO3
【反思与评价】Na2CO3 取少量滤液C于试管中,加入足量CaCl2溶液,过滤,在滤液中滴加无色酚酞试液 有白色沉淀生成,溶液由无色变成红色
(3)②③
28.学习化学开启了我们认识物质之旅。某实验小组的同学对氢氧化钠的性质及应用进行了如下的探究。
探究一:溶解过程中的能量变化如图所示,同学们设计了不同的实验方案进行探究:
(1)实验一中的硝酸铵溶解后,溶液温度______(填“升高”、“降低”或“不变”)。
(2)实验二所加试剂及用量如图,将分液漏斗中的水全部加入试管后,立即关闭分液漏斗的活塞,此时观察到U形管的液面左低右高,由此小明得出“氢氧化钠溶于水时放出热量”的结论,你是否同意小明的结论并写出你的理由______。
探究二:氢氧化钠的化学性质如图,同学们用氢氧化钠溶液进行了下列实验,请分析并回答下列问题:
(3)A试管中观察到的现象是_____。
(4)C、D试管中均无明显现象。
①为了证明D中已发生化学反应,向该试管中再加入足量的_____,观察到有气泡产生。
②为了证明氢氧化钠溶液和稀盐酸能发生化学反应,同学们设计并进行了如图实验:(所用稀盐酸经估算确保过量)整个实验过程中无明显现象,证明氢氧化钠溶液和稀盐酸能发生化学反应。请写出步骤Ⅱ中所加试剂_____。
探究三:工业中的应用
氢氧化钠常用于制造人造丝、造纸、炼油、纺织、印染与橡胶工业。某造纸厂废水中NaOH的质量分数1.6%,现有废硫酸4.9t(H2SO4的质量分数为20%),可以处理的废水质量是______t。结合化学方程式中的数据分析:若将等质量、等溶质质量分数的稀硫酸和氢氧化钠溶液混合,充分反应后,请判断溶液中一定含有的溶质,并简述你的判断理由:______。
【答案】 ①. 降低 ②. 加入10mL水后试管中的部分空气被排出,也会使U形管中液面左低右高,无法得到小明的结论(其他合理答案均可) ③. 溶液由无色变红色 ④. 稀盐酸(或稀硫酸等) ⑤. 酚酞试液(或硫酸铜溶液或氯化铁溶液) ⑥. 50 ⑦. 溶质是一定有NaOH和Na2SO4,因为NaOH与H2SO4反应生Na2SO4和H2O,所以反应后的溶质一定含Na2SO4,又依据可知每98份质量的H2SO4和80份质量的NaOH恰好完全反应,所以等质量、等溶质质量分数的稀硫酸和氢氧化钠溶液混合,充分反应后氢氧化钠过量,所以溶液中一定有NaOH
相关试卷
这是一份中考化学一轮复习考点过关练习考点34 常见的碱及性质(含解析),共27页。试卷主要包含了 常见碱的性质及用途, 碱的化学性质, 氢氧化钠和氢氧化钙的变质探究,下列关于Ca2的说法错误的是,22L<V<0等内容,欢迎下载使用。
这是一份中考化学一轮复习过关练习考点34 常见的碱及性质(教师版),共27页。试卷主要包含了 常见碱的性质及用途, 碱的化学性质, 氢氧化钠和氢氧化钙的变质探究,下列关于Ca2的说法错误的是,22L<V<0等内容,欢迎下载使用。
这是一份初中化学中考复习 考点34 常见的碱及性质-备战2022年中考化学一轮复习考点帮(原卷版),共18页。试卷主要包含了 常见碱的性质及用途, 碱的化学性质, 氢氧化钠和氢氧化钙的变质探究,下列关于Ca2的说法错误的是等内容,欢迎下载使用。








