

2022年广东省深圳市中考模拟化学试卷3(word版含答案)
展开
这是一份2022年广东省深圳市中考模拟化学试卷3(word版含答案),共13页。试卷主要包含了单项选择 I,单项选择 II,非选择题等内容,欢迎下载使用。
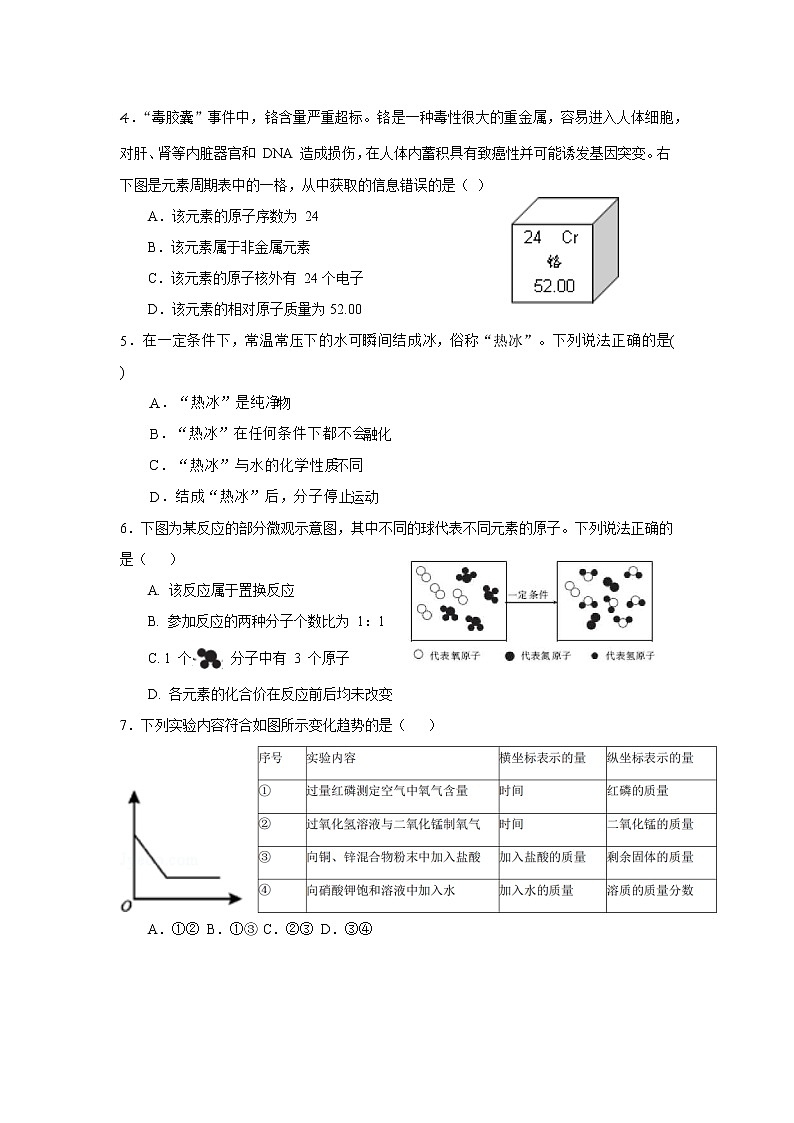
2022年广东省深圳市中考化学模拟卷(3)第一部分:选择题一、单项选择 I:(本大题共 8 小题,每小题 1.5 分,共 12 分。在每小题列出的 四个选项中,只有一项符合题意。)1.中考复习阶段,小轩同学梳理了以下知识:①利用金属的化学性质可以区别不同金属的活动性强弱;②催化剂一定能加快化学反应的速率;③具有可燃性的气体有甲烷、氢气和氧气;④燃烧需要同时满足三个条件,故破坏其中一个条件就可以灭火;⑤微量元素是人体健康必不可少的,但补充微量元素也要适可而止;⑥二氧化碳能灭火是因为不能燃烧也不能支持燃烧且密度比空气大,而用水灭火是因为可降低可燃物的着火点。其中你认为合理的是( )A. ①④⑤ B. ①③⑥ C. ②⑤⑥ D. ②④⑤2.下列关于四种粒子的结构示意图的说法中正确的是( ) A. ① ③是不同种元素B. ① ④表示的是离子C. ② 表示的元素在化合物中通常显-1价D. ③ ④在化学变化中易得到电子3.下列实验操作中正确的是( ) A. 取用少量液体 B. 过滤 C. 闻气味 D. 稀释浓硫酸 4.“毒胶囊”事件中,铬含量严重超标。铬是一种毒性很大的重金属,容易进入人体细胞,对肝、肾等内脏器官和 DNA 造成损伤,在人体内蓄积具有致癌性并可能诱发基因突变。右下图是元素周期表中的一格,从中获取的信息错误的是( ) A.该元素的原子序数为 24B.该元素属于非金属元素C.该元素的原子核外有 24个电子D.该元素的相对原子质量为52.005.在一定条件下,常温常压下的水可瞬间结成冰,俗称“热冰”。下列说法正确的是( ) A.“热冰”是纯净物B.“热冰”在任何条件下都不会融化C.“热冰”与水的化学性质不同D.结成“热冰”后,分子停止运动6.下图为某反应的部分微观示意图,其中不同的球代表不同元素的原子。下列说法正确的是( )A. 该反应属于置换反应B. 参加反应的两种分子个数比为 1:1C. 1 个 分子中有 3 个原子D. 各元素的化合价在反应前后均未改变7.下列实验内容符合如图所示变化趋势的是( ) A.①② B.①③ C.②③ D.③④ 8.蚂蚁会分泌一种信息素(C10H18O)。下面对该信息素的说法中正确的是( )A.该信息素是由C、H、O三种元素组成的有机物B.该信息素中C、H、O三种元素的质量比为10:18:1C.C10H18O的相对分子质量为156D.该信息素中氢元素的质量分数最大二、单项选择 II:(本大题共 4 小题,每小题 2 分,共 8 分。在每小题列出的四个选项中,只有一项符合题意。)9.下列除杂所用试剂及实验过程都正确的是(括号内为杂质)( )A. KCl(K2CO3) 加足量稀硫酸、过滤、蒸发、结晶B. BaSO4(BaCO3) 加足量稀盐酸、过滤、洗涤、干燥C. CuO(Cu) 加足量稀盐酸、过滤、洗涤、干燥D. NaCl (KCl) 加水溶解、过滤、蒸发、结晶10.如图是a、b、c三种物质的溶解度曲线,下列说法错误的是
A. t2℃时,将30g a物质加入到50g水中充分搅拌,得到75g a的饱和溶液B. 将c的饱和溶液变为不饱和溶液,可采用降温的方法C. P点表示t1℃时,a、c两种物质的溶解度相等D. t2℃时a、b、c三种物质的饱和溶液降温到t1℃时所得溶液溶质质量分数由大到小的顺序是b>a≥c 11.下列关于图像的描述正确的是( )① ② ③ ④A.图①表示室温下向饱和石灰水中加入一定量氧化钙,并恢复至室温B.图②表示把布满锈迹的铁钉投入到过量的稀硫酸中C.图③表示向氢氧化钠溶液中加入大量的水D.图④表示将饱和硝酸钾溶液恒温蒸发水份12.A-D是初中化学中常见物质,其转化关系如图所示(部分反应物和生成物、反应条件已略去),物质A、B常温下为无色气体且组成元素相同,物质C、D均为黑色粉末。下列判断错误的是 ( )A. 物质A、B均为氧化物B. 反应②属于置换反应C. 物质C可能是铜D. 物质B可以作植物营养剂 第二部分:非选择题三、非选择题:(本大题包括 4 小题,共 30 分)13.请结合图示实验装置,回答下列问题。(1)写出有标号的仪器名称:②____________ 。(2)用高锰酸钾制氧气选用的发生装置是___________________ (选填序号),反应的化学方程式为______________________________________ 。(3)若B装置中固体为锌粒,②中加入稀硫酸试剂可制H2。要获得干燥的H2,应先将气体通过盛有(填试剂名称)______________ 的D装置,再用E装置收集,气体应从(选填“a”或“b”)____________ 端通入。(4)实验室可用B或C装置制CO2,C相对于B装置的优点有_________________。14.某Fe3O4样品中可能含有的杂质是Fe2O3和FeO其中的一种。为探究杂质的情况设计如下方案:【实验设计】同学们称取了23.28 g该Fe3O4样品用图①进行了下列实验:【实验分析】因探究思路不同,兴趣小组分成甲、乙、丙三个讨论小组。甲组;(1)该组同学欲通过B装置反应前后的质量变化来计算确认该Fe3O4样品中的杂质。B中的最佳试剂是______(填序号)。①澄清石灰水 ②氢氧化钠浓溶液 ③稀盐酸 ④水(2)上述实验过程中,CO的作用有_______ (填序号)。①CO气体作为反应物②实验开始时,排尽装置中的空气,防止加热时发生爆炸③停止加热后,防止A中生成物被氧化④停止加热后防止B中的溶液倒吸入A中⑤对B中反应物起到一定的搅拌作用,便于CO2与反应液充分接触而反应乙组:(3)乙组同学认为B装置反应前后的质量差会偏小而影响计算、分析,你认为他们的理由是_______ ;改进为在B装置后接一盛有_______(填试剂名称)的广口瓶的吸水装置,将B装置和该装置“捆绑”称量,从而减小误差。丙组:(4)丙组同学将B装置中液体改换为Ba(OH)2溶液,通过测量生成的_______(填化学式)沉淀的质量来计算求解。为了获得沉淀,该组同学需要进行的操作有过滤→_______→________→称量。【查阅资料】Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4,再生成FeO(黑色),最后生成Fe;利用仪器测定并绘制成反应过程中A装置中玻璃管内的固体质量随温度的变化曲线(见图②)。(5)写出BC段发生反应的化学方程式:______________ 。(6)确定该Fe3O4样品中含有的杂质是_______,其中含Fe3O4的质量是_______g(不需要写出过程)(已知Fe3O4、FeO、Fe2O3中铁元素的质量分数分别为72.4%、77.8%、70.0%)。 15.根据“粗盐中难溶性杂质的去除”实验,回答有关问题。Ⅰ(1)实验步骤:①溶解 称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.2g。②过滤③蒸发 请从溶解度的角度分析,试验中不采用降低溶液温度的方法得到精盐的依据是__________。④计算产率 得到精盐3.2g,则精盐的产率为__________(计算结果保留一位小数)。(2)整个实验中至少要进行__________次称量。(3)从海水中获得的粗盐,经过上述实验得到的精盐属于__________(填“混合物”或“纯净物”)。Ⅱ乙同学用天平称量一定量的可能含氯化镁、硫酸钠和氯化钙的粗盐,并设计了如下过程进行除杂提纯,实验后得到较纯净的氯化钠固体。(此题中微溶物视为可溶物)(1)混合物甲中一定有的成分是____________________。(2)白色固体中一定有的成分为____________________。(3)加入B溶液后的现象为____________________。 16.实验室有一瓶久置的氢氧化钠固体,某兴趣小组同学想了解其变质情况,甲、乙同学各称取9.3g干燥的样品分别设计以下实验,实验过程如下:(1)实验一:甲同学取样品,加水使其完全溶解,然后向其中逐渐滴加氢氧化钙溶液,所得沉淀质量与加入氢氧化钙溶液质量关系如图所示,请回答以下问题:①B点对应的溶液中的溶质有_________________.②实验中若用氯化钙溶液代替氢氧化钙溶液,所得沉淀的质量_______________5g(填“大于”“等于”“小于”)(2)计算样品中碳酸钠的质量_____________,通过计算可知该氢氧化钠固体的变质程度为___________.(填“完全变质”“部分变质”“没有变质”)(3)实验二,乙同学取样品,加水使其完全溶解,往其中加入质量分数为7.3%的盐酸溶液,滴加至100克时,不再产生气体,请画出生成气体随加入盐酸溶液质量变化的曲线图. 参考答案与试题解析1.A2.D
3.C
4.B
5.A
6.A
7.B
8.A
9.B
10.D
11.B
12.B
13.分液漏斗 A 2KMnO4△K2MnO4+MnO2+O2↑ 浓硫酸 a 可控制反应的发生与停止【解析】(1). 分液漏斗(2). 用高锰酸钾制氧气选用的发生装置是加热固体制取气体的发生装置A (3).高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰、氧气, 化学方程式为2KMnO4△K2MnO4+MnO2+O2↑ (4). 浓硫酸有吸水性,可干燥氢气 ; (5). 用E装置收集,氢气的密度比空气小,气体应从a端通入。 (6). 发生装置C的优点是可控制反应的发生与停止,关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。14.(1)② (2)①②③④⑤(3)CO从B中溶液里逸出时会带出部分水蒸气 浓硫酸(4)BaCO3 洗涤 干燥 (5)Fe3O4+CO高温3FeO+CO2 (6)Fe2O3 21【解析】试题分析:(1)该组同学欲通过B装置反应前后的质量变化来计算确认该Fe3O4样品中的杂质,那么B装置的主要目的就是吸收反应生成的二氧化碳,故B中的最佳试剂是②,不用澄清石灰水的原因是氢氧化钙的溶解度很小,吸收效果差(2)上述实验过程中,CO的作用有:①CO气体作为反应物,正确,②实验开始时,排尽装置中的空气,防止加热时发生爆炸,正确,③停止加热后,防止A中生成物被氧化,正确,④停止加热后防止B中的溶液倒吸入A中,正确,⑤对B中反应物起到一定的搅拌作用,便于CO2与反应液充分接触而反应,正确,故选①②③④⑤(3)乙组同学认为B装置反应前后的质量差会偏小而影响计算、分析,他们的理由是:CO从B中溶液里逸出时会带出部分水蒸气,使得质量差偏小;由于浓硫酸具有吸水性,故可改进为在B装置后接一盛有浓硫酸的广口瓶的吸水装置,将B装置和该装置“捆绑”称量,从而减小误差(4)丙组同学将B装置中液体改换为Ba(OH)2溶液,那么发生反应:CO2 +Ba(OH)2 ==BaCO3↓+ H20,故可通过测量生成的BaCO3沉淀的质量来计算求解。为了获得沉淀,该组同学需要进行的操作有过滤→洗涤→干燥→称量(5)根据资料:Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4,再生成FeO(黑色),最后生成Fe ,故BC段发生反应的化学方程式:Fe3O4+CO高温3FeO+CO2(6)根据质量守恒定律,反应结束后得到铁的质量为16.8g,说明原样品中含铁元素的质量也为16.8g ,故铁元素的质量分数=16.8g/23.28g×100%=72.2%,本着“中间值或平均值”的思想,Fe3O4中铁元素的质量分数=77.8%>72.2%,那么另一种物质的铁元素质量分数就要小于72.2%,故Fe3O4样品中含有的杂质是Fe2O3;可设含Fe3O4的质量是x,那么Fe2O3的质量是(23.28g-x),故可列等式:x×168/232×100%+(23.28g-x)×112/160×100%,可计算出x=21g15. 氯化钠的溶解度受温度影响小 84.2% 3 混合物 NaCl,BaCl2,MgCl2 BaCO3 开始无现象,一段时间后产生气泡【解析】Ⅰ(1)③从溶解度的角度分析,实验中不采用降低溶液温度的方法得到精盐的依据是:氯化钠的溶解度受温度的变化影响较小,相同情况下降温析出的晶体比较少;故填:氯化钠的溶解度受温度的变化影响较小;④精盐的产率为: =84.2%,(2)需要称量的数据有:最初所取粗盐的质量、剩余粗盐的质量(以此运用差量法得出溶解的粗盐的质量),以及所得精盐的质量,因此,最少需要3次称量;(3)精盐中除了食盐,还有可溶性杂质,所以得到的精盐属于混合物;Ⅱ(1)加入氯化钡溶液无明显现象,说明样品中不含有硫酸钠,加入氢氧化钠溶液后产生沉淀,说明样品中含有氯化镁,因此混合物甲中一定有的成分是氯化钠、氯化钡、氯化镁;(2)加入碳酸钠溶液后得到的白色沉淀中一定有氯化钡和碳酸钠反应生成的碳酸钡,可能含有氯化钙和碳酸钠反应生成的碳酸钙,因此白色固体中一定有的成分为碳酸钡;(3 )加入的B溶液是稀盐酸,稀盐酸能和氢氧化钠反应生成氯化钠和水,能和碳酸钠反应生成氯化钠、水和二氧化碳,能够观察到开始无明显现象,后产生气泡。16. NaOH Ca(OH)2 等于 5.3g 部分变质 【解析】(1)①B点对应的溶液是氢氧化钙和碳酸钠反应后氢氧化钙过量的点,因此溶液中的溶质有反应生成的氢氧化钠和过量的氢氧化钙;
②实验二中若用氯化钙溶液代替氢氧化钙溶液,所得沉淀碳酸钙的质量取决于碳酸根结合钙离子的质量,与阴离子无关,故质量相等;
(2)设样品中碳酸钠的质量为x
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
x 5g= 解:x=5.3g;
样品的质量为9.3g,而碳酸钠为5.3g,因此还含有氢氧化钠,故是部分变质;(3)样品的质量为9.3g,而碳酸钠为5.3g,含有氢氧化钠9.3g-5.3g=4.0g
设与氢氧化钠反应的盐酸为y,与碳酸钠反应的盐酸为z,生成二氧化碳为n
Na2CO3+2HCl=2NaCl+H2O+CO2↑;NaOH+HCl=NaCl+H2O
106 73 44 80 36.5
5.3g z×7.3% n 4.0g y×7.3% =
解得:z=50g,y=50g,n=2.2g;
由图盐酸优先与氢氧化钠反应,后与碳酸钠反应,所以图示为
相关试卷
这是一份2022年广东省深圳市中考化学模拟卷(word版含答案),共5页。试卷主要包含了下列过程中发生化学变化的是,94,李兰娟院士的研究团队发现,下列实验方案错误的是等内容,欢迎下载使用。
这是一份2022年广东省深圳市中考模拟化学试卷10 (word版含答案),共9页。试卷主要包含了单项选择 I,单项选择 II,非选择题等内容,欢迎下载使用。
这是一份2022年广东省深圳市中考模拟化学试卷7 (word版含答案),共10页。试卷主要包含了单项选择 I,单项选择 II,非选择题等内容,欢迎下载使用。









