

所属成套资源:2020年上海各区高考一模化学(含答案)-word精校版
2020年上海市嘉定区高考一模化学试卷(含答案)
展开
这是一份2020年上海市嘉定区高考一模化学试卷(含答案),共9页。试卷主要包含了12, 符号“2p”没有给出的信息是, 下列烷烃命名错误的是, 下列制绿矾的方法最适宜的是等内容,欢迎下载使用。
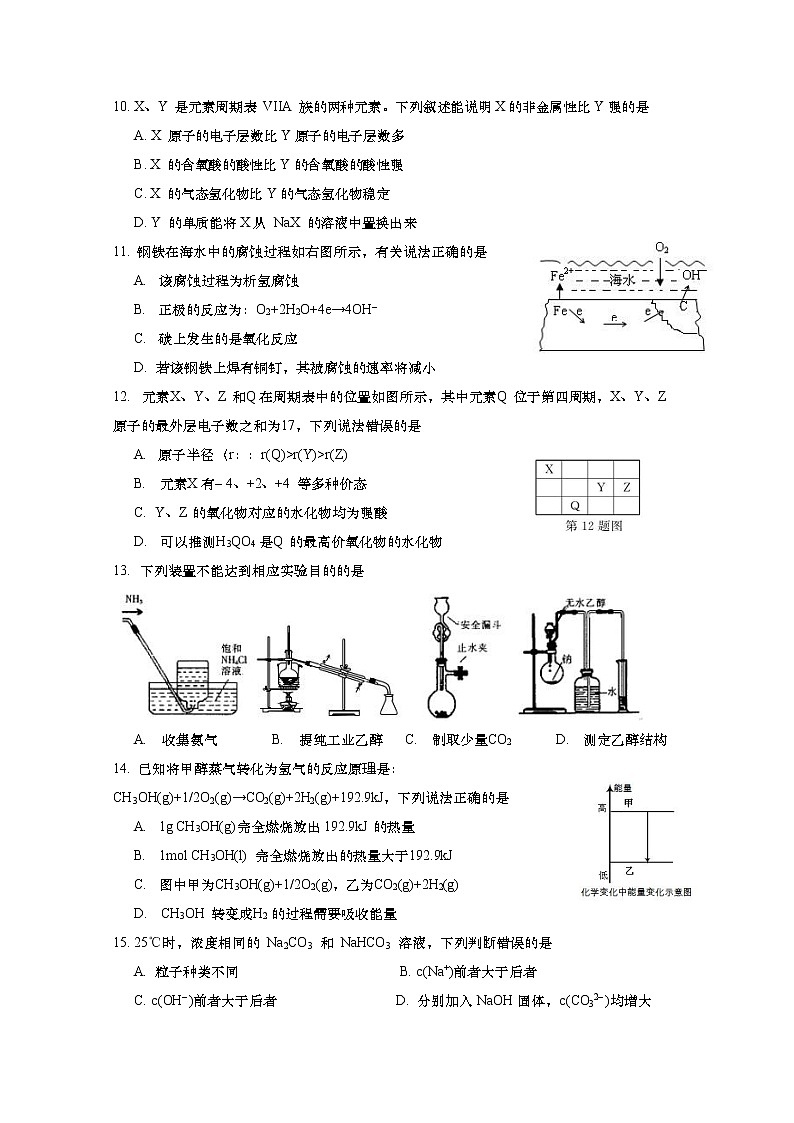
嘉定区2019~2020年度第一学期高中等级考模拟质量调研高三年级化学学科试卷 2019.12相对原子质量:H– 1 C– 12 N– 14 O– 16 S– 32 I– 127 Cu– 64一、 选择题(本题共40分,每小题2分,每题只有一个正确选项)1. 下列关于氯气性质的描述错误的是A. 无色气体 B. 能溶于水 C. 有刺激性气味 D. 光照下与氢气反应2. 符号“2p”没有给出的信息是A. 能级 B. 电子层 C. 电子亚层 D. 电子云在空间的伸展方向3. 下列烷烃命名错误的是A. 2– 甲基戊烷 B. 3– 乙基戊烷 C. 3,4– 二甲基戊烷 D. 3– 甲基己烷4. 同位素常用做环境分析指示物,下列对同位素的说法正确的是A. 34S 原子核内的中子数为 16 B. 16O 与 18O 的核电荷数相等C. 13C 和 15N 原子核内的质子数相差 2 D. 2H+质量与 1H+的质量相同5. 具有下列电子排布式的原子中,半径最大的是A. 1s22s22p63s23p1 B. 1s22s22p3 C. 1s22s22p2 D. 1s22s22p63s23p46. 某晶体中含有极性键,关于该晶体的说法错误的是A. 不可能有很高的溶沸点 B. 不可能是单质C. 可能是有机物 D. 可能是离子晶体7. 配制一定物质的量浓度的溶液时,要用到下列仪器中的 A. B. C. D. 8. 下列制绿矾的方法最适宜的是A. FeO与稀 H2SO4 B. Fe屑与稀 H2SO4C. Fe(OH)2 与稀 H2SO4 D. Fe2(SO4)3 与 Cu粉9. 下列离子能大量共存的是A. H+、AlO2–、CO32– B. K+、Ba2+、SO42–C. NH4+、OH–、NO3– D. Fe3+、NO3–、Cl– 10. X、Y 是元素周期表 VIIA 族的两种元素。下列叙述能说明X的非金属性比Y强的是A. X 原子的电子层数比Y原子的电子层数多 B. X 的含氧酸的酸性比Y的含氧酸的酸性强 C. X 的气态氢化物比Y的气态氢化物稳定D. Y 的单质能将X从 NaX 的溶液中置换出来11. 钢铁在海水中的腐蚀过程如右图所示,有关说法正确的是A. 该腐蚀过程为析氢腐蚀B. 正极的反应为:O2+2H2O+4e→4OH– C. 碳上发生的是氧化反应D. 若该钢铁上焊有铜钉,其被腐蚀的速率将减小12. 元素 X、Y、Z 和 Q在周期表中的位置如图所示,其中元素 Q 位于第四周期,X、Y、Z 原子的最外层电子数之和为 17,下列说法错误的是A. 原子半径(r)::r(Q)>r(Y)>r(Z)B. 元素 X有– 4、+2、+4 等多种价态C. Y、Z 的氧化物对应的水化物均为强酸D. 可以推测 H3QO4 是 Q 的最高价氧化物的水化物13. 下列装置不能达到相应实验目的的是A. 收集氨气 B. 提纯工业乙醇 C. 制取少量 CO2 D. 测定乙醇结构14. 已知将甲醇蒸气转化为氢气的反应原理是:CH3OH(g)+1/2O2(g)→CO2(g)+2H2(g)+192.9kJ,下列说法正确的是A. 1g CH3OH(g)完全燃烧放出192.9kJ 的热量B. 1mol CH3OH(l) 完全燃烧放出的热量大于 192.9kJC. 图中甲为 CH3OH(g)+1/2O2(g),乙为 CO2(g)+2H2(g) D. CH3OH 转变成 H2 的过程需要吸收能量15. 25℃时,浓度相同的 Na2CO3 和 NaHCO3 溶液,下列判断错误的是A. 粒子种类不同 B. c(Na+)前者大于后者C. c(OH– )前者大于后者 D. 分别加入NaOH固体,c(CO32– )均增大16. 将 1mol H2(g)和 2mol I2(g)置于某2L密闭容器中,在一定温度下发生如下反应,并达到平衡:H2(g)+I2(g)2HI(g)+Q(Q>0)HI 的体积分数 HI%随时间变化如曲线(I)所示,若改变反应条件,HI%的变化如曲线(II)所示,则改变的条件可能是A. 恒温条件下,加入适当催化剂B. 恒温条件下,缩小反应容器体积C. 恒容条件下升高温度D. 恒温条件下,扩大反应容器体积17. 布洛芬片常用来减轻感冒症状,其结构简式如图,有关说法错误的是A. 布洛芬的分子式为 C13H18O2 B. 布洛芬与苯乙酸是同系物C. 1mol 布洛芬最多能与 3mol 氢气发生加成反应D. 布洛芬在苯环上发生取代反应,其一氯代物有 4 种18. 某无色溶液含有 Na+、Fe3+、Cl– 、SO42– 中的 2种离子,分别取该溶液进行了下列实验:(1)向溶液中滴加用硝酸酸化的 AgNO3 溶液,有白色沉淀产生;(2)向溶液中滴加 Ba(NO3)2 溶液,没有任何现象。根据上述实验,可以确定溶液中一定存在的离子是A. Fe3+和 Cl– B. Na+和 SO42– C. Fe3+和SO42– D. Na+和 Cl–19. 有关硫酸铜晶体中结晶水含量测定的操作正确的是 A. 实验方案仅设计为:称量、加热、冷却、再称量 B. 称取一定量的胆矾,放在铁坩埚中进行加热C. 加热到蓝色完全变白,然后把坩埚移至干燥器中冷却D. 进行恒重操作,直至连续两次称量的结果相差不超过 0.01g 为止20. 某温度下,关于 pH 相等的盐酸和醋酸溶液(两溶液的 OH– 浓度也相等),下列说法正确的是A. c(HCl)>c(CH3COOH) B. c(Cl– )=c(CH3COO– )C. 等体积的盐酸和醋酸溶液分别与足量的 Zn 完全反应,盐酸产生的 H2 多D. 用同浓度的 NaOH 溶液分别与等体积的盐酸和醋酸溶液恰好反应完全,盐酸消耗的 NaOH 溶液体积多
二、 综合分析题(60 分)(一)(本题15 分)氧族元素的单质及其化合物对人类的生活、生产有着举足轻重的影响。 如氧气、水、二氧化硫等。21. 氧族元素原子最外层电子数与次外层中 p 亚层电子数相同的元素名称是_______________;硫单质常见形式是 S8,它的摩尔质量是______________;Se是人体不可或缺的微量元素,它在周期表中的位置是__________________,Se 原子最外层轨道表示式_____________________。 22. 在氧、硫、硒(Se)、碲(Te)元素原子形成的简单阴离子中,其离子半径由大到小的顺序为______________________________(用离子符号表示)。用化学方程式表示SO2形成硫酸型酸雨的反应___________________________________________________________________________。 23. 氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是_______A. 氧族元素气态氢化物的稳定性按 H2O、H2S、H2Se、H2Te 的顺序依次减弱B. 其氢化物中的键长按 O—H、S—H、Se—H、Te—H 的顺序依次减小C. 其阴离子的还原性按 O2–、S2–、Se2–、Te2–的顺序依次增强D. 其最高价氧化物的水化物酸性按 H2SO4、H2SeO4、H2TeO4顺序依次增强 24. 亚硫酸钠和碘酸钾在酸性溶液里反应生成硫酸钠、硫酸钾、碘和水 _____Na2SO3+_____KIO3+_____H2SO4 → _____Na2SO4+_____K2SO4+_____I2+_____H2O 配平该反应,若反应中有 0.5mol 电子转移,则生成的碘是_________g 25. 从右图可知氧族元素氢化物的沸点变化规律是______________________________________________________________________。
(二)(本题共 15 分)乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用 a 装置来制备。 完成下列填空:26. a 装置中玻璃仪器除导管和试管外还有_________________________________________仪器。27. 实验时,通常加入过量的乙醇,原因是:___________________________________________。加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是:_____________________________________________________, 浓硫酸用量又不能过多,原因是___________________________________________________________________________________________________________。28. 饱和Na2CO3溶液的作用是_______________________________________________________。29. 反应结束后,将试管中收集到的产品倒入分液漏斗中,_______________、______________,然后分液。这样得到的乙酸乙酯是粗产品,要进一步提纯精制,通常先用饱和食盐水洗涤除去少量Na2CO3溶液,再用饱和CaCl2溶液除去少量_________________________。30. 若用b装置制备乙酸乙酯,其缺点有______________________________________________、______________________________________________。
(三)(本题共 15 分) 已知在催化剂存在条件下,能发生如下反应:CO + H2O H2 +CO2 + Q(Q>0)31. 该反应的平衡常数表达式为:________________。在5 L盛有固体催化剂(其体积可忽略不计)的密闭容器中,通入反应物,10 s 后,生成了氢气 0.4 g,则此 10 s内 CO的平均反应速率为 v(CO) =___________________________。 32. 在该密闭容器中,下列叙述可以说明反应已经达到平衡状态的是____________。A. 若容器体积不变,在一定温度下压强达到恒定B. CO2的生成速率与 H2O 蒸气的生成速率之比为 1 : 1C. CO、H2O、H2、CO 在容器中的物质的量浓度保持不变D. 反应体系中混合物的平均摩尔质量保持不变33. 在上述反应达平衡状态后,分别改变条件,请完成下列两张图:A.在第 20 s 时将容器体积缩小至原来的一半后压强变化图B.在第 20 s 时,向容器中注入少量的CO 气体后正逆反应速率变化图34. 某化学小组在做澄清石灰水导电性实验时,发现石墨两极产生气体,溶液出现白色浑浊,请根据已有知识推测,两极产生的气体可能是_____________,白色浑浊是______________。为验证白色浑浊物的成分,该同学向白色浑浊液体中加入盐酸,没有观察到气泡产生。他们继续实验,将浑浊的液体倒入密闭容器,通过注射器注入稀盐酸,并用二氧化碳传感器来测定装置中二氧化碳含量的变化,装置和图像如下图所示: 请解释上述现象并分析产生白色浑浊可能的原因_____________________________________________________________________________________________________________________________。(四)(本题共 15分) 根据图示回答第 35—40 题:35. 写出E的名称_____________________,G的结构简式______________________________。36. 反应条件Ⅱ的试剂_____________________,反应的类型:___________________________。37. 反应②的化学方程式(包括反应条件)是__________________________________________________________________________________。38. F和G反应有许多副产物,写出两种主要的副产物的结构简式: ________________________________________,________________________________________。39. 将大量的A通入浓溴水中,观察到的实验现象是:____________________________________________________________,获取生成有机物的方法是:_________________(填操作名称)。40. F是一种重要的工业原料,利用它可制得多种有机物质。请完成由一氯乙烷合成F的路线图 (合成路线常用的表示方法为:)
嘉定区2019~2020年度第一学期高中等级考模拟质量调研高三年级化学学科试卷参考答案 一、 选择题12345678910ADCBAADBDC11121314151617181920BCACACDDCB 二、综合分析题 (一)(本题共 15 分)21.(4 分)硫等 256g/mol 第四周期VIA族(只写周期或族不得分) 4S 4P22.Te2– > Se2– > S2– > O2–(2 分)SO2+ H2O H2SO3 2H2SO3+O22H2SO4(2 分)23. AC (2 分,漏选一个得 1 分,错选不得分)24.5,2,1,→ 5,1,1,1(2 分),12.7g(1 分)(共 3 分)25.除水外,随着氢化物的相对分子质量增大而沸点也升高(2分) (二)(本题共 15 分)26. 酒精灯、干燥管、烧杯(2 分)27. 增大反应物浓度,使平衡向生成酯的方向移动,提高酯的产率,增大乙酸转化率(合理即给分)(2 分) 浓 H2SO4 能吸收生成的水,使平衡向生成酯的方向移动,提高酯的产率。(2 分) 浓 H2SO4 具有强氧化性和脱水性,会使有机物碳化,降低酯的产率。(1 分) 28. 中和乙酸、溶解乙醇、减少乙酸乙酯在水中的溶解度(3 分)29. 振荡、静置,乙醇(3 分)30. 原料损失较大、易发生副反应(2 分)
(三)(本题共 15 分)31. K = ; 0.002 mol/(L.s)32.BC(2 分,漏选一个得 1 分,错选不得分)33. 34. (3 分)H2和O2,碳酸钙(碳酸钙必写,氢氧化钙可写可不写) 澄清石灰水浓度小,产生碳酸钙的量少,滴加稀盐酸后产生的二氧化碳也很少,二氧化碳能溶于水,故无法观察到明显气泡。二氧化碳传感器表明随着反应的进行,二氧化碳的量在增加,证明白色浑浊物是碳酸 钙。阳极产生的氧气与石墨电极中的碳反应,生成二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙,出现白色浑浊。(2 分) (四)(本题共 15 分)35. 聚氯乙烯(1 分)36. NaOH 水溶液,加热(1 分)取代反应(1 分) 37. 38. (2 分)或其他合理答案39. 溴水褪色,溶液分层,上层无色,下层油状液体(2 分)分液(1 分)40.(4 分)试剂 3分条件 1 分
相关试卷
这是一份2022年上海市嘉定区高考化学二模试卷(等级考),共33页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份2021年上海市嘉定区高考化学二模试卷,共34页。试卷主要包含了选择题,综合题等内容,欢迎下载使用。
这是一份2023年上海市嘉定区高考二模化学答案,共2页。试卷主要包含了选择题,综合分析题等内容,欢迎下载使用。









