




浙教版九年级上册第2节 物质的酸碱性课文内容课件ppt
展开电离时生成的阳离子全部都是氢离子的化合物
HCl 、H2SO4、HNO3、H2CO3、醋酸等
电离时生成的阴离子全部都是氢氧根离子的化合物
NaOH、Ca(OH)2、KOH、Ba(OH)2 、NH3·H2O等
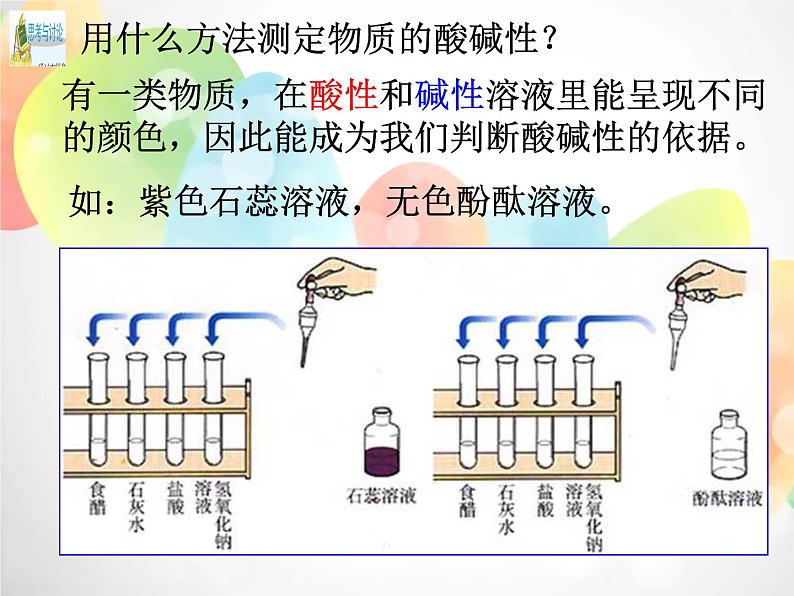
用什么方法测定物质的酸碱性?
有一类物质,在酸性和碱性溶液里能呈现不同的颜色,因此能成为我们判断酸碱性的依据。
如:紫色石蕊溶液,无色酚酞溶液。
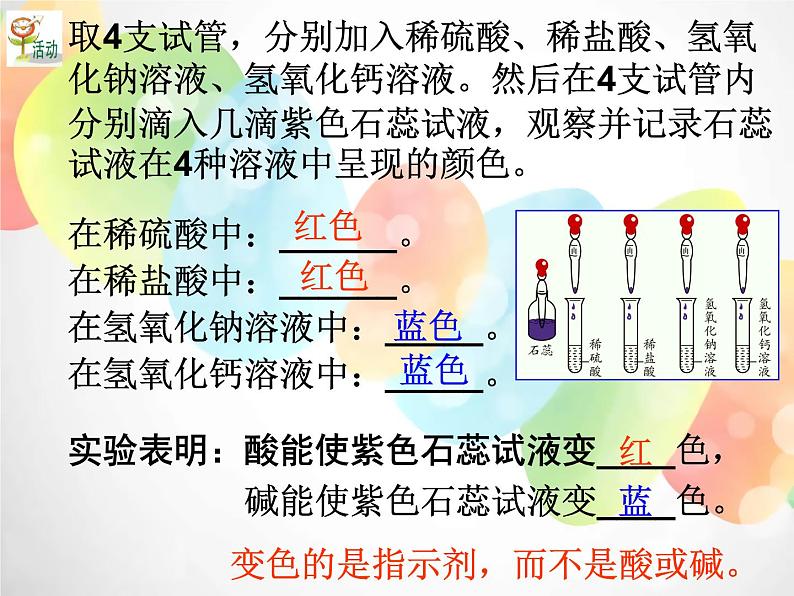
取4支试管,分别加入稀硫酸、稀盐酸、氢氧化钠溶液、氢氧化钙溶液。然后在4支试管内分别滴入几滴紫色石蕊试液,观察并记录石蕊试液在4种溶液中呈现的颜色。
在稀硫酸中:______。在稀盐酸中:______。在氢氧化钠溶液中:_____。在氢氧化钙溶液中:_____。
实验表明:酸能使紫色石蕊试液变____色, 碱能使紫色石蕊试液变____色。
变色的是指示剂,而不是酸或碱。
在酸性或碱性溶液里能显示出不同颜色的物质,叫做酸碱指示剂,通常简称指示剂。
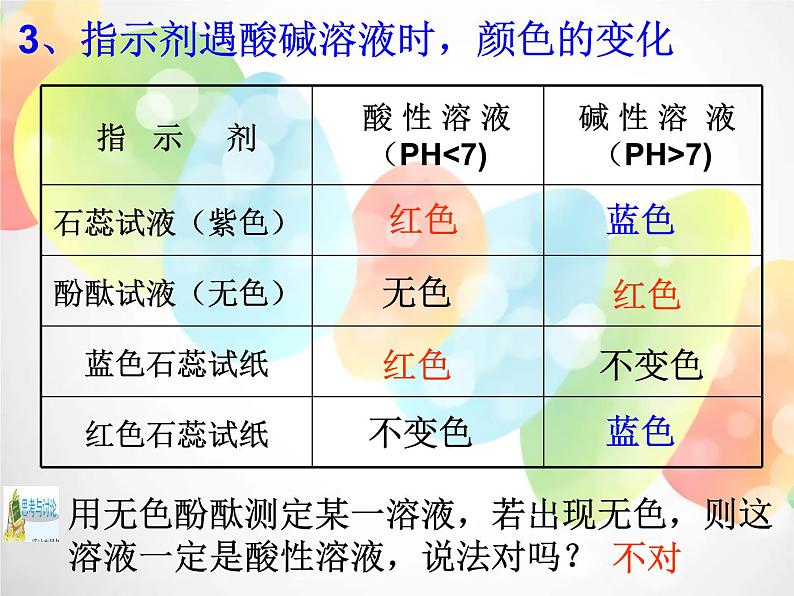
3、指示剂遇酸碱溶液时,颜色的变化
用无色酚酞测定某一溶液,若出现无色,则这溶液一定是酸性溶液,说法对吗?
三、溶液酸碱性的强弱程度
1、测定溶液酸碱性强弱的意义
土壤的酸碱性的强弱对农作物生长有很大的影响。所以,测定土壤的酸碱性非常必要。
土地的盐碱化使土壤碱性增强。
碱性土壤会腐蚀农作物并板结成块。草木难生。
一般的雨水具有微弱的酸性,但有些地方由于工业废气的过量排放,雨水酸性过强,形成酸雨。
2、物质酸碱性强弱的测定
pH是反映物质酸碱性强弱的指标。
范围通常在 0 ~14 之间。
pH越低,酸性越强;pH越高,碱性越强;
pH小于7 的呈酸性;pH大于7 的呈碱性。
测定物质酸碱性强弱最常用、最简单的方法是使用pH试纸。
pH试纸在酸碱性强弱不同的溶液里会显示出不同的颜色。
1、用洁净的玻璃棒蘸取被测试的溶液;
3、将试纸显示的颜色与标准比色卡对照;
4、看与哪种颜色最接近,从而确定溶液的pH。
1.用玻璃棒分别蘸取少许水、柠檬汁、白醋、盐酸、肥皂水、洗涤剂、4% 氢氧化钠溶液,滴在 pH 试纸中部,观察试纸的颜色变化。
2.在白色点滴板的空穴(或小试管)里分别滴入几滴上述样品,再滴加2~3滴紫色石蕊试液,观察其颜色的变化,并将上述实验结果都填入表1-3中。
表1—3 实验过程中物质的颜色变化
你能得出什么结论? __________________________ ___________________________________________。
不同物质酸碱性的强弱程度不同;
pH试纸显示酸碱性的强弱程度,而酸碱指示剂只能指示酸碱性
用pH试纸测试溶液酸碱性强弱需要注意哪些问题?
1、试纸不可直接伸入溶液中。
2、不能先用蒸馏水将pH试纸润湿。
(因为润湿试纸相当于稀释被检测的溶液, 这会导致检测不准确)
用pH试纸测试溶液与红蓝石蕊试纸测试溶液有什么不同?
pH试纸能显示酸碱性的强弱(定量测定酸碱度),而红蓝石蕊试纸则只能指示溶液是否显酸性或碱性(定性测定酸碱性)。
用pH试纸测试的方法比较粗略。
精确的测试可使用一种称为酸度计的仪器。
用pH试纸测试溶液酸碱性的方法有什么缺点?
酸、碱溶液分别与水混合时,pH的变化规律:
许多植物的花、果、茎、叶中都含有某些显色的物质,它们在酸性溶液或碱性溶液里会显示不同的颜色。如果你有兴趣,可以取这些植物的花、果、茎、叶切碎捣烂,用酒精浸制,所得的浸出液可以作为酸碱指示剂,如表 1-2所示。
我们生活中一些物质的pH
pH 是定量反映物质酸碱性强弱的重要指标,它与我们的生活密切相关。
人体血液的pH为7.39 ~ 7.45。当血液的 pH降到7.0以下或升到7.8以上时,人就有生命危险。人处在通风不良的环境中时间过长,吸入的二氧化碳过多,血液中二氧化碳的含量增大,酸性就会增强,从而引起恶心、头晕等症状。
人的汗液的pH大约为5.5~6.6。洗衣皂、香皂、药皂的pH也有所不同。洗衣皂的pH高,碱性强,适用于洗衣物 ;香皂、药皂的pH低,适用于洗脸、洗澡。
牛奶的pH 通常小于 7,酱油的pH 为4.8 左右,番茄的pH ≤ 4.5。生鲜肉的pH为7.0 ~ 7.4 之间,生肉久放后,由于肉中蛋白质凝固,失去一些水分,pH变为5.4~5.5。食用醋酸的pH为3左右,因为酸性 环境可抑制细菌的繁殖,所以人们喜欢在一些食物中加入少许食用醋酸,这样既能使食品不易变质,又可增加风味。
土壤的酸碱性的强弱对农作物生长有很大的影响,各种农作物对pH有一定的适应 性。一般来说,中性土壤最适宜于微生物生长繁殖,有利于土壤中有机质向有效养分转化,促进农作物生长。pH为4 ~6 的土壤会使农作物根系发黑;pH为8以上的土壤会腐蚀农作物并板结成块。盐碱地的pH多在9以上,草木难生。
科学浙教版第2节 物质的酸碱性教案配套课件ppt: 这是一份科学浙教版第2节 物质的酸碱性教案配套课件ppt,共13页。PPT课件主要包含了不变色,酸碱指示剂,判断物质的酸碱性,pH试纸,最简单的方法,标准比色卡,PH试纸,使用方法,玻璃棒,pH值等内容,欢迎下载使用。
初中科学浙教版九年级上册第2节 物质的酸碱性精品课件ppt: 这是一份初中科学浙教版九年级上册第2节 物质的酸碱性精品课件ppt,共23页。PPT课件主要包含了是酸的吗,想一想,动手试一试,动动脑动动脑,pH56的降水,想一想想一想等内容,欢迎下载使用。
初中科学浙教版九年级上册第6节 电能备课课件ppt: 这是一份初中科学浙教版九年级上册第6节 电能备课课件ppt,共13页。PPT课件主要包含了纯电阻等内容,欢迎下载使用。













