



2022安庆示范高中高三下学期4月联考试题理综化学含答案
展开2022年安庆市示范高中高三联考试题
理科综合能力测试(化学)
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 C12 O16 F19 Na 23 Mg 24 P 31 S32 Cl 35.5 Ti 48Se 79 Cd 112 Ce 140
一、选择题:本题共7小题,每题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
7.2022年北京冬奥会是我国提出“2030年前实现碳达峰、2060年实现碳中和”目标后的首个世界级的体育盛会。下列冬奥会中使用的新科技、新材料与促进“碳达峰、碳中和”无关的是
A.聚乳酸制作可降解餐具 B.氢气代替丙烷作为火炬燃料
C.二氧化碳跨临界直冷技术制冰 D.风力发电和光伏发电为奥运场馆提供电力供应
8.设NA为阿伏加德罗常数的值,下列说法错误的是
A.常温常压下,11.2g乙烯中共用电子对数目为2.4NA
B.0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA
C.120g MgSO4和NaHSO4的固体混合物中含有阳离子的总数为NA
D.将1mol NH4NO3溶于适量稀氨水,所得溶液呈中性,则溶液中的NH4+数目为NA
9.氯吡格雷是抑制血小板聚集的药物,其结构简式如图所示。下列有关该物质的叙述正确的是
A.分子式为C16H15ClNO2S
B.所有碳原子一定可以共平面
C.既可以发生水解反应又可以发生消去反应
D.1mol该物质最多可与5molH2发生加成反应
10.下列有关实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向某白色晶体中滴加几滴浓硫酸, 将湿润的品红试纸靠近试管口 | 产生的无色气体使试纸变白 | 该晶体中一定含有SO32- |
B | 向5mL0.1mol·L-1KI溶液中加入 10mL 0.1mol·L-1FeCl3溶液, 充分反应后滴加KSCN溶液 | 溶液变红 | I-与Fe3+的反应是可逆反应 |
C | 常温下,用pH计测量0.1mol·L-1 NH4CN溶液的pH | pH=8.6 | 电离平衡常数: Kb(NH3·H2O)>Ka (HCN) |
D | 取一支试管装入2mL2mol·L-1NaOH溶液,先滴入1mL1mol·L-1MgCl2溶液,再滴入几滴1mol·L-1CuCl2溶液 | 先生成白色沉淀,后沉淀变为蓝色 | Ksp[Cu(OH)2]>Ksp(Mg(OH)2) |
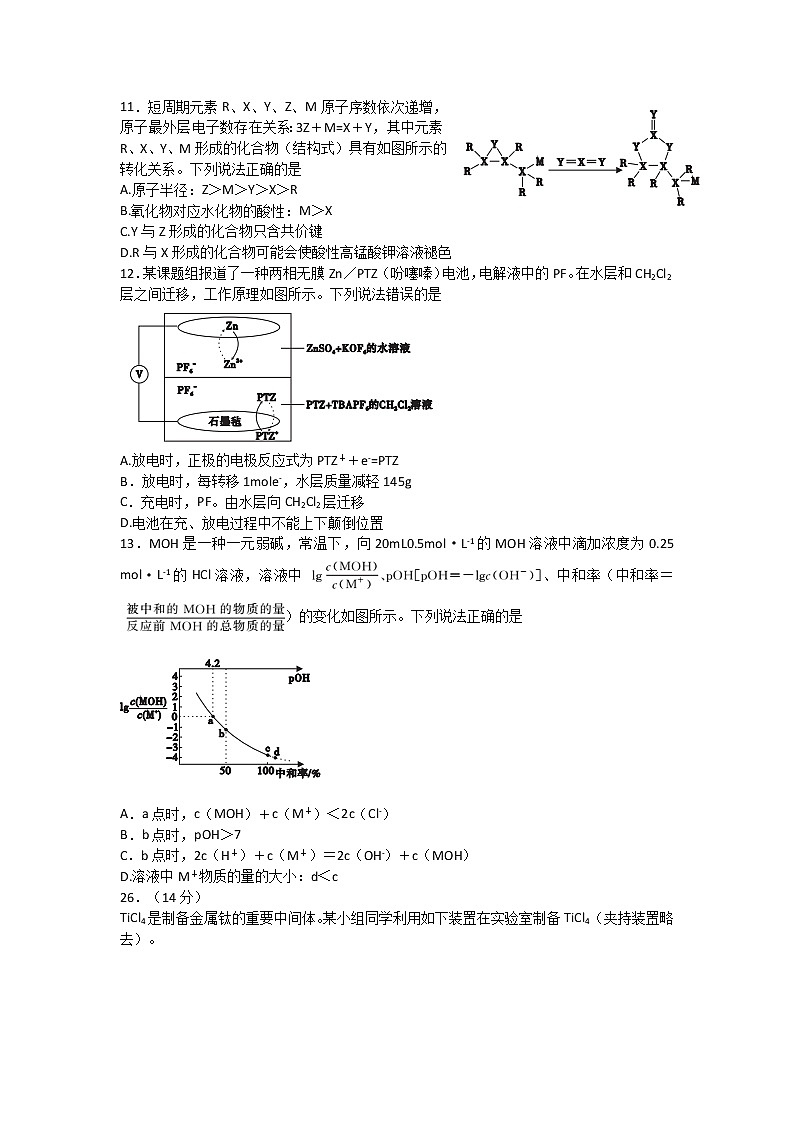
11.短周期元素R、X、Y、Z、M原子序数依次递增,原子最外层电子数存在关系:3Z+M=X+Y,其中元素R、X、Y、M形成的化合物(结构式)具有如图所示的转化关系。下列说法正确的是
A.原子半径:Z>M>Y>X>R
B.氧化物对应水化物的酸性:M>X
C.Y与Z形成的化合物只含共价键
D.R与X形成的化合物可能会使酸性高锰酸钾溶液褪色
12.某课题组报道了一种两相无膜Zn/PTZ(吩噻嗪)电池,电解液中的PF。在水层和CH2Cl2层之间迁移,工作原理如图所示。下列说法错误的是
A.放电时,正极的电极反应式为PTZ++e-=PTZ
B.放电时,每转移1mole-,水层质量减轻145g
C.充电时,PF。由水层向CH2Cl2层迁移
D.电池在充、放电过程中不能上下颠倒位置
13.MOH是一种一元弱碱,常温下,向20mL0.5mol·L-1的MOH溶液中滴加浓度为0.25 mol·L-1的HCl溶液,溶液中、中和率(中和率=)的变化如图所示。下列说法正确的是
A.a点时,c(MOH)+c(M+)<2c(Cl-)
B.b点时,pOH>7
C.b点时,2c(H+)+c(M+)=2c(OH-)+c(MOH)
D.溶液中M+物质的量的大小:d<c
26.(14分)
TiCl4是制备金属钛的重要中间体。某小组同学利用如下装置在实验室制备TiCl4(夹持装置略去)。
已知:TiCl4易挥发,高温时能与O2反应,不与HCl反应,其他相关信息如下表所示:
| 熔点/℃ | 沸点/℃ | 密度/(g·cm-3) | 水溶性 |
TiCl4 | -24 | 136.4 | 1.7 | 易水解生成白色沉淀,能溶于有机溶剂 |
CC14 | -23 | 76.8 | 1.6 | 难溶于水 |
回答下列问题:
(1)A装置仪器b的名称是 ,E装置中的试剂是 。
(2)装置A中发生反应的离子方程式为
(3)在通入Cl2前,先打开开关k,从侧管持续通入一段时间的CO2气体的目的是
(4)装置C中除生成TiCl4外,还生成一种气态不成盐氧化物,该反应的化学方程式为
(5)制得的TiCl4中常含有少量CCl4,从混合液中分离出TiCl4操作的名称是
(6)利用如右图装置测定所得TiCl4的纯度:取wg产品加入烧瓶,向安全漏斗中加入适量蒸馏水,待TiCl4充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴0.1mol·L-1K2CrO4溶液作指示剂,用cmol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液VmL。
已知:常温下,Ksp(AgC1)=1.8×10-10、Ksp(Ag2CrO4)=1.1×10-12,Ag2CrO4呈砖红色,TiCl4+(2+n)H2O=TiO2·nH2O ↓+4HC1
①安全漏斗在本实验中的作用除加水外,还有 ;
②滴定终点的判断方法是 ;
③产品的纯度为 (用含w、c和V的代数式表示)。
27.(14分)
二氧化铈(CeO2)可用作玻璃工业添加剂和有机反应催化剂。以氟碳铈矿(主要含有CeFCO3)为原料制备二氧化铈的一种工艺流程如图:
已知:①Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF6-;②Ce4+能被萃取剂TBP萃取,而Ce3+不能。回答下列问题:
(1)“氧化焙烧”时,为了加快反应速率、提高原料利用率的措施有 。(写一种,合理即可)
(2)“氧化焙烧”后的固体产物中含有CeO2和CeF4,二者物质的量之比为3:1,“酸浸”时发生反应的离子方程式为
(3)TBP是一种有机萃取剂,“萃取”时发生反应:CeF3++TBP→CeTBP4++F-,氟洗液中添加A13+的作用是
(4)“反萃取”时加入H2SO4和H2O2的混合液,H2O2的作用为
(5)“反萃取”后的水层溶液中c(Ce3+)=1mol·L-1,c(Al3+)=0.01mol·L-1。室温下,“调pH”时,先除去Al3+,若忽略过程中溶液的体积变化,则需加入NaOH调节溶液pH的范围为 ,过滤后,再向滤液加入NaOH使Ce3+沉淀完全(已知:室温下,当溶液中的离子浓度c≤1.0×10-5mol·L-1时,可认为该离子沉淀完全。K[Al(OH)3]=1.0×10-32,K[Ce(OH)3]=1.0×10-21)。
(6)“氧化”时发生反应的化学方程式为
(7)用10吨含70%CeFCO3的矿石,按上述工艺生产,制得CeO24.48吨,则CeO2的产率为 (保留三位有效数字)。
28.(15分)
合成气(CO和H2)是一种重要的化工原料气,可以合成甲酸甲酯、二甲醚等化工产品,合成气的制备具有重要的研究价值。回答下列问题:
I.催化分解法
(1)催化剂作用下,用甲醇制备合成气的反应为CH3OH(g)=CO(g)+2H2(g)ΔH>0,理论上欲提高甲醇的平衡转化率,适宜采用的措施是 (填标号)。
A.高温高压 B.低温高压 C.高温低压 D.低温低压
(2)科研发现,在钯催化剂作用下,甲醇制备合成气的反应历程如图所示(吸附在钯催化剂表面上的物种用*标注)。
该历程中,最大能垒(活化能)为 kJ·mol-1,放热最多步骤的化学方程式为
II.自热重整法
甲烷、二氧化碳自热重整制合成气发生的反应主要有:
i.CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH1
ii.H2(g)+CO2(g)==CO(g)+H2O(g) ΔH2=+41kJ·mol-1
(3)已知部分化学键的键能数据如下表:
化学键 | C-H | H-H | C=O | C=O(CO) |
键能/kJ·mol-1 | 413 | 436 | 803 | 1076 |
则ΔH1= kJ·mol-1。
(4)将1molCH4与1mol CO2在2L密闭容器中反应制取CO和H2时,CH4和CO2的平衡转化率随温度的变化如图所示。
①代表CO2平衡转化率随温度变化的曲线是 (填“A”或“B”)。
②计算923K时反应i的化学平衡常数K= (计算结果保留小数点后2位)。
③1200K以上CH4和CO2的平衡转化率趋于相等的原因可能是
III.电解转化法
(5)我国科学家设计了一种电解装置,能将二氧化碳转化为合成气,同时获得甘油醛,装置如图所示。
①催化电极a应与电源 (填“正”或“负”)极相连。
②催化电极b生成合成气的电极反应式为
35.[化学-选修3:物质结构与性质](15分)
Ge、GaAs、CdTe、CdSe等均为重要的半导体材料,在电子、材料等领域应用广泛。回答下列问题:
(1)Ge基态原子核外电子排布式为[Ar]
(2)第四周期主族元素中,第一电离能介于Ga、As之间的元素是 (填元素符号)。
(3)碲的化合物TeO2、TeO3、H2Te三种物质中,H2Te的中心原子杂化类型为 ,分子构型为V形的是
(4)GaCl3熔点为77.9℃,气体在270℃左右以二聚体存在,GaCl3二聚体的结构式为 。GaF3熔点为1000℃,GaCl3熔点低于GaF3的原因是
(5)CdSe的一种晶体为闪锌矿型结构,晶胞结构如图所示。
①原子坐标参数A为(),则B、C的原子坐标参数分别为 、
②已知Cd、Se的半径分别为anm和bnm,则CdSe的密度为 g·cm-3(列出计算表达式,NA表示阿伏加德罗常数的值)。
36.[化学-选修5:有机化学基础](15分)
美托拉宗是一种利尿药物,可以采用如下路线合成:
回答下列问题:
(1)A的化学名称为 。
(2)A→B反应的试剂和条件为 。
(3)C中含有官能团的名称为 。
(4)D的结构简式为 。
(5)F→G的反应类型为 。
(6)写出反应G→H的化学方程式 。
(7)化合物M是比化合物A相对分子质量大14的同系物。化合物M的芳香族同分异构体中,同时满足如下条件的有 种。其中核磁共振氢谱有5组峰,且峰面积之比为1:1:2:2:3的同分异构体的结构简式为 。
①能与碳酸氢钠溶液反应
②苯环只含有两个取代基
安徽省安庆市示范高中2023届高三下学期4月联考理综化学试题: 这是一份安徽省安庆市示范高中2023届高三下学期4月联考理综化学试题,共8页。
安徽省安庆市示范高中2023届高三化学下学期4月联考试题(Word版附解析): 这是一份安徽省安庆市示范高中2023届高三化学下学期4月联考试题(Word版附解析),共16页。试卷主要包含了本试卷分第I卷和第II卷两部分等内容,欢迎下载使用。
安徽省安庆市2023届高三下学期高考模拟(二模)理综化学试题: 这是一份安徽省安庆市2023届高三下学期高考模拟(二模)理综化学试题,共15页。试卷主要包含了单选题,实验题,工业流程题,原理综合题,有机推断题等内容,欢迎下载使用。












