






鲁教版九年级下册第二节 碱及其性质课堂教学课件ppt
展开1、通过观察氢氧化钠和氢氧化钙,记住它们的主要物理性质;通过实验,能认识到它们具有强烈的腐蚀性。2、通过实验探究氢氧化钠和氢氧化钙的化学性质与化学变化。会写氢氧化钠和氢氧化钙的化学性质中的有关化学方程式,记住相应的反应现象3、明白碱具有相似化学性质的原因及归纳碱的通性
虎门销烟是我国历史上著名的历史事件,林则徐用的是什么物质来硝烟的呢?你又看到了什么现象呢?
碱的定义:溶于水后解离出的阴离子全部是氢氧根离子(OH-)的化合物叫碱。NaOH、Ca(OH)2是最常用的两种碱。
【活动天地7-3】认识氢氧化钠和氢氧化钙各取适量固体氢氧化钠(NaOH)和氢氧化钙,分别放入两个小烧杯中。1.观察其颜色状态。
2.露置在空气一段时间后,再观察它们的颜色和状态的变化。
3.向两只小烧杯中分别加入少量水,振荡,观察它们的溶解情况。用手触摸烧杯 外壁。
4.把一根头发放入试管中,向试管里加入上述实验得到的氢氧化钠溶液,加热煮沸2--3min,观察头发的变化。
易溶于水(放出大量的热)
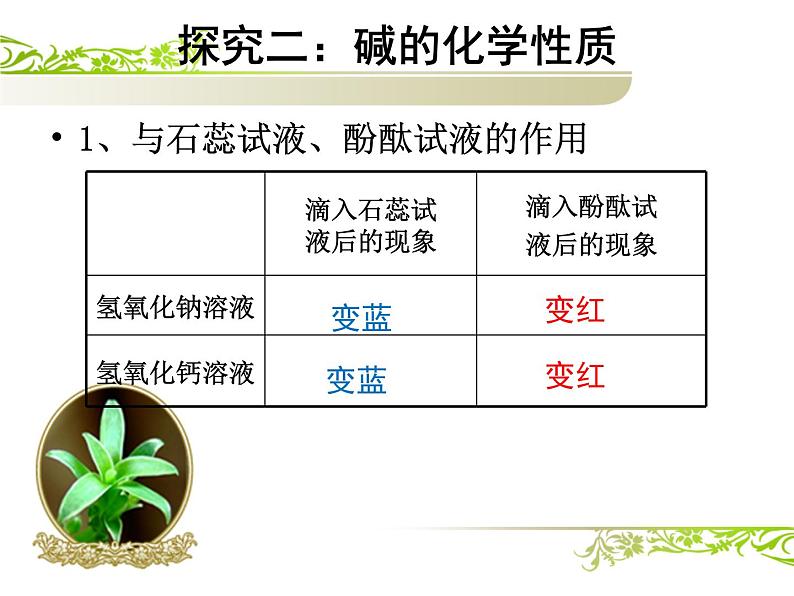
1、与石蕊试液、酚酞试液的作用
2NaOH+CuCl2 =
Ca(OH)2+CuCl2=
Ca(OH)2+Na2CO3=
2、氢氧化钠和氢氧化钙的化学性质
Cu(OH)2↓+2NaCl
Cu(OH)2↓+CaCl2
2NaOH+CaCO3↓
2NaOH+CO2=Na2CO3+H2O
Ca(OH)2+CO2 =CaCO3↓+H2O
思考:有的同学认为,“实验4中矿泉水瓶变瘪,不足以证明二氧化碳和氢氧化钠或氢氧化钙溶液发生了化学反应,因为二氧化碳溶解在水中也会产生类似的现象”。你同意这种观点吗?
方法指导:1.利用“二氧化碳气体被消耗,容器内外会形成压强差”的原理。设计对比实验,在使用此方法时,要注意控制变量。2.向反应后的溶液中滴加某种试剂检验生成物的存在。
方案⑴:分别向装满二氧化碳气体的两个塑料瓶中,倒入等量的氢氧化钠溶液和水振荡,观察塑料瓶变瘪的程度。
方案⑵:取少量通入二氧化碳气体的氢氧化钠溶液,加入适量的稀盐酸,若有气泡生成,说明二氧化碳与氢氧化钠反应了。
课本选取紫色石蕊试液、无色酚酞试液、二氧化碳、生锈铁钉、碳酸钠和氯化铜溶液来进行碱的性质探究,每一种具体物质背后代表的是哪类物质?你能总结出碱的通性吗?
(2)碱 + 非金属氧化物
(3)碱 + 盐
2NaOH+CuCl2=Cu(OH)2↓+2NaCl
Ca(OH)2+Na2CO3=2NaOH+CaCO3↓
(1)碱溶液都可以使紫色的石蕊变蓝、无色的酚酞变红。
Ca(OH)2+CuCl2=Cu(OH)2↓+CaCl2
(不溶性的碱在水中不会解离出氢氧根离子,不能使紫色石蕊试液和无色酚酞试液变色;并不是所有非金属氧化物都与碱反应。) 由于不同的碱溶于水时解离出的阳离子不同,其性质也存在差异。如: Ca(OH)2+Na2CO3=2NaOH+CaCO3↓
1.下列有关物质的名称、俗名、化学式中,三者皆指同一 物质的是 ( ) A.氧化钙、消石灰、CaO B.氯化氢、盐酸、HCl C.碳酸钙、熟石灰、CaCO3 D.氢氧化钠、烧碱、NaOH 2.下列物质与澄清的石灰水混合,观察不到明显现象的是( ) A.二氧化碳 B.氯化钙溶液 C.硫酸铜溶液 D.碳酸钠溶液
3.某同学为了区别氢氧化钠溶液和澄清石灰水,设计了如下图所示的四组实验方案,其中能达到目的的是( ) A. B. C. D.
4.固体氢氧化钠暴露在空气中易吸收_____而潮解,又能与_____反应而变质,所以需要密封保存。
5.实验室中有两瓶失去标签的无色溶液,已知其中一瓶是氢氧化钠溶液,一瓶为澄清石灰水,你用哪些方法可以将两者区分开?比比谁的方法多。
通过本节课的学习,你有哪些收获?1.知识方面:2.方法方面:
初中化学鲁教版九年级下册第二节 碱及其性质课文课件ppt: 这是一份初中化学鲁教版九年级下册第二节 碱及其性质课文课件ppt,共26页。PPT课件主要包含了常见的碱,碱的化学性质等内容,欢迎下载使用。
初中化学鲁教版九年级下册第二节 碱及其性质背景图课件ppt: 这是一份初中化学鲁教版九年级下册第二节 碱及其性质背景图课件ppt,共36页。PPT课件主要包含了生活体验,氢氧化钡,KOH,溶碱钾钠钡钙铵中寻,议一议,想一想等内容,欢迎下载使用。
2020-2021学年第二节 碱及其性质备课ppt课件: 这是一份2020-2021学年第二节 碱及其性质备课ppt课件,共14页。PPT课件主要包含了常见的碱,易溶于水溶解时放热,无变化不可做干燥剂,碱的化学性质,变蓝色,变红色,pH7,水蒸气,CO2,蓝色沉淀等内容,欢迎下载使用。













