




九年级化学复习 物质的鉴别 反应后溶液中溶质成分探究 优质课件
展开
这是一份九年级化学复习 物质的鉴别 反应后溶液中溶质成分探究 优质课件,共18页。PPT课件主要包含了NaCl,实验操作与实验安全,CaCl2,思维拓展,能力提升,牛刀小试,Na+,CO32,Ca2+等内容,欢迎下载使用。
反应一: Na2CO3 +CaCl2 2NaCl + CaCO3猜想反应后溶液中溶质的成分: 猜想一:(恰好完全反应) 猜想二:(Na2CO3 过量) 猜想三:(CaCl2 过量) 猜想四:(反应物都过量) NaCl、CaCl2 、Na2CO3
反应后溶液中溶质成分探究
NaCl、过量的Na2CO3
NaCl、过量的 CaCl2
注意:①规范操作,注意实验安全。 ②随时将实验环节和现象仔细记录。 ③分工明确,小组协同。 ④实验探究时长五分钟。
A B C D
猜想反应后溶液中溶质的成分: 猜想一:恰好完全反应—— 猜想二:反应物A过量—— 猜想三:反应物B过量——
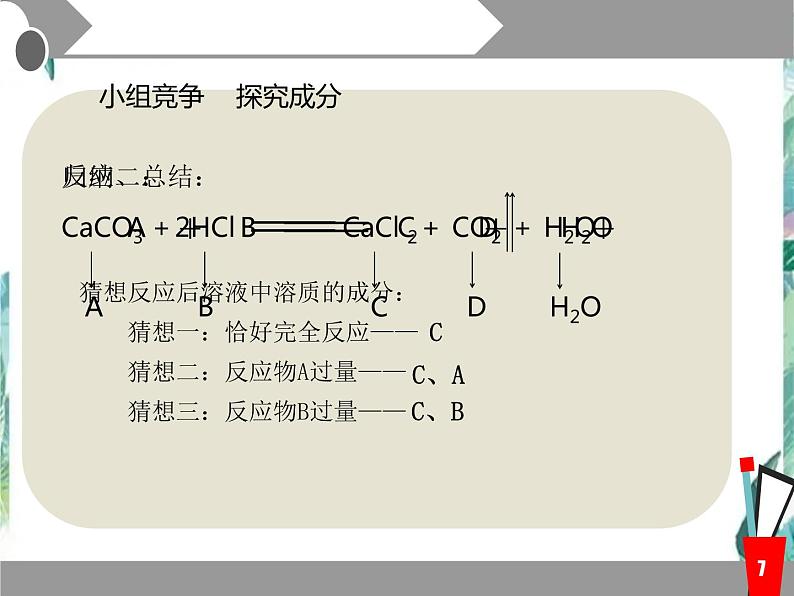
反应二: CaCO3 +2HCl CaCl 2+ CO2 + H2O猜想反应后溶液中溶质的成分: 猜想一:(恰好完全反应) 猜想二:(HCl过量) 猜想三:(CaCO3过量)
小组竞争 探究成分
CaCl 2 、过量的HCl
CaCl 2 、过量的 CaCO3
注意:①规范操作,注意实验安全。 ②随时将实验环节和现象,仔细记录。 ③分工明确,小组协同。 ④实验探究时长五分钟。
A B C D H2O
反应三: NaOH +HCl NaCl +H2O猜想反应后溶液中溶质的成分: 猜想一:(恰好完全反应) 猜想二:(NaOH过量) 猜想三:(HCl过量)
知识升华 知识拓展
NaCl 、过量的 NaOH
NaCl 、过量的HCl
A B C H2O
反应三: NaOH +HCl NaCl +H2O
滤液为无色澄清,硫酸铜溶液为蓝色。
【变式训练】 十八中的学生在做完用氢氧化钠溶液吸收二氧化碳气体后,想要探究吸收二氧化碳后溶液中溶质的成分。 1、请先提出合理猜想。 猜想一:氢氧化钠、碳酸钠 猜想二:碳酸钠 2、设计实验进行验证。
知识升华、思维拓展
补充实验探究: 如何证明NaOH 和HCl是否发生反应?思考:(1)化学反应的实质? (2)如何检验Cl— ? (3) Cl— 的来源?
猜想二:(Na2CO3 过量)NaCl、Na2CO3
1、稀盐酸2、氯化钙溶液 3、无色酚酞溶液
观察是否有气体产生。
观察是否有白色沉淀生成。
观察酚酞是否由无色变为红色。
猜想三:(CaCl2 过量)NaCl、 CaCl2
1、Na2CO3溶液(向反应后的溶液中加入Na2CO3溶液,观察是否生成白色沉淀。)
猜想二:(HCl过量) CaCl 2 、过量的HCl
1、紫色石蕊溶液、pH试纸。2、活泼金属。3、金属氧化物。4、难溶性碱。5、碳酸盐。6、可溶性碱+酚酞溶液。例:NaOH+酚酞。
观察到固体逐渐减少,得到有色溶液的现象。
观察到难溶性碱逐渐减少,溶液变为有色溶液。
观察溶液颜色是否由红色变为无色。
相关课件
这是一份专题07 反应后溶质成分的判断(复习课件)-2022年中考化学二轮复习讲练测,共24页。PPT课件主要包含了pH≤7,AgNO3,CuNO32等内容,欢迎下载使用。
这是一份九年级第一学期3.2 溶液多媒体教学ppt课件,共42页。PPT课件主要包含了学习目标,科学探究的一般环节,提出问题,设计实验及验证猜想,反思与评价,总结归纳,紫色石蕊,作出猜想,课堂小结,作出合理的猜想等内容,欢迎下载使用。
这是一份2023年中考化学二轮复习考点专题突破中和反应及反应后成分的探究课件,共30页。PPT课件主要包含了专题精讲,逐渐变浅,更充分,防止加入过量的稀盐酸,氢氧化钠已经变质,方法二pH变化法,pH=7,NaCl,HCl和NaCl,活泼金属如Fe等内容,欢迎下载使用。








