




初中1 酸及其性质图文ppt课件
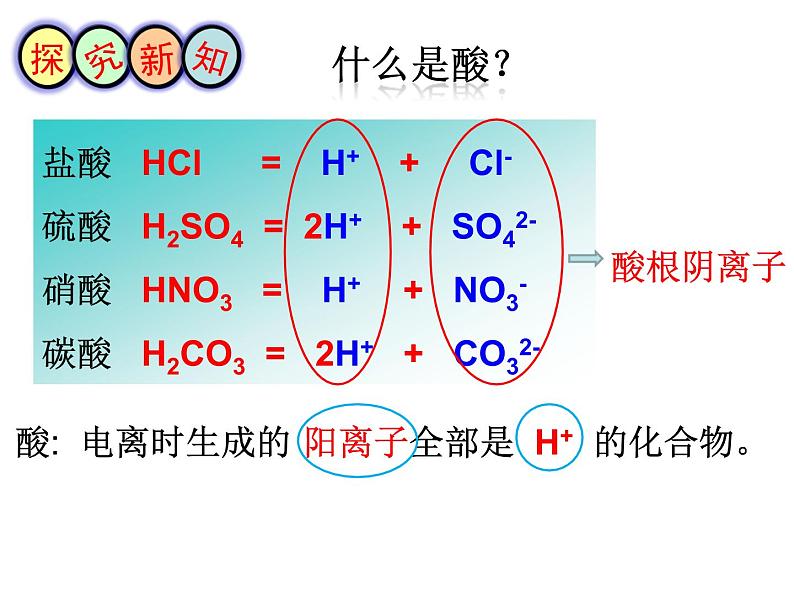
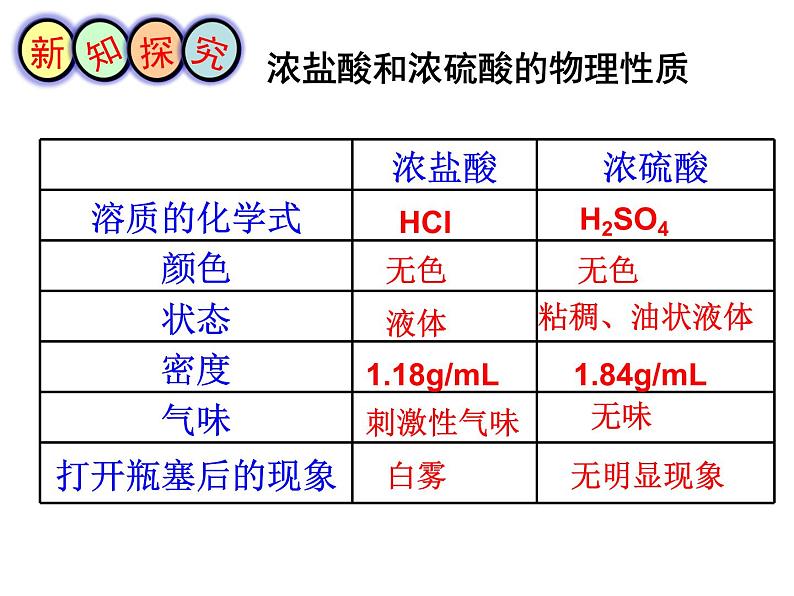
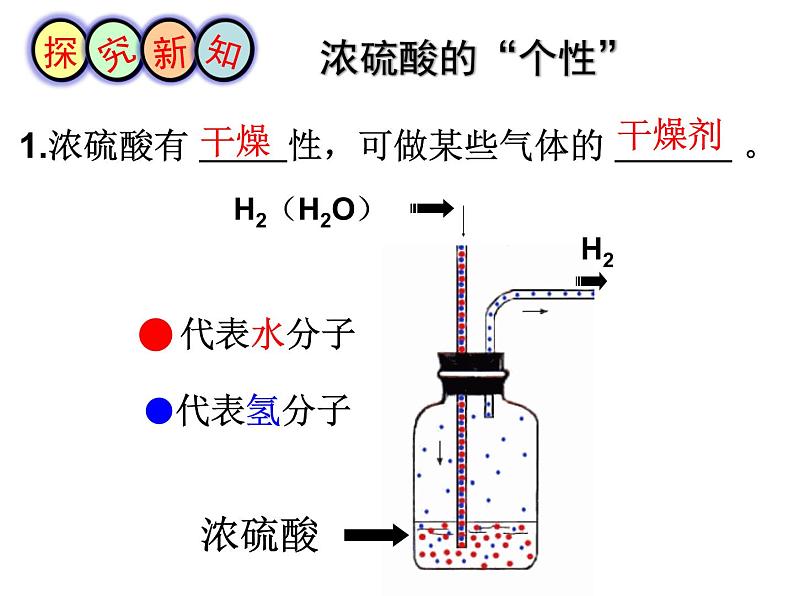
展开第一节 酸及其性质盐酸硫酸食醋西红柿橙子山楂盐酸 HCl = H+ + Cl- 硫酸 H2SO4 = 2H+ + SO42- 硝酸 HNO3 = H+ + NO3-碳酸 H2CO3 = 2H+ + CO32- 酸: 电离时生成的 阳离子全部是 H+ 的化合物。酸根阴离子什么是酸?认识浓盐酸和浓硫酸ρ=1.84g/ml浓盐酸和浓硫酸的物理性质无色白雾1.84g/mL粘稠、油状液体无味刺激性气味无明显现象1.18g/mL无色液体H2SO4HCl 浓盐酸挥发出来的氯化氢气体跟空气里的水蒸气接触,形成盐酸小液滴的缘故。 说明浓盐酸有挥发性。1、为什么打开盛浓盐酸的试剂瓶会看到有白雾出现?体现了浓盐酸的什么性质?2、如果浓盐酸溶液敞口放置,会发生什么变化? 浓盐酸具有挥发性,会导致溶液质量和溶液中溶质的质量分数都减小。 浓盐酸的“个性” 浓硫酸的“个性”代表水分子代表氢分子浓硫酸H2(H2O)H21.浓硫酸有 性,可做某些气体的 。干燥 干燥剂2.浓硫酸有 性, 使用时应非常小心。 浓硫酸的“个性”强腐蚀 演示实验:“黑面包”的形成 浓硫酸的“个性”发烫浓硫酸稀释放热演示实验:浓硫酸的稀释注意事项:稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢注入水里,并不断搅拌。切不可将水倒进浓硫酸里! 浓硫酸溅到皮肤上的处理方法: 应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液。 浓硫酸可以用作干燥剂,是因为它具有 性,所以敞口放置的浓硫酸质量会 ,溶质质量分数会 。稀释浓硫酸一定要把 沿器壁慢慢注入 里,并不断用玻璃棒搅拌,其目的是 。吸水 增大 减小浓硫酸 水加快散热 结合本节课所学知识,你有哪些方法来区分浓硫酸和浓盐酸?打开试剂瓶瓶塞有刺激性气味,出现白雾的为浓盐酸量取等体积液体,称重质量重的为浓硫酸量取等体积液体,溶于等体积水中放热多的为浓硫酸 本节课你学到了哪些知识?有什么收获和感悟?畅谈收获1、下列物质中,不需要密封保存的是( )A.浓硫酸 B.浓盐酸 C.大理石 D.澄清石灰水2、下列说法错误的是( )A.浓盐酸敞口放置一段时间后,溶质质量分数减小B.浓盐酸敞口放置一段时间后,溶质质量分数增加C.浓盐酸在空气中会产生白雾D.浓硫酸敞口一段时间后,溶质的质量分数会减少CB 3、下列说法正确的是( )A.盐酸能使紫色石蕊试液变蓝B.浓硫酸露置于空气中,溶质的质量分数变大C.醋酸露置于空气中可闻到酸味,说明醋酸有挥发性D.打开盛浓盐酸的试剂瓶,瓶口会产生白烟CD4、下列关于浓硫酸的描述错误的是( ) A.溶于水时放出大量的热 B.有强烈的腐蚀性 C.稀释浓硫酸时,切不可将水倒进浓硫酸中 D.可在量筒中用浓硫酸配制稀硫酸谢谢大家!敬请指正!
化学1 酸及其性质优秀ppt课件: 这是一份化学1 酸及其性质优秀ppt课件,文件包含第一节酸及其性质ppt、氯化钡与硫酸wmv、浓硫酸的物理性质mp4、盐酸的物理性质mp4、硝酸银与盐酸wmv、碳酸钠粉末与稀盐酸wmv、稀释浓硫酸的错误操作mp4、酸与指示剂作用wmv、酸与铁锈反应wmv、镁条与盐酸的反应wmv等10份课件配套教学资源,其中PPT共36页, 欢迎下载使用。
鲁教版 (五四制)九年级全册1 酸及其性质背景图课件ppt: 这是一份鲁教版 (五四制)九年级全册1 酸及其性质背景图课件ppt,共23页。PPT课件主要包含了学习目标,什么叫盐,效果检测等内容,欢迎下载使用。
鲁教版 (五四制)九年级全册1 酸及其性质课堂教学ppt课件: 这是一份鲁教版 (五四制)九年级全册1 酸及其性质课堂教学ppt课件,共23页。PPT课件主要包含了“尝起来酸酸的”,温故知新,HCl,HNO3,燃烧与燃料,探究之旅一,直接观察,认识浓盐酸和浓硫酸,颜色状态,探究之旅二等内容,欢迎下载使用。













