


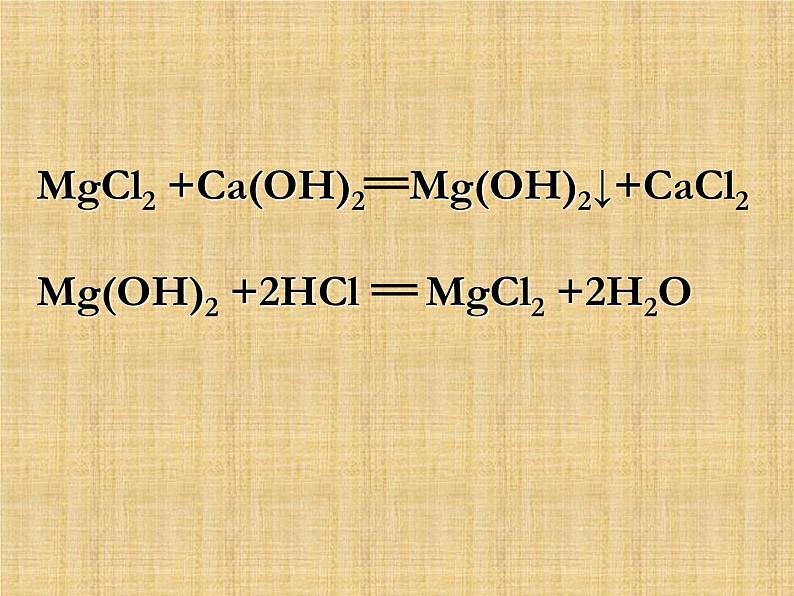


沪教版九下化学 化学反应 课件
展开
这是一份沪教版九下化学 化学反应 课件,共21页。
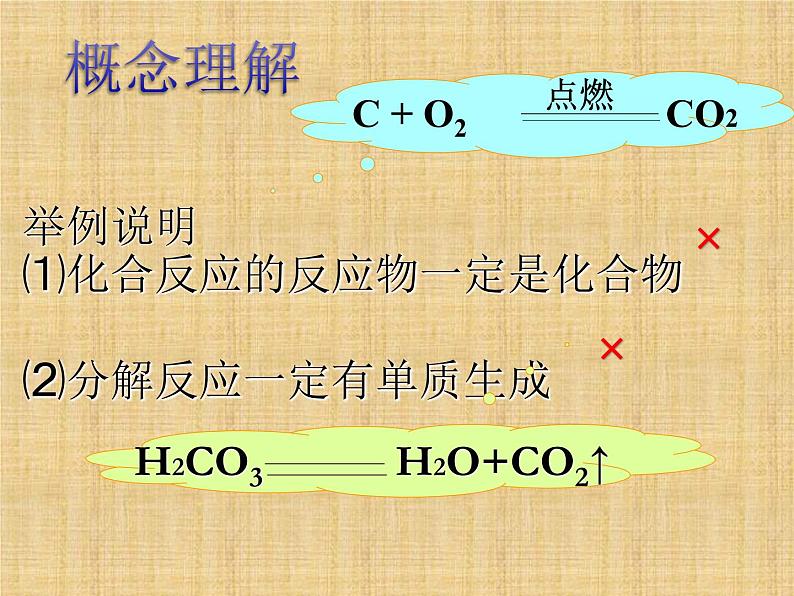
专题复习----化学反应 请写出有二氧化碳参加或有二氧化碳生成的化学方程式( 每种类型各写一个) 化合:A+B+ ==C分解:C==A+B+ 置换:A+BC==B+AC复分解:AB+CD==AD+CB回顾过去 实验室制取氧气、二氧化碳、氢气的过程中,不涉及到的反应类型是( )A.化合 B.分解 C.置换 D.复分解 学以致用生产过程:此过程发生的化学反应基本类型均属于( ) A.化合反应 B.分解反应 C.置换反应 D.复分解反应MgCl2 海水(主要成MgCl2)Mg(OH)2D学以致用举例说明⑴化合反应的反应物一定是化合物 ⑵分解反应一定有单质生成 概念理解⑶有单质和化合物生成的反应一定是置换反应⑷两种化合物生成另外两种化合物的反应一定是复分解反应 概念理解⑸生成盐和水的反应一定是中和反应概念理解化合分解置换四种化学反应基本类型中反应前后化合价的变化情况复分解反思不变:H2CO3 == H2O+CO2↑不变:H2O+CO2==H2CO3可能变可能变一定变一定不变什么情况下化合反应、分解反应的化合价会变再思复分解 氧化还原反应与四种基本类型的反应有何关系?收获复分解反应的特点1、两种化合物互相交换成分生成两种化合物;2、生成物必须有沉淀、气体或水;3、反应物溶于水或溶于酸,即盐和盐,盐和碱反应,两种反应物必须 可溶(至少微溶)4、所有元素的化合价不变回顾①氢前金属 ②稀盐酸、稀硫酸③浓硫酸、硝酸除外金属与酸发生置换反应的规律金属与盐发生置换反应规律①前置换后 ②盐必须可溶③钾、钙、钠三种金属除外注意:置换反应生成的一般是亚铁盐回顾 不是四种基本反应类型,但有二氧化碳生成或参与的反应,各举一例。提升CO2+Ca(OH)2==CaCO3+2H2O?波尔多液[CuSO4、Ca(OH)2]为何不能在铁桶中配啊?用化学方程式说明学以致用 1、(2017泉州质检)实验室制取某气体的化学方程式为:MnO2 + 4HCl(浓)== MnCl2 + X↑+ 2H2O,下列有关该反应的判断错误的是( ) A.X的化学式为Cl2 B.该反应涉及的物质中没有碱C.该反应是置换反应 D.反应前后锰元素的化合价由+4价变为+2价C轻松闯关 (2017厦门质检)甲和乙反应生成丙和丁,反应前后分子变化的微观示意图如图所示,下列叙述正确的是( )A.物质乙为催化剂B.该反应的基本类型为复分解反应C.物质甲为氧化物D.生成物丙和丁的分子个数比为1:3 轻松闯关D (2017莆田质检) 现有X、Y、Z三种金属,分别放入稀盐酸、硝酸银溶液中,结果如下表所示。判断X、Y和Z的金属活动性顺序由强到弱正确的是( ) A.X>Y>Z B.Y>Z>XC.Y>X>Z D.X>Z>Y C轻松闯关 (2017福州质检)一定条件下,A和B物质转化为C物质的关系如图所示(部分条件和部分物质未标出)。(1)若A物质是CuSO4①写出该转化属于置换反应的化学方程式: (写一个)。②若该转化属于复分解反应,C物质难溶于水,则C物质为 (写一个化学式)。(2)若A、B、C三种物质中有一种是O2①写出该属于分解反应的化学方程式: (写一个,下同)。②写出该转化不属于基本反应类型的化学方程式: 。我来试试我来试试我来试试 甲、乙、丙是初中化学常见的物质,它们之间存在如下图所示的反应关系(“—”表示物质间相互反应,“→”表示物质间的转化,部分反应物、生成物及反应条件略去)。(1)若乙、丙都是金属单质。 ①乙与丙的盐溶液反应生成丙,则金属活动性乙比丙 (填“强”或“弱”);②丙为铜,则甲物质不可能是 (填标号)。 a.O2 b.HCl c.AgNO3 d.KOH(2)若乙、丙都是常见碱,其中乙的相对分子质量大于丙。写出甲和乙反应的一个化学方程式 。(3)若甲、乙、丙分别是氧化物、酸、盐三种类别中的一种,丙常用做食品的干燥剂,则乙的化学式为: 。我来试试
相关课件
这是一份沪教版九年级上册第1节 常见的化学反应——燃烧教课内容ppt课件,共30页。PPT课件主要包含了学习目标,新课讲解,燃烧的条件,物质具有可燃性,三者缺一不可,燃烧条件,该物质的着火点,常见物质的着火点,完全燃烧与不完全燃烧,一氧化碳的化学性质等内容,欢迎下载使用。
这是一份沪教版第2节 化学反应中的质量关系评优课课件ppt,共28页。PPT课件主要包含了物质质量总和不变,质量守恒定律原因,原子数目,原子质量,原子种类,元素质量,元素种类,物质的种类,分子的种类,分子数目等内容,欢迎下载使用。
这是一份初中化学沪教版九年级上册第4章 认识化学变化第1节 常见的化学反应——燃烧试讲课课件ppt,共52页。PPT课件主要包含了观察到的现象,燃烧的特征可归纳为,蜡烛不完全燃烧,常见气体的爆炸极限,清除隔离可燃物,隔绝氧气,灭火的原理,完成课后习题等内容,欢迎下载使用。











