


福建省厦门市2021届高三三模化学练习题
展开
这是一份福建省厦门市2021届高三三模化学练习题,文件包含福建省厦门市2021届高三三模化学答案doc、福建省厦门市2021届高三三模化学试卷docx等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。
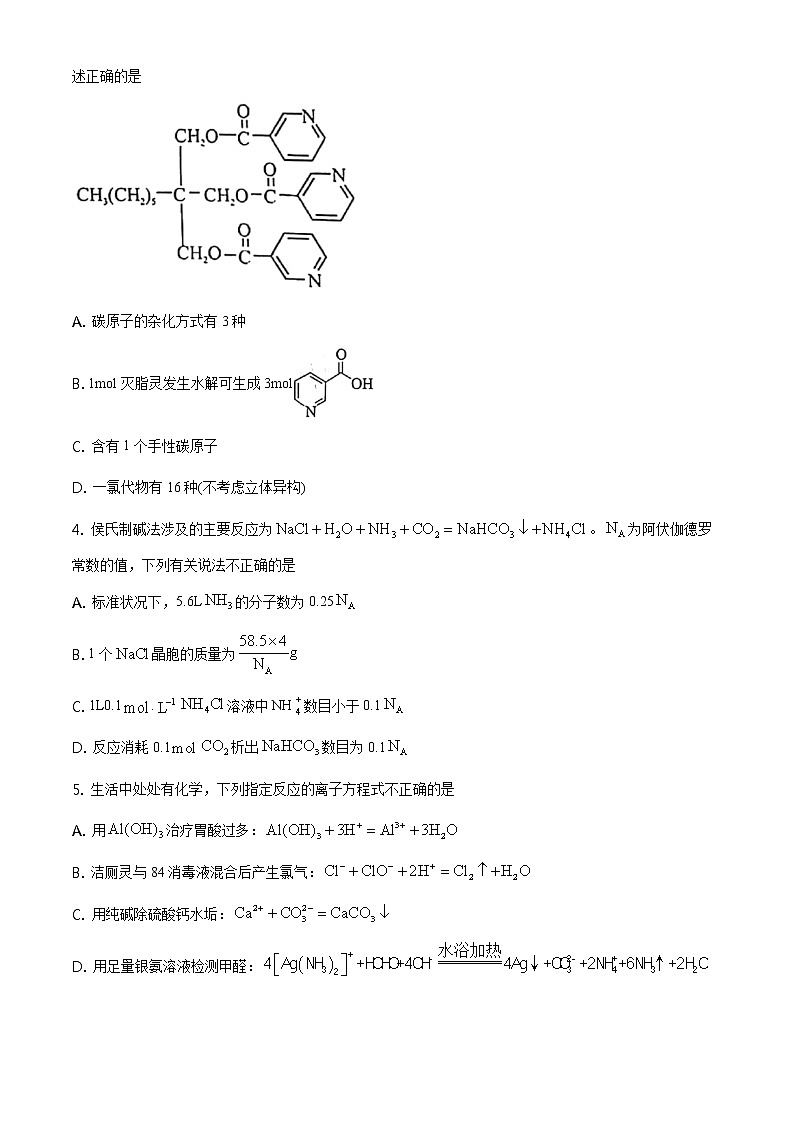
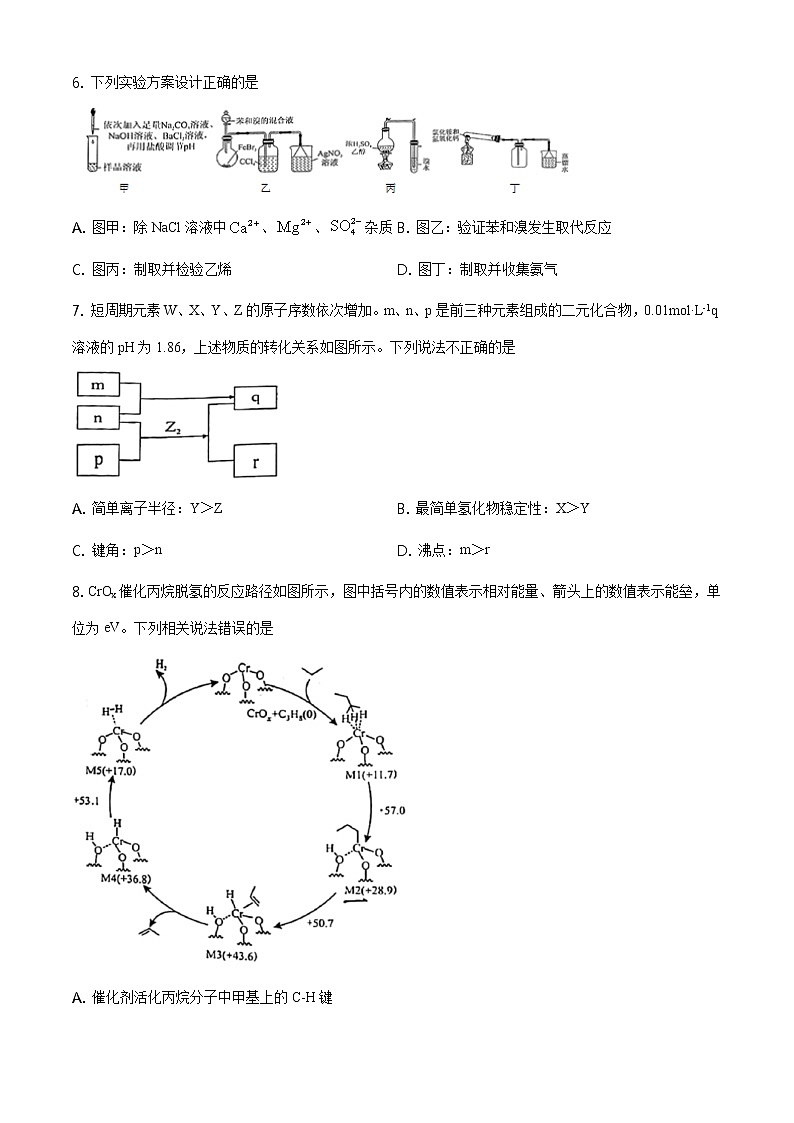
厦门市2021届高三毕业班第三次质量检测化学试题(考试时间:75分钟 满分:100分)注意事项:1.答卷前,考生务必将自己的姓名,准考证号填写在答题卡上。2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在试卷上无效。3.考试结束后,将本试卷和答题卡一并交回。可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5 Zn 65 Pb 207一、选择题:本题共10小题,每小题4分,共40分。每小题只有一个选项符合题目要求。1. 我国古代《演繁露》记载:“盐已成卤水,暴烈日,即成方印,洁白可爱,初小渐大或数十印累累相连”,其中涉及的分离方法是A. 升华 B. 蒸发 C. 萃取 D. 过滤【答案】B2. 科学家设计下列装置捕获,助力碳中和。下列有关说法错误的是
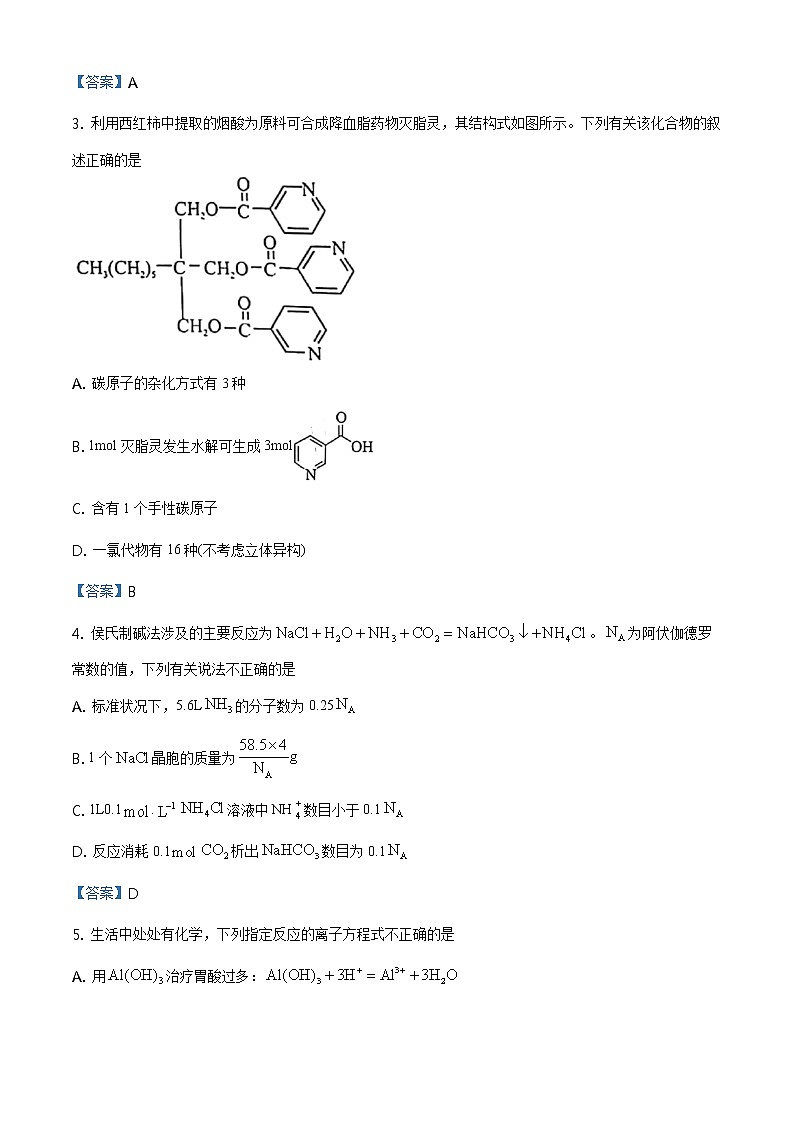
A. 与中心原子的杂化方式相同B. 的电子式为C. 阳极电极反应式为D. 的结构式为【答案】A3. 利用西红柿中提取的烟酸为原料可合成降血脂药物灭脂灵,其结构式如图所示。下列有关该化合物的叙述正确的是A. 碳原子的杂化方式有3种B. 1mol灭脂灵发生水解可生成3molC. 含有1个手性碳原子D. 一氯代物有16种(不考虑立体异构)【答案】B4. 侯氏制碱法涉及的主要反应为。为阿伏伽德罗常数的值,下列有关说法不正确的是A. 标准状况下,5.6L的分子数为0.25B. 1个晶胞的质量为C. 1L0.1溶液中NH数目小于0.1D. 反应消耗0.1析出数目为0.1【答案】D5. 生活中处处有化学,下列指定反应的离子方程式不正确的是A. 用治疗胃酸过多:B. 洁厕灵与84消毒液混合后产生氯气:C. 用纯碱除硫酸钙水垢:D. 用足量银氨溶液检测甲醛:【答案】C6. 下列实验方案设计正确的是A. 图甲:除NaCl溶液中、、杂质 B. 图乙:验证苯和溴发生取代反应C. 图丙:制取并检验乙烯 D. 图丁:制取并收集氨气【答案】B7. 短周期元素W、X、Y、Z的原子序数依次增加。m、n、p是前三种元素组成的二元化合物,0.01mol·L-1q溶液的pH为1.86,上述物质的转化关系如图所示。下列说法不正确的是A. 简单离子半径:Y>Z B. 最简单氢化物稳定性:X>YC. 键角:p>n D. 沸点:m>r【答案】C8. CrOx催化丙烷脱氢的反应路径如图所示,图中括号内的数值表示相对能量、箭头上的数值表示能垒,单位为eV。下列相关说法错误的是A. 催化剂活化丙烷分子中甲基上的C-H键B. “M2→M3”过程仅形成极性共价键C. 该催化循环中Cr的成键数目发生变化D. 该催化循环中丙烷上氢原子转移是决速步【答案】B9. 我国研制的碱性锌铁液流电池工作原理如图。下列说法不正确的是A. 充电时,a电极反应式为B. 充电时,b电极区pH增大C. 理论上,每消耗6.5gZn,溶液中将增加0.1D. 采用带负电隔膜可减少充电时产生锌枝晶破坏隔膜【答案】C10. 谷氨酸()的解离反应式:向10.000.1000谷氨酸溶液中通入或加入固体,所得溶液随加入酸或碱物质的量变化曲线如图。下列说法不正确的是A. B. 水的电离程度:b点点C. d点存在关系:D. 当谷氨酸所带净电荷为0(即与数目相等)时,溶液为3.22【答案】D二、非选择题:本题共5小题,共60分。11. 利用废铅蓄电池的铅泥(含PbSO4、PbO2和Pb)制备碱式碳酸铅[2PbCO3·Pb(OH)2]的工艺流程如下图所示:已知:25℃时,,,(1)“还原”时PbO2转化为PbO,则氧化剂与还原剂的物质的量之比为___________。(2)“转化”时溶液中___________。(3)“酸溶”时生成气体化学方程式有___________。(4)“调pH”获得2PbCO3·Pb(OH)2的相关反应:ⅰ.ⅱ.产物产率与反应温度、反应后溶液pH关系如下表。反应温度/℃反应终液pH值2PbCO3·Pb(OH)2产率/%704.350854.6747.8955.9083.41055.36866①85℃时,产物中PbCO3含量高于2PbCO3·Pb(OH)2是因为尿素水解速率___________(填“大于”或“小于”) CO结合Pb2+速率。②85~95℃,升高温度,2PbCO3·Pb(OH)2产率增加的原因为___________。(5)称取9.085g粗产品,加热分解,测得产生1.100gCO2和0.180gH2O,则产品纯度为___________(假设杂质只有PbCO3,计算结果保留3位有效数字)。【答案】 (1). 1:1 (2). 2×105 (3). 3Pb+8HNO3=3Pb(NO3)2+2NO↑+4H2O、PbCO3+2HNO3=Pb(NO3)2+CO2↑+H2O (4). 小于 (5). 温度升高,尿素水解速率加快,CO水解程度加大,溶液碱性增强,2PbCO3·Pb(OH)2产率增加 (6). 85.3%12. 碘水中存在可逆反应:I2(aq)+I-(aq)I(aq),为测定该反应的平衡常数K进行如下实验。实验i 测定平衡体系中I2和I总浓度实验ii 测定饱和碘水中I2浓度已知:。(1)碘量瓶是带磨口塞和水封槽的锥形瓶,盖上塞子后可以水封瓶口,常用于碘量分析本实验采用碘量瓶的目的是___________。(2)滴定过程应使用___________滴定管。(3)滴定过程,当溶液变为浅黄色时再加入淀粉溶液,滴定终点现象为___________。(4)实验i和实验ii中I2浓度近似相等,则实验i剩余碘固体的质量___________实验ii(填“大于”、“小于”或“等于”)。(5)实验测得平衡体系中c(I)=___________mol·L-1,平衡常数K=___________(列表达式即可)(6)下列关于实验分析的说法正确的是___________(填标号)。A.实验i的碘量瓶在使用前未烘干会影响实验结果B.实验i应精准控制加入溶液的体积C.实验ii吸取上层清液时,不慎吸入碘固体,则测得的K偏大D.实验ii滴定终点时俯视读数,则测得的K偏大(7)另外设计实验方案测定平衡常数K:取10.00碘量瓶②中上层清液,加入10萃取并分液。用0.0050溶液分别滴定水层和有机层、消耗溶液的体积为和。试分析该方案是否可行,并说明理由___________。【答案】 (1). 减小碘单质的损失 (2). 碱式 (3). 溶液蓝色褪去 (4). 小于 (5). (6). (7). AD (8). 不可行,根据数据只能获得水层中I和I2的总浓度,无法算出各自浓度,故无法算出K。或可行,根据有机层I2的浓度及分配比算出水层I2的浓度,再依次算出水层和的浓度,即可算出K。13. 低碳烷烃脱氢制低碳烯烃对有效利用化石能源有重要意义。(1)乙烷脱氢制乙烯主反应:C2H6(g)=C2H4(g)+H2(g) ΔH1副反应:2C2H6(g)=C2H4(g)+2CH4(g) ΔH2C2H6(g)=C(s)+3H2(g) ΔH3①标准摩尔生成焓是指在25℃和101kPa,由最稳定的单质生成1mol化合物的焓变。利用下表数据计算ΔH1=___________。物质C2H6(g) C2H4(g)CH4(g)标准摩尔生成焓/kJ·mol-1-84.7+52.3-74.8②恒容条件下,有利于提高C2H6平衡转化率的措施是___________(填标号)。A.高温 B.高压 C.原料气中掺入H2 D.原料气中掺入CO2③在800℃、恒容条件下,1mol C2H6进行脱氢反应,测得平衡体系中气体有0.3mol C2H6、0.6mol C2H4、0.1mol CH4和xmolH2,压强170kPa,则x=___________,主反应Kp=___________ kPa。(2)乙烷裂解中各基元反应及对应活化能如下表。反应类型反应活化能链引发ⅰ 451ⅱ 417链传递ⅲ 47ⅳ 54ⅴ 181链终止ⅵ 0ⅶ 0根据上表判断:①链引发过程中,更容易断裂的化学键是___________。②链传递的主要途径为反应___________→反应___________(填序号),造成产物甲烷含量不高。(3)使用进行乙烷脱氢催化性能研究。不同温度下,乙烷转化率及乙烯选择性随反应时间变化曲线分别如图a、图b。①550~620℃,在反应初始阶段,温度越高,乙烷转化率越大的原因是___________。②该催化剂的最佳工作温度为___________。【答案】 (1). +137.0 kJ·mol-1 (2). AD (3). 0.7 (4). 140 (5). C-C键 (6). ⅲ (7). ⅴ (8). 温度越高反应速率越快;乙烷脱氢反应为吸热,温度升高,平衡正向移动 (9). 550℃14. 我国科学家合成无铅钙钛矿单晶CsMnCl3(H2O)2,在防伪或信息加密等方面具有潜在应用。CsMnCl3(H2O)2溶剂致变色效应原理如下图。(1)基态Mn2+的价电子轨道表达式为___________。(2)CsMnCl3(H2O)2中,主族元素的电负性从大到小的顺序为___________。(3)变色过程,锰离子的配位数___________(填“有”或“没有”)发生变化。(4)从结构角度分析DMAC[结构简式为(CH3)2NCOCH3]能使含锰配离子发生变化的原因___________。(5)Cs3MnCl5晶体为正交晶系结构,晶胞参数a=b≠c,α=β=γ=90°,晶胞结构如图所示,其中Mn位于面上。①每个晶胞含Cs3MnCl5的单元数有___________个。②Cs沿z轴投影图正确的是___________(填标号)。A. B. C. D. 【答案】 (1). (2). O>Cl>H>Cs (3). 有 (4). DMAC的N、O与H2O的H形成分子间氢键,可将含锰配离子的H2O夺走,使配离子结构发生改变 (5). 4 (6). C15. 大黄酚是常用中药大黄、何首乌的有效成分,其合成路线如下。已知:回答下列问题:(1)A的化学名称为___________。(2)由C生成D的化学方程式为___________。(3)E的结构简式为___________。(4)由F生成G的反应类型为___________。(5)下列对大黄酚的描述,正确的是___________(填标号)。A.分子式为C15H10O4 B.极易溶于水C.所有碳原子共平面 D.与足量H2加成最多消耗6molH2(6)M为H的一种同分异构体,已知:1molM与饱和NaHCO3溶液充分反应能生成2molCO2与足量的Na充分反应能生成1.5 molH2;M的核磁共振氢谱显示有五组峰,峰面积之比为4∶4∶2∶1∶1.M的结构简式为___________。【答案】 (1). 邻二甲苯 (2). +(CH3CO)2O+2CH3COOH (3). (4). 还原反应 (5). AC (6).
相关试卷
这是一份2023届福建省南平市高三三模化学试题,文件包含2023学年高三市三检试卷参考答案评分细则pdf、高三化学试题pdf等2份试卷配套教学资源,其中试卷共5页, 欢迎下载使用。
这是一份2023届福建省宁德市高三三模化学试卷,共10页。
这是一份2022届福建省福州高三三模化学试卷及答案,文件包含2022届福建省福州市高中毕业班+高三下学期5月质量检测化学试卷docx、2022届福建省福州市高中毕业班+高三下学期5月质量检测化学试卷答案docx等2份试卷配套教学资源,其中试卷共12页, 欢迎下载使用。








