





初中化学沪教版九年级下册第2节 常见的酸和碱教学ppt课件
展开
这是一份初中化学沪教版九年级下册第2节 常见的酸和碱教学ppt课件,共23页。PPT课件主要包含了不变色,常见的酸,显酸性,浓盐酸,刺激性气味,18gml,瓶口出现白雾,浓硫酸,油状液体,84gml等内容,欢迎下载使用。
1.知道浓硫酸、浓盐酸的物理性质,了解稀释浓硫酸的正确操作;2.初步学会用实验探究的方法认识盐酸、稀硫酸的主要化学性质;3.了解常见的酸在生活、生产中的用途。
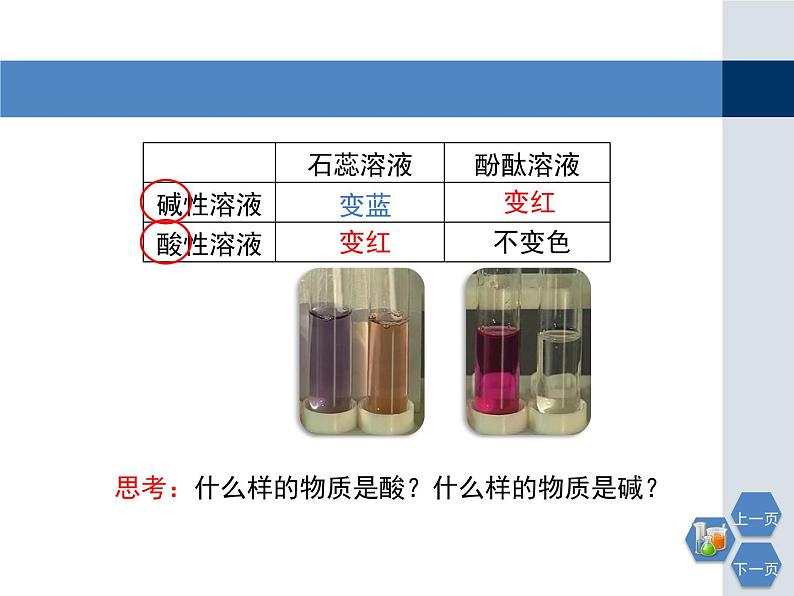
思考:什么样的物质是酸?什么样的物质是碱?
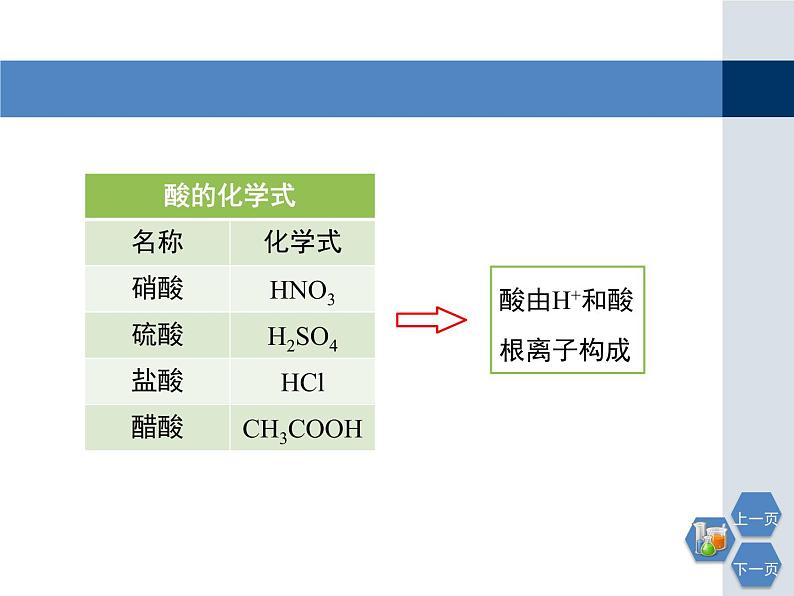
常见的酸有盐酸、硫酸、硝酸、醋酸等
浓盐酸易挥发,挥发出的氯化氢气体与水蒸气接触,形成盐酸小液滴
浓硫酸具有强烈的腐蚀性,使用时应小心
浓盐酸和浓硫酸都具有强烈的腐蚀性。
浓硫酸使纸张、木条等脱水炭化
脱水作用:浓硫酸将物质中的氢、氧元素按水的组成比脱去的作用。
浓硫酸具有吸水性,可用作干燥剂。
浓硫酸可干燥O2、H2、CO2等不与其反应的气体。
如图所示已平衡的天平两端放着两个分别盛有浓盐酸和浓硫酸的敞口烧杯,过一段时间后,天平会( )A. 左端下沉B. 右端下沉C. 仍平衡D. 无法判断
把浓硫酸缓缓注入盛有水的烧杯中,沿着烧杯壁缓缓倾倒并用玻璃棒不断搅拌。
切记:不可将水倒进浓硫酸里
活动与探究:金属与酸的作用
Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
思考:哪些金属能与盐酸反应?哪些金属不能与盐酸反应?
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
注意:位于氢前面的金属能置换出盐酸、稀硫酸中的氢,而位于氢后面的金属不能与稀盐酸、稀硫酸发生置换反应。
在实验室制备氢气可以用( )A.炭粒跟水起反应 B.铁屑跟盐酸起反应C.锌粒跟硝酸起反应 D.氧化锌跟盐酸起反应
活动与探究:金属氧化物与酸的作用
①Fe2O3+6HCl == 2FeCl3+ 3H2O②Fe2O3+3H2SO4 = Fe2(SO4)3 + 3H2O
工业上和生活中常利用酸的这一性质除去钢铁制品表面的铁锈
1.酸能使紫色石蕊试液变红;2.酸与较活泼的金属反应生成盐和氢气;3.酸与金属氧化物反应生成盐和水。
盐酸、硫酸、硝酸的用途非常广泛
用稀硫酸除铁锈的原理是( )A. FeO+H2SO4 == FeSO4+H2OB. Fe2O3+3H2SO4 == Fe2(SO4)3+3H2↑C. Fe2O3+2H2SO4 == 2FeSO4+2H2OD. Fe2O3+3H2SO4 == Fe2(SO4)3+3H2O
与酸碱指示剂反应与活泼金属反应与金属氧化物反应
重要的酸浓硫酸和浓盐酸的重要性质浓硫酸的稀释
酸具有共性的原因:溶液中含有氢离子
相关课件
这是一份中考化学复习第十单元酸和碱第1课时常见的酸和碱教学课件,共40页。PPT课件主要包含了刺激性,HCl,干燥剂,CH3COOH,纸上显出黑色字迹,蘸有浓硫酸的部位变黑,腐蚀或脱水,盐+氢气,盐+水,NaCl+H2O等内容,欢迎下载使用。
这是一份中考化学复习第十单元第1课时常见的酸和碱教学课件,共40页。PPT课件主要包含了刺激性,HCl,干燥剂,CH3COOH,纸上显出黑色字迹,蘸有浓硫酸的部位变黑,腐蚀或脱水,盐+氢气,盐+水,NaCl+H2O等内容,欢迎下载使用。
这是一份中考化学复习第十单元酸和碱第1课时常见的酸和碱教学课件,共40页。PPT课件主要包含了刺激性,HCl,干燥剂,CH3COOH,纸上显出黑色字迹,蘸有浓硫酸的部位变黑,腐蚀或脱水,盐+氢气,盐+水,NaCl+H2O等内容,欢迎下载使用。









