
沪教版基础实验7 溶液的酸碱性课后测评
展开
这是一份沪教版基础实验7 溶液的酸碱性课后测评,文件包含基础实验7溶液的酸碱性-2021-2022学年九年级化学下册精品课堂同步检测卷沪教版解析版docx、基础实验7溶液的酸碱性-2021-2022学年九年级化学下册精品课堂同步检测卷沪教版原卷版docx等2份试卷配套教学资源,其中试卷共18页, 欢迎下载使用。
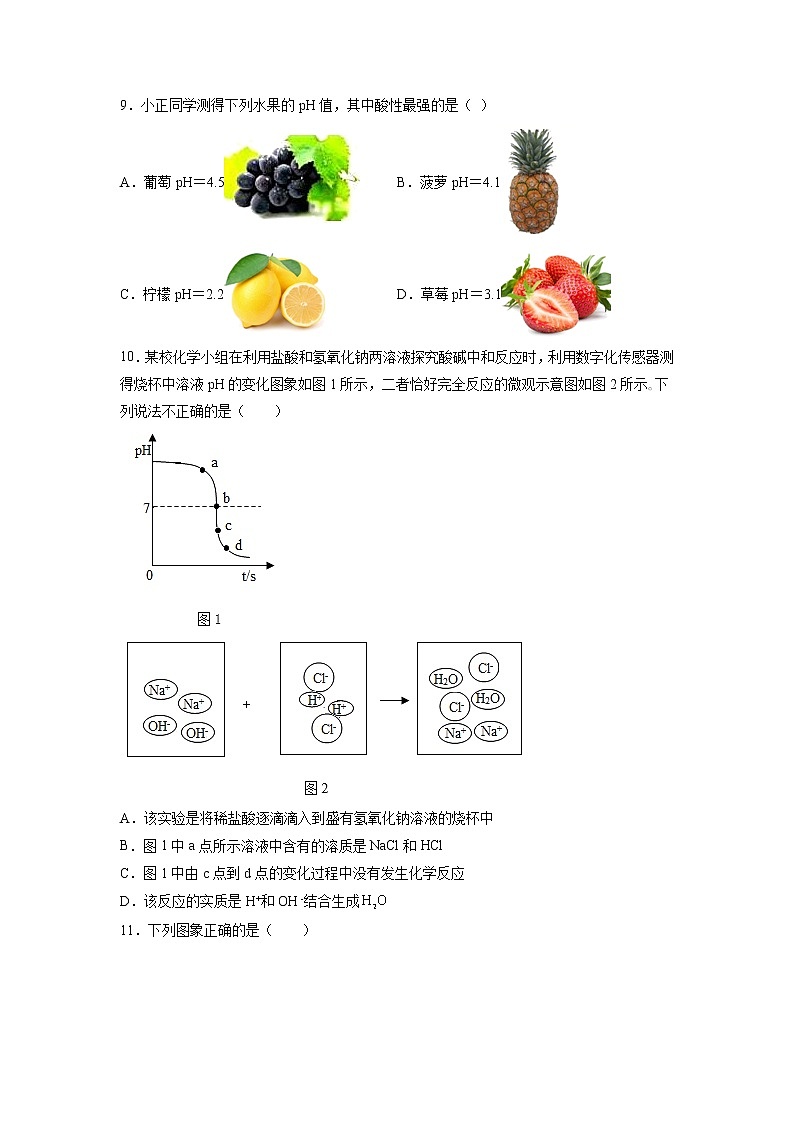
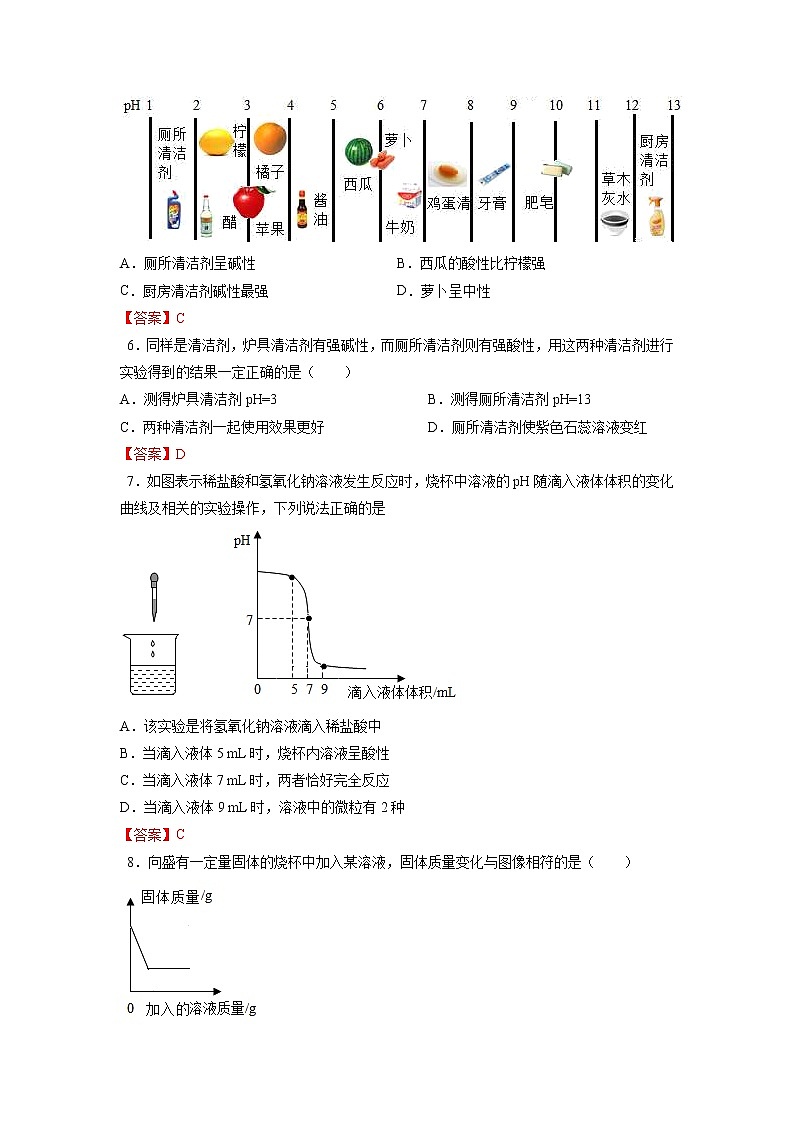
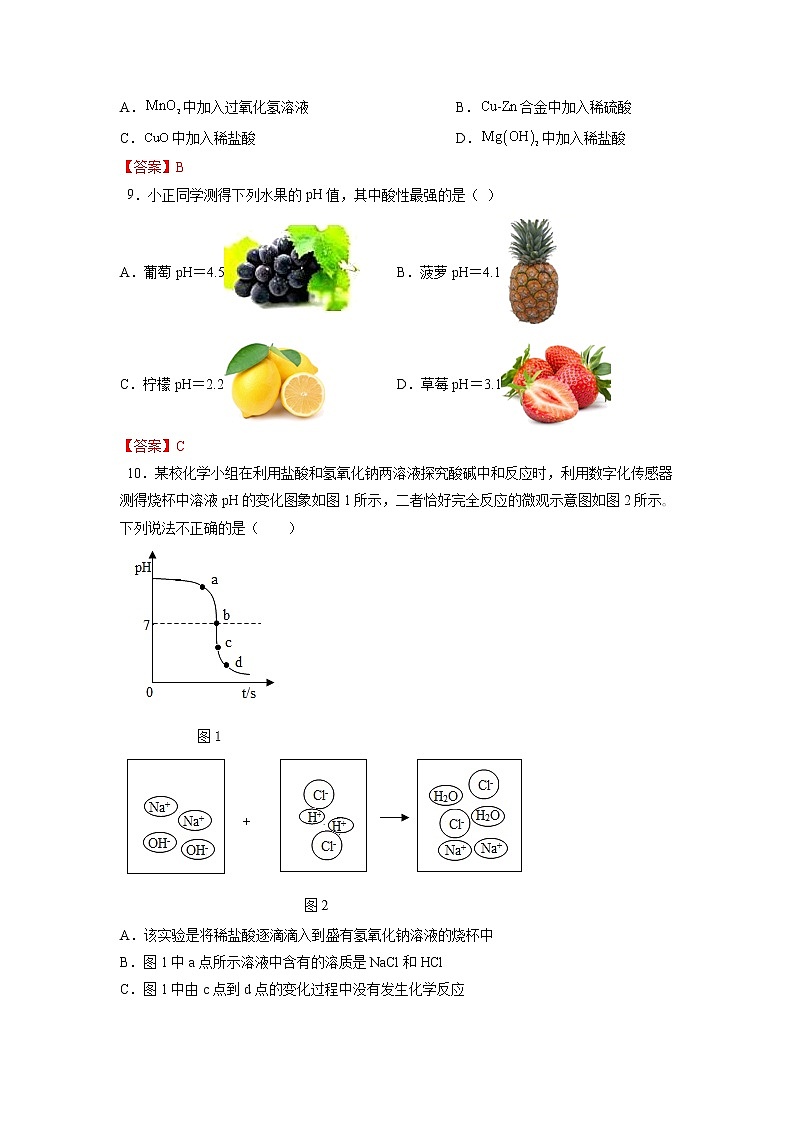
基础实验7 溶液的酸碱性第I卷(选择题)一、单选题1.用pH试纸测定某溶液的酸碱度时,如果先将试纸用蒸馏水润湿,再把该溶液滴在试纸上,则测得的结果与白醋实际的pH比较( )A.偏低 B.偏高 C.相等 D.均有可能【答案】B 2.与如图三个实验操作相对应的溶液pH变化的图象正确的是( )A.①②③ B.③①② C.②③① D.①③②【答案】B 3.在生活、生产和科学研究中,常用pH试纸测定溶液的pH。以下测定操作正确是( )A.将被测液滴到放在玻璃片上的pH试纸上,显色后,与标准比色卡比较B.将pH试纸直接投入被测液中,显色后,取出与标准比色卡比较C.先用少量水湿润试纸,后滴上被测液,显色后,与标准比色卡比较D.先用蒸馏水清洗滴管,随后吸取被测液滴到试纸上,显色后,与标准比色卡比较【答案】A 4.下列能使紫色石蕊试液和无色酚酞试液均变色的是( )A.pH=1的盐酸 B.pH=3的硫酸C.pH=7的氯化钠溶液 D.pH=14的氢氧化钾溶液【答案】D 5.如图为身边一些物质的pH图,以下说法正确的是( )A.厕所清洁剂呈碱性 B.西瓜的酸性比柠檬强C.厨房清洁剂碱性最强 D.萝卜呈中性【答案】C 6.同样是清洁剂,炉具清洁剂有强碱性,而厕所清洁剂则有强酸性,用这两种清洁剂进行实验得到的结果一定正确的是( )A.测得炉具清洁剂pH=3 B.测得厕所清洁剂pH=13C.两种清洁剂一起使用效果更好 D.厕所清洁剂使紫色石蕊溶液变红【答案】D 7.如图表示稀盐酸和氢氧化钠溶液发生反应时,烧杯中溶液的pH随滴入液体体积的变化曲线及相关的实验操作,下列说法正确的是A.该实验是将氢氧化钠溶液滴入稀盐酸中B.当滴入液体5 mL时,烧杯内溶液呈酸性C.当滴入液体7 mL时,两者恰好完全反应D.当滴入液体9 mL时,溶液中的微粒有2种【答案】C 8.向盛有一定量固体的烧杯中加入某溶液,固体质量变化与图像相符的是( )A.中加入过氧化氢溶液 B.合金中加入稀硫酸C.中加入稀盐酸 D.中加入稀盐酸【答案】B 9.小正同学测得下列水果的pH值,其中酸性最强的是( )A.葡萄pH=4.5 B.菠萝pH=4.1C.柠檬pH=2.2 D.草莓pH=3.1【答案】C 10.某校化学小组在利用盐酸和氢氧化钠两溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图1所示,二者恰好完全反应的微观示意图如图2所示。下列说法不正确的是( )A.该实验是将稀盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中B.图1中a点所示溶液中含有的溶质是NaCl和HClC.图1中由c点到d点的变化过程中没有发生化学反应D.该反应的实质是H+和OH -结合生成【答案】B 11.下列图象正确的是( ) A.甲:向酸溶液中不断加水稀释 B.乙:向碱溶液中不断加水稀释 C.丙:向稀盐酸中不断加NaOH溶液 D.丁:向KOH溶液中不断滴加稀硫酸【答案】B【解析】A、酸溶液显酸性pH<7,向酸中加入水,酸性减弱,溶液的pH增大,但是不会大于7,故错误,不符合题意;B、碱溶液显碱性pH>7,向碱中加入水,碱性减弱,溶液的pH减小,但是不会小于7,故正确,符合题意;C、原溶液是稀盐酸,pH<7,当加入氢氧化钠与其反应,pH逐渐增大到等于7;当稀盐酸全部反应后,随着氢氧化钠增多,pH>7,故错误,不符合题意;D、原溶液是氢氧化钾,pH>7,当加入稀硫酸与其反应,pH逐渐减小到等于7;当稀硫酸全部反应后,随着稀硫酸增多,pH<7,故错误,不符合题意。故选B。12.下列有关pH试纸的使用说法正确的是( )A.把pH试纸浸入待测液B.用湿润的玻璃棒蘸取待测液C.把显色的pH试纸与标准比色卡对照读数D.测出石灰水的pH为12.4【答案】C 13.下列现象中,能说明某溶液呈酸性的是( )A.用pH试纸测定,其pH=8 B.用pH试纸测定,其pH=7C.向其中滴加紫色石蕊溶液,呈红色 D.向其中滴加无色酚酞溶液,呈红色【答案】C 14.大致测定某溶液是酸性还是碱性,要采取( )①石蕊试液 ②酚酞试液 ③石蕊试纸 ④pH试纸A.只有①② B.只有①②③C.只有①④ D.以上都可以【答案】D 15.SO2是造成酸雨的主要气体之一,其水溶液叫亚硫酸(H2SO3)溶液。H2S是一种具有臭鸡蛋气味 的剧毒气体,其水溶液叫氢硫酸溶液。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。室温下,向饱和的亚硫酸溶液中通入过量的硫化氢气体,发生反应如下: 。则下图中溶液的 pH 随通入硫化氢体积的变化曲线示意图正确的是( )A. B. C. D.【答案】A【解析】酸性溶液pH小于7,且酸性越强pH越小。随着反应2H2S+H2SO3═3S↓+3H2O的发生,溶液的酸性变弱,pH会不断变大,图象会是一条上升的曲线;至恰好反应时pH等于7,继续滴加氢硫酸溶液会再次显酸性,但由于氢硫酸的酸性弱于亚硫酸,故溶液最后的pH会比开始时大。故选A。16.下列两种不同pH的溶液混合,有可能得到中性溶液的是( )A.pH=1和pH=7 B.pH=5和pH=14C.pH=3和pH=4 D.pH=8和pH=10【答案】B【解析】A、pH=1的溶液呈酸性,pH=7的溶液呈中性,二者混合不能得到中性溶液,故A错误。B、pH=5的溶液呈酸性,pH=14的溶液呈碱性,二者混合可能得到中性溶液,故B正确。C、pH=3的溶液呈酸性,pH=4的溶液呈酸性,二者混合溶液仍然呈酸性,故C错误。D、pH=8的溶液呈碱性,pH=10的溶液呈碱性,二者混合溶液仍然呈碱性,故D错误。故选:。17.如表是人体部分体液的正常pH范围,其中酸性最强的是( )体液唾液胃液胰液胆汁pH6.6~7.10.9~1.57.5~8.07.1~7.3【答案】B【解析】溶液酸性越强,pH越小;碱性越强,pH越大。一般情况下,0<pH<7时溶液呈酸性,pH越小,酸性越强;7<pH<14时溶液呈碱性,pH越大,碱性越强。由表格可知,胃液的pH<7且是最小,所以胃液的酸性最强,故B正确故答案为B。18.日常生活中常见的下列物质,酸性最强的是( )A.洗涤剂 B.酱油 C.柠檬汁 D.鸡蛋清【答案】C 第II卷(非选择题 共46分)二、填空题19.NaOH是化学实验中常用的试剂。
(1)将某NaOH溶液逐滴滴入一定量的某盐酸中,溶液的pH随所加氢氧化钠溶液质量而变化,如图1所示.其中合理的图象是__________(选填“甲”或“乙”)。(2)如图2表示该反应前后溶液中存在的主要离子,在下面横线上写出这两种图形表示的离子(填离子符号)。____________________。【答案】乙 20.将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度随加入稀盐酸的质量变化曲线如下图所示:(1)在滴加的过程中,烧杯中溶液的pH逐渐_________(选填“增大”“减小”或“不变”)。(2)由图可知,稀盐酸与氢氧化钠溶液发生的反应是________(选填“放热”或“吸热”)反应。(3)图中B点时,溶液中的溶质是_________(填化学式)。(4)图中C点对应的溶液中存在的离子有_________(填写离子符号)。【答案】减小 放热 NaCl Na+、Cl-、H+ 【解析】(1)在滴加过程中,氢氧化钠与盐酸反应生成氯化钠和水,故溶液的pH逐渐减小;(2)由图可知,随着反应的进行,溶液温度逐渐升高,说明稀盐酸与氢氧化钠发生的反应是放热反应;(3)由图可知,图中B点时,温度最高,说明此时氢氧化钠与稀盐酸恰好完全反应生成氯化钠和水,故溶液中的溶质是:NaCl;(4)C点时,盐酸过量,溶液中的溶质是NaCl、HCl,故存在的离子有:Na+、Cl-、H+。21.硫酸是一种常见的酸,完成下列问题。(1)实验室浓硫酸稀释的方法是______。(2)为研究稀硫酸的化学性质,某同学进行了如下实验。实验中,有气泡产生的反应的化学方程式是______,溶液有颜色变化的是______(填序号),E试管中观察到的现象是______。【答案】将浓硫酸沿烧杯壁缓慢注入水中,并用玻璃棒不断搅拌
ACD有白色沉淀生成 三、实验题22.中和反应在工农业生产和生活中有广泛应用。某学生课外兴趣小组对中和反应进行研究。对于没有明显实验现象产生的中和反应,如稀盐酸与稀氢氧化钠溶液的反应,要证明它们之间确实发生了化学反应,可通过如下实验来进行。(1)向一锥形瓶中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为_______色为止,共用去稀盐酸20g,则反应后溶液中溶质质量分数为___________(结果精确到0.1%)。反应后溶液中的溶质可用_________的方法(填一操作名称)使其析出。(2)向一支试管内倒入约2mL氢氧化钠溶液,再逐滴滴入盐酸,边滴边振荡。然后用玻璃棒蘸取反应液沾到pH试纸上,与标准比色卡对照。因无法通过肉眼观察到反应进程,需间隔数滴多次检测溶液的pH,所以每使用玻璃棒蘸取溶液前,必须进行______________的预处理。下列使用pH试纸的方法中,正确的是______________(填序号)。A将pH试纸剪成几段使用B将pH试纸直接插入待测液中C将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上D将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上E读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照同学们经过前几次测量发现pH在不断减小,能否仅从pH变小得出盐酸与氢氧化钠确实发生反应的结论?为什么? ________________________。【答案】无 2.9% 蒸发溶剂 洗涤擦拭 ACE 不能仅从pH变小得出盐酸与氢氧化钠确实发生反应的结论,理由是稀盐酸可能和碳酸钠反应,导致pH变小 【解析】(1)氢氧化钠溶液显碱性,能使酚酞试液变红色,向一锥形瓶中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,溶液变红色,氢氧化钠和稀盐酸反应生成氯化钠和水,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为无色为止,共用去稀盐酸20g。设反应后溶液中溶质质量为x x=1.17g故反应后溶液中溶质质量分数为 。氯化钠的溶解度受温度影响较小,故反应后溶液中的溶质可用蒸发溶剂的方法使其析出。(2)蘸取的氢氧化钠溶液和空气中二氧化碳反应生成碳酸钠和水,所以每使用玻璃棒蘸取溶液前,必须进行洗涤擦拭的预处理。A、使用pH试纸时,可将pH试纸剪成几小段后使用,故A正确;B、不能将pH试纸伸入溶液中检测溶液的pH,否则会污染试剂,故B不正确;C、将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上,再与标准比色卡对照,故C正确;D、pH试纸先用水润湿再用玻璃棒蘸取少量待测点在试纸上,这样的操作会使溶液变稀,测量的数据不准确,故D不正确;E、读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照,故E正确。故选ACE。氢氧化钠和空气中的二氧化碳反应生成碳酸钠和水,稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,经过测量发现pH在不断减小,不能仅从pH变小得出盐酸与氢氧化钠确实发生反应的结论,理由是稀盐酸可能和碳酸钠反应,导致pH变小。四、科学探究题23.要探究酸和碱能否发生化学反应,进行如下实验,请完成下列问题:实验步骤实验现象或结果记录1.提出问题:氢氧化钠溶液与稀盐酸反应吗?设计方案:向试管中加入2mL溶质质量分数为0.4%的氢氧化钠溶液,然后逐滴滴入质量分数为0.4%的稀盐酸,边滴加边振荡,观察现象_____2.重新设计方案,继续探究。(1)分别测量水、0.4%的氢氧化钠溶液、0.4%的稀盐酸的pH并记录(2)如图:分別取2mL水和0.4%的氢氧化钠溶液于两支试管中,各加入2mL0.4%的稀盐酸。测量所得溶液的pH并记录。水的pH等于7,氢氧化钠溶液的pH大于7,稀盐酸的PH_____。混合后,溶液甲的PH_____,溶液乙的pH减小。反应的化学方程式:_____。3.获得结论:稀盐酸和氢氧化钠溶液_____(填“能”或“不能”)发生化学反应,但是_____(填“有”或“没有”)明显现象,可以借助测定溶液反应前后_____变化的方法来帮助人们判断它们是否发生反应。【答案】无明显现象 小于7 减小 能 没有 酸碱度(或PH) .实验小组的四位同学在探究碱的性质时发现氢氧化钠、氢氧化钙等可溶性碱都能使酚酞试液变红.他们想进一步探究:不溶性的氢氧化镁是否也能使酚酞试液变红.为此,他们将适量的氢氧化镁加入到盛有热水的烧杯中搅拌,然后向浑浊的液体中滴加酚酞试液,发现酚酞试液变红,可是过一会儿红色又消失了.四位同学依据所学的化学知识,分别对上述酚酞试液变红、红色又消失的原因作了如下猜想:小明:可能是个偶然现象.小东:可能是浑浊液体中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了.小花:可能是酚酞试液与空气中的氧气反应,使红色消失;也可能是氢氧化镁溶液与空气中的二氧化碳反应的缘故.小红:可能是在热水中氢氧化镁的溶解度大,溶液中OH-离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中OH-离子变少,酚酞试液又变无色.(1)对小明猜想“是个偶然现象”,四位同学都认为可以用科学探究的一般方法排除偶然现象.他们的方法是:________.(2)小花认为小东的猜想不正确,她从碱使酚酞试液变色的原因上给予了否定,小花的理由是_ __ 。(3)四位同学讨论后认为要验证小花的猜想,还需做如下实验,你知道其实验的目的吗?实验步骤设计目的将氢氧化镁加入到热水中搅拌,滴入酚酞试液,并在上方滴一些植物油①_____(4)对小红的猜想,实验小组的同学设计了多种实验方案进行证明.请你写出其中一种.实验方法可能观察到的现象相应结果或结论①________②______③________【答案】做重复实验 固体氢氧化镁中没有自由移动的OH-离子,不能使酚酞试液变红 隔绝空气证明红色消失与氧气和二氧化碳无关 取两支试管,分别加入相同质量的氢氧化镁和相同质量的热水振荡,各滴加数滴酚酞试液,一支保持温度不变,另一支自然冷却 保持温度不变的红色不消失(或消失),自然冷却的红色消失(或不消失) 红色消失与氢氧化镁的溶解度随温度降低而减小有关(或无关)
相关试卷
这是一份初中化学沪教版九年级下册基础实验7 溶液的酸碱性课时作业,共13页。试卷主要包含了单选题,判断题,填空题,综合应用题等内容,欢迎下载使用。
这是一份沪教版九年级下册第2节 糖类 油脂课后测评,文件包含第2节糖类油脂-2021-2022学年九年级化学下册精品课堂同步检测卷沪教版解析版docx、第2节糖类油脂-2021-2022学年九年级化学下册精品课堂同步检测卷沪教版原卷版docx等2份试卷配套教学资源,其中试卷共11页, 欢迎下载使用。
这是一份初中化学沪教版九年级下册基础实验8 酸与碱的化学性质同步练习题,文件包含基础实验8酸与碱的化学性质-2021-2022学年九年级化学下册精品课堂同步检测卷沪教版解析版docx、基础实验8酸与碱的化学性质-2021-2022学年九年级化学下册精品课堂同步检测卷沪教版原卷版docx等2份试卷配套教学资源,其中试卷共17页, 欢迎下载使用。