

2022届中考化学工艺流程题型专练(2)提纯类
展开(2)提纯类
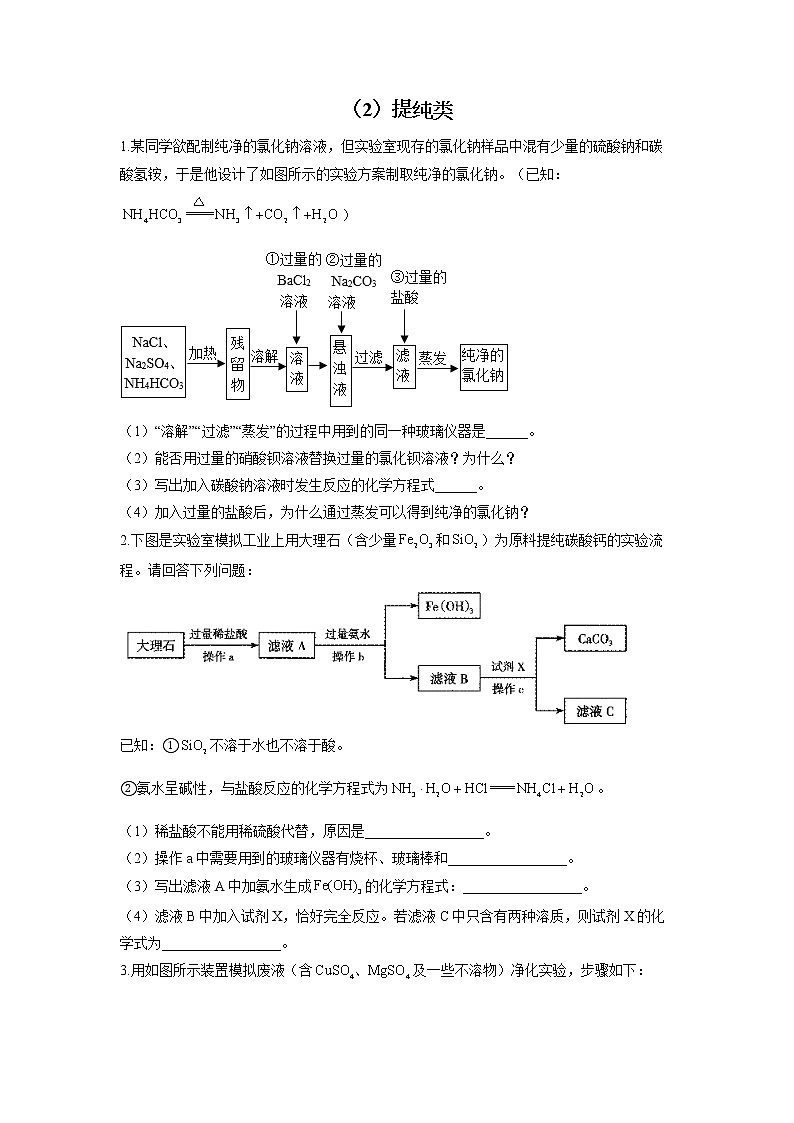
1.某同学欲配制纯净的氯化钠溶液,但实验室现存的氯化钠样品中混有少量的硫酸钠和碳酸氢铵,于是他设计了如图所示的实验方案制取纯净的氯化钠。(已知:)
(1)“溶解”“过滤”“蒸发”的过程中用到的同一种玻璃仪器是______。
(2)能否用过量的硝酸钡溶液替换过量的氯化钡溶液?为什么?
(3)写出加入碳酸钠溶液时发生反应的化学方程式______。
(4)加入过量的盐酸后,为什么通过蒸发可以得到纯净的氯化钠?
2.下图是实验室模拟工业上用大理石(含少量和)为原料提纯碳酸钙的实验流程。请回答下列问题:
已知:①不溶于水也不溶于酸。
②氨水呈碱性,与盐酸反应的化学方程式为。
(1)稀盐酸不能用稀硫酸代替,原因是_________________。
(2)操作a中需要用到的玻璃仪器有烧杯、玻璃棒和_________________。
(3)写出滤液A中加氨水生成的化学方程式:_________________。
(4)滤液B中加入试剂X,恰好完全反应。若滤液C中只含有两种溶质,则试剂X的化学式为_________________。
3.用如图所示装置模拟废液(含及一些不溶物)净化实验,步骤如下:
Ⅰ.往沉降槽中加入适量絮凝剂(混凝剂)甲,加速沉降:
Ⅱ.往反应槽中缓慢加入一定浓度的NaOH溶液,至沉淀完全;
Ⅲ.通过盛装有活性炭的水槽后,调节溶液的pH=7,储存在指定容器中。
(1)测得原废液pH=5,显_________________(填“酸性”“碱性”或“中性”)。
(2)甲是_________________(写物质名称);操作X可使固体与液体分离,操作X是_________________;活性炭的作用是_________________。
(3)反应槽中生成沉淀的化学方程式为_________________(写一个)。
4.五氧化二钒()广泛应用于化工行业。工业上的钒废催化剂主要含硫酸氧钒()和少量的(难溶于水且不与水反应)杂质,现要除去杂质并得到固体,其流程如下:
(1)操作①的名称是______,废渣的主要成分是______。
(2)25℃时,取样进行分析,得到沉淀率和溶液pH之间的关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
在以上流程中,步骤③中加入氨水调节溶液的最佳pH范围为______。
(3)步骤④的另一产物是水,该步骤反应的化学方程式为______。
(4)该工艺流程中可以循环利用的物质(除水外)是______。
5.某工厂的废水中含有和,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如下图所示。
(1)固体A与某酸反应的化学方程式为__________。
(2)实验室在进行操作②时,当__________即可停止加热。
(3)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为__________。
(4)溶液a除了可能含有NaOH外,还一定含有的溶质是__________(填化学式)。
6.硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料。某硫酸钠粗盐中含有少量和,实验室进行提纯的流程如下:
回答下列问题:
(1)溶解过程需要的玻璃仪器有烧杯和________。
(2)用NaOH除杂时,反应的化学方程式为________。
(3)NaOH和如果添加过量了,可加入适量________除去。
(4)“后续处理”的主要操作是蒸发,为了获得纯净的硫酸钠,应蒸发至________(填序号)。
A.完全蒸干时停止加热
B.有较多固体析出时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
7.电子工业常用30%的溶液腐蚀覆盖一层薄铜的绝缘板,制成印刷电路板。人们为了从废腐蚀液(含有和)中回收铜,并重新得到溶液,设计如下实验流程。
已知:。
(1)属于_____(填“酸”“碱”或“盐”)。
(2)反应①后进行的分离操作的名称是_____,得到的滤渣成分是_____。
(3)反应②的基本反应类型是_____。
(4)反应③为化合反应,则该反应的化学方程式是_____。
8.实验室有100g废液,其中含有。现对废液进行处理得到铜和硫酸锌溶液,实验流程如图所示。
(1)步骤I、Ⅱ、Ⅲ中均包含的操作名称是滤液B中除水外,还含有的物质是_________。
(2)步骤I反应的化学方程式为_________。
(3)步骤Ⅱ当观察到_________时,说明滤渣A中铁已经完全反应;反应的化学方程式为_________。
(4)步骤Ⅲ中加入的X是_________(填化学式)。
9.小刚收集到一瓶浑浊的东江水,他要模拟自来水厂的净水过程,最终制成蒸馏水。其实验过程如下所示。请回答以下问题。
(1)A物质的名称是_____________,操作①的名称是_____________,若经过操作①后,所得液体C中仍浑浊,其原因可能有_____________(填写序号);
a.漏斗内的滤纸有破损
b.漏斗下端未靠在烧杯内壁
c.漏斗内液面高于滤纸的边缘
(2)操作②主要是除去一些异味和色素,应选用药品是_____________,该过程主要是_____________变化(填“物理”或“化学”)。
(3)小刚取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是_____________水。操作③应选用的方法是_____________,经过操作③以后,小刚重复上述实验,他观察到的实验现象是_____________。
10.完成“金属的化学性质”实验后,废液桶里的废液中含有大量的氯化锌、氯化亚铁和氯化铜。为了回收氯化锌晶体并分离得到单质铜和单质铁,同学们设计了如图所示的回收流程。
(1)操作①、②、④中均用到了同一玻璃仪器,该仪器是_______。
(2)固体C的成分是_______。操作③所用的物品是_______。
(3)固体A中加入了适量的氯化亚铁溶液,_______(填“能”或“不能”)改用氯化铜溶液。请说明理由:_______(用化学方程式表示)。
(4)写出固体A中加入氯化亚铁溶液反应的化学方程式:_______。
答案以及解析
1.答案:(1)玻璃棒
(2)不能。硫酸钠和硝酸钡溶液反应生成硝酸钠和硫酸钡沉淀,会引入新的杂质硝酸钠
(3)
(4)蒸发过程中盐酸中的氯化氢逸出
解析:(1)“溶解”“过滤”“蒸发”的过程中用到的同一种玻璃仪器是玻璃棒。故填:玻璃棒。
(2)硫酸钠和硝酸钡溶液反应生成硝酸钠和硫酸钡沉淀,会引入新的杂质硝酸钠。所以,不能用过量的硝酸钡溶液替换过量的氯化钡溶液。故填:不能。因为硫酸钠和硝酸钡溶液反应生成硝酸钠和硫酸钡沉淀,会引入新的杂质硝酸钠。
(3)加入碳酸钠溶液时与剩余的氯化钡反应生成碳酸钡沉淀和氯化钠。故填:。
(4)加入过量的盐酸后,通过蒸发可以得到纯净的氯化钠是因为盐酸具有挥发性。蒸发过程中盐酸中的氯化氢逸出。故回答成:蒸发过程中盐酸中的氯化氢逸出。
2.答案:(1)硫酸与碳酸钙反应,生成微溶的硫酸钙阻止反应继续进行
(2)漏斗
(3)
(4)
解析: (1)硫酸与碳酸钙反应生成的硫酸钙微溶于水,附着在碳酸钙表面,阻止反应的进一步发生。
(2)操作a是过滤,还需要的玻璃仪器是漏斗。
(3)反应物之一为,生成物中有沉淀,分析流程可知另一种反应物为,故另一种生成物为,配平即可。
(4)滤液C中有两种溶质;加入的X中含,则加入的X不引入新的阳离子,为。
3.答案:(1)酸性
(2)明矾(或其他合理答案);过滤;吸附
(3)[或]
解析:(1)测得原废液pH=5,则显酸性。
(2)往沉降槽中加入适量的絮凝剂明矾可加速沉降;往反应槽中缓慢加入一定浓度的氢氧化钠溶液,至沉淀完全,发生的反应有硫酸铜和氢氧化钠反应生成硫酸钠和氢氧化铜沉淀,硫酸镁和氢氧化钠反应生成硫酸钠和氢氧化镁沉淀,再经过滤操作可使固体与液体分离。
4.答案:(1)过滤;
(2)1.7~1.8
(3)
(4)氨气(或氨水)
解析:(1)操作①将废渣和溶液分离开,为过滤操作;将钒废催化剂的主要成分和操作①后溶液中的主要成分对比可知废渣的主要成分是。
(2)制备流程中,应让沉淀率最高,所以应调节溶液pH的范围为1.7~1.8。
(4)流程中步骤④的产物有氨气水和,步骤③需加入氨水,因此可循环利用的物质是氨气(或氨水)。
5.答案:(1)
(2)出现较多固体时
(3)
(4)
解析:(1)从题图可知固体A中加入某酸溶液后得到的是硫酸镁,所以某酸溶液指的是硫酸,固体A是与NaOH反应生成的,写出反应的化学方程式即可。
(3)固体B加热得到氧化铁,所以固体B应是与NaOH反应生成的,根据质量守恒定律可知,另一种氧化物的化学式应为。
(4)溶液a中含有反应生成的NaCl和。
6.答案:(1)玻璃棒
(2)
(3)稀硫酸
(4)B
解析:除杂过程中加入NaOH是为了除去,加入是为了除去。NaOH和如果添加过量,可加入适量的酸除去,考虑到最后的产品是硫酸钠固体,为了不引入新的杂质,应加入稀硫酸。
7.答案:(1)盐
(2)过滤;铜、铁
(3)置换反应
(4)
8.答案:(1)过滤;硫酸亚铁、硫酸锌
(2)
(3)不再产生气泡;
(4)Zn
解析:(1)步骤I、Ⅱ、Ⅲ中均包含的操作名称是过滤。滤液B中除水外,还含有的物质是反应生成的、废液中原有的硫酸亚铁及没有反应的硫酸锌。
(2)步骤I中,铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式:。
(3)由于步骤I中加入的铁过量,所以滤渣A中含有Fe、Cu,加入过量稀硫酸,稀硫酸与Fe反应生成和,所以步骤Ⅱ当观察到不再产生气泡时,说明滤渣A中铁已经完全反应;反应的化学方程式:。
(4)滤液B中含有溶液C中含有,欲得到溶液,则步骤Ⅲ中加入的X是Zn。
9.答案:(1)明矾;过滤 ;a、c
(2)活性炭;物理
(3)硬水;蒸馏(或煮沸);有较多泡沫且没有浮渣
解析:(1)在自来水的生产中一般要先加入絮凝剂,使小颗粒泥尘凝聚成大颗粒,最常用的絮凝剂是明矾;紧接着是过滤,分离出不溶性的固体,所以操作①是过滤,所得液体C中仍有浑浊,可能是滤纸破了或者液面高于滤纸的边缘,故选a、c;
(2)经过过滤得到的水还含有有色或有异味的物质,要经过活性炭吸附才能除去,故操作②应选择装置川,该过程没有新物质生成,所以是物理变化;
(3)硬水中含有较多的可溶性钙、镁化合物,当加入肥皂水后,会出现许多浮渣,因此液体D是硬水;要使硬水变成蒸馏水,必须经过蒸馏,故小发应选装置I;经过操作③(蒸馏)以后可得蒸馏水,不含有可溶性钙、镁化合物,因此再加入肥皂水时就看不到浮渣了,反而有许多泡沫。
10.答案:(1)玻璃棒
(2)铁和铜(或Fe和Cu);磁铁
(3)不能;
(4)
解析:(1)操作①和②都得到固体和液体,是过滤操作;操作④是由溶液得到晶体,是蒸发操作。过滤和蒸发都用到玻璃棒。
(2)固体A是铁、铜和过量的锌,加入适量氯化亚铁后,锌与氯化亚铁反应生成单质铁,故固体C是铁和铜。操作③可用磁铁吸引把铜和铁分离开来。
(3)固体A中加入氯化亚铁的目的是除去过量的锌,若用氯化铜溶液,铁也会与氯化铜反应,可能会导致铁又转化为盐而溶解。
(4)锌与氯化亚铁反应生成氯化锌和铁,反应的化学方程式为。
2022届中考化学复习增分策略题型专练08 工艺流程题(含答案): 这是一份2022届中考化学复习增分策略题型专练08 工艺流程题(含答案),共60页。试卷主要包含了海水的综合利用,提纯回收类,制备类,环境污染类等内容,欢迎下载使用。
2022年中考化学二轮复习热点专练03工艺流程题类: 这是一份2022年中考化学二轮复习热点专练03工艺流程题类,共18页。试卷主要包含了单选题,共12小题,填空题,共4小题,综合题,共3小题等内容,欢迎下载使用。
2022年中考化学二轮复习热点专练03工艺流程题类(2): 这是一份2022年中考化学二轮复习热点专练03工艺流程题类(2),共20页。试卷主要包含了单选题,共12小题,填空题,共4小题,流程题,共4小题等内容,欢迎下载使用。












