
2022届中考化学工艺流程题型专练(4)环境保护类
展开(4)环境保护类
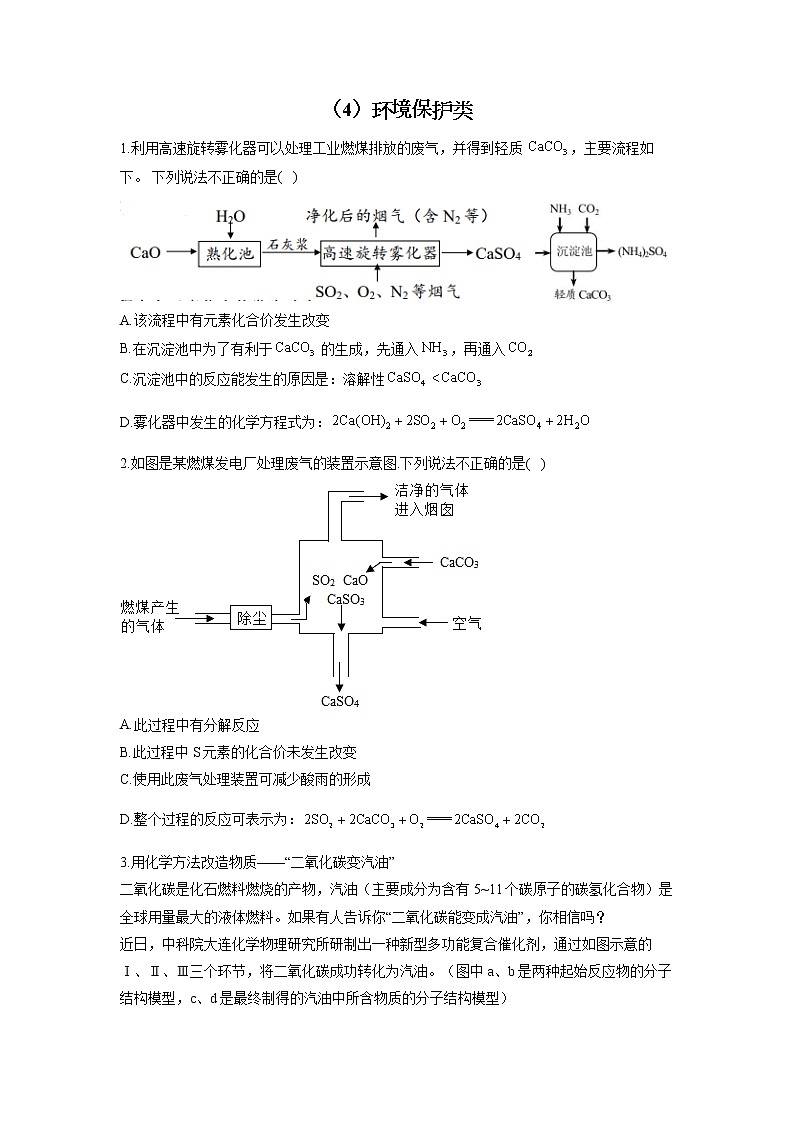
1.利用高速旋转雾化器可以处理工业燃煤排放的废气,并得到轻质 ,主要流程如下。 下列说法不正确的是( )
A.该流程中有元素化合价发生改变
B.在沉淀池中为了有利于 的生成,先通入,再通入
C.沉淀池中的反应能发生的原因是:溶解性
D.雾化器中发生的化学方程式为:
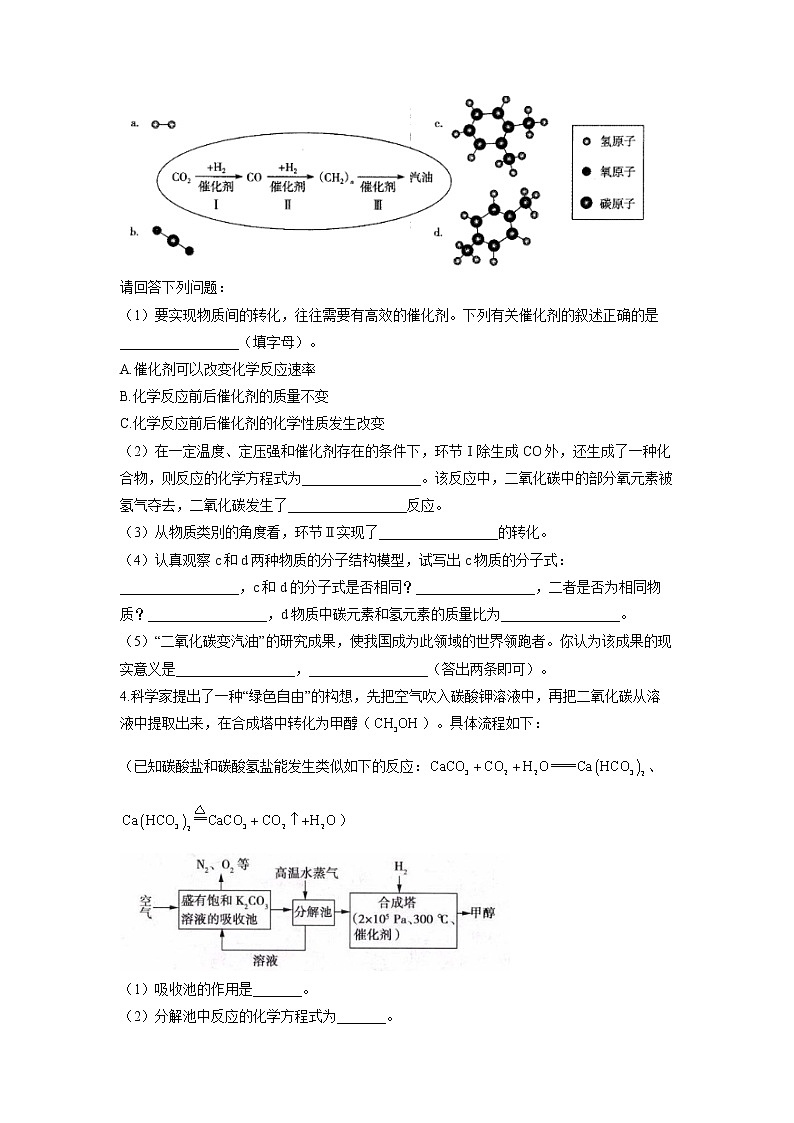
2.如图是某燃煤发电厂处理废气的装置示意图.下列说法不正确的是( )
A.此过程中有分解反应
B.此过程中S元素的化合价未发生改变
C.使用此废气处理装置可减少酸雨的形成
D.整个过程的反应可表示为:
3.用化学方法改造物质——“二氧化碳变汽油”
二氧化碳是化石燃料燃烧的产物,汽油(主要成分为含有5~11个碳原子的碳氢化合物)是全球用量最大的液体燃料。如果有人告诉你“二氧化碳能变成汽油”,你相信吗?
近日,中科院大连化学物理研究所研制出一种新型多功能复合催化剂,通过如图示意的Ⅰ、Ⅱ、Ⅲ三个环节,将二氧化碳成功转化为汽油。(图中a、b是两种起始反应物的分子结构模型,c、d是最终制得的汽油中所含物质的分子结构模型)
请回答下列问题:
(1)要实现物质间的转化,往往需要有高效的催化剂。下列有关催化剂的叙述正确的是_________________(填字母)。
A.催化剂可以改变化学反应速率
B.化学反应前后催化剂的质量不变
C.化学反应前后催化剂的化学性质发生改变
(2)在一定温度、定压强和催化剂存在的条件下,环节Ⅰ除生成CO外,还生成了一种化合物,则反应的化学方程式为_________________。该反应中,二氧化碳中的部分氧元素被氢气夺去,二氧化碳发生了_________________反应。
(3)从物质类別的角度看,环节Ⅱ实现了_________________的转化。
(4)认真观察c和d两种物质的分子结构模型,试写出c物质的分子式:_________________,c和d的分子式是否相同?_________________,二者是否为相同物质?_________________,d物质中碳元素和氢元素的质量比为_________________。
(5)“二氧化碳变汽油”的研究成果,使我国成为此领域的世界领跑者。你认为该成果的现实意义是_________________,_________________(答出两条即可)。
4.科学家提出了一种“绿色自由”的构想,先把空气吹入碳酸钾溶液中,再把二氧化碳从溶液中提取出来,在合成塔中转化为甲醇()。具体流程如下:
(已知碳酸盐和碳酸氢盐能发生类似如下的反应:、)
(1)吸收池的作用是_______。
(2)分解池中反应的化学方程式为_______。
(3)在合成塔中,与反应生成水和甲醇,写出合成塔中反应的化学方程式:_______。
(4)该流程中可以循环利用的物质(水除外)是_______。
(5)如果空气不经过吸收池和分解池,直接通入合成塔,从安全的角度考虑不可行,理由是_______。
5.矿山废水中含有大量的和,直接排放会影响水体酸碱性,并造成重金属污染。通过处理可以回收金属铜,并使废水的pH和重金属离子含量达到排放标准。
已知:步骤I中与并没有发生反应;属于一种常见的重金属盐。
(1)步骤I中发生反应的化学方程式为_______。
(2)废水①中一定含有的阳离子有_______。
(3)加入少量可以降低步骤Ⅱ中铁的消耗量,原因是_______。
(4)步骤Ⅲ中需加入才能使废水达到排放标准,由此推测废水③不达标的主要原因是其中还含有较多的_______(填离子符号);达标废水的pH比废水①的pH_______(填“大”或“小”)。
6.我国科技部制定发布了《“十二五”国家碳捕集利用与封存科技发展专项规划》,碳捕集、利用与封存技术可实现大规模二氧化碳减排。常利用NaOH溶液来“捕捉”,工艺过程如图所示(部分条件及物质未标出)。
(1)将工业生产中产生的含量高的气体吹瑞足量的NaOH溶液中来“捕捉”,则“捕捉室”中发生反应的化学方程式为________。
(2)在“分离室”中,将NaOH溶液与进行分离的基本操作是________。
(3)该流程图所标出的物质中,有一种氧化物溶于水放出大量的热,该反应的基本反应类型为________;将该氧化物加入X溶液中,发生反应的化学方程式为________。
(4)“碳捕捉”技术所捕捉到的可进行储存和利用,如制备的干冰常用于________;但该“碳捕捉”技术存在的一大缺点为________。
7.硫化钠是重要化工产品,主要用于皮革、毛纺、高档纸张、染料等行业。工业上利用工业尾气硫化氢制得产品硫化钠固体。其工业流程示意图如下图:
(1)图中A操作利用玻璃纤维作除尘分离塔的滤材,玻璃纤维的作用是过滤,该操作在实验室里要使用玻璃棒的作用为_____。
(2)硫化氢中硫元素的化合价为_____。硫化氢气体能溶于水,其水溶液呈酸性,称为氢硫酸,则其pH_____(填“<”、“>”或“=”)7。
(3)目前采用氢氧化钠溶液吸收工业尾气中的硫化氢,可减少空气污染。吸收塔中氢氧化钠溶液与硫化氢溶液发生硫化钠和水,写出该反应的化学方程式为_____,其基本类型为_____。
(4)产品硫化钠的物质类别属于_____(“酸”、“碱”、“盐”或“氧化物”)。硫化钠固体在空气中易氧化并易溶于水,保存硫化钠的正确方法为_____。
(5)硫化钠的溶解度随着温度升高明显增大。D操作中精制过程,从硫化钠的饱和溶液中分离出硫化钠晶体,采用的结晶方法是_____(填“蒸发溶剂”或“降温结晶”)。
8.绿色化学是指:利用化学技术和方法去减少或消灭那些对人体健康、社区安全、生态环境有害的原料、催化剂、溶剂和试剂、产物及副产物等的实用和生产。化学链燃烧是一种绿色的、高效的燃烧方式,燃料不直接与空气接触。下图是某科研组利用金属镍(Ni)进行化学链燃烧的流程图:
(1)空气反应器中,Ni在一定条件下转化成NiO的化学方程式为____________;
(2)燃料反应器中发生的部分化学反应如下:其中属于置换反应的是______(填序号);
①
②
(3)该流程中可以循环利用的物质是__________。
9.某发电厂附近海水中含有等物质,该工厂采用海水脱硫技术吸收燃煤烟气中的,其主要设备及流程如下图所示。
(1)含的烟气不经处理排放到空气中可能带来的环境问题是______。该工厂的处理方法无法大规模推广的原因是:______。
(2)吸收塔中让烟气从底部进入与自上而下的海水相向流动的原因是______。
(3)曝气池中的一种酸化合反应生成了硫酸,反应的化学方程式是______。
(4)稀释池中的由3变为7,主要原因是______(填离子符号)减少。
(5)空气中的浓度用的空气中所含的质量表示。我国对空气中的浓度级别规定如下
浓度级别 | 一级 | 二级 | 三级 |
标准 | 浓度0.15 | 0.15浓度0.50 | 0.50浓度0.70 |
将发电厂周围的空气通入含为为2.54mg的碘水中,经测定恰好完全反应(反应方程式为:)。则该空气中的浓度级别为______级。
10.某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如图所示:
资料1:垃圾焚烧产生的烟气中含有SO2等有害气体。
资料2:FeSO4容易被空气中的O2氧化。
回答下列问题:
(1)石灰浆吸收SO2(性质与CO2相似)的化学方程式为 。
(2)溶解步骤中同时发生的三个化学反应方程式为 Fe+Fe2(SO4)3=3FeSO4、 、 。
(3)将所得FeSO4溶液在氮气环境中蒸发浓缩、 、过滤,得到FeSO4晶体,其中氮气的作用是 。
(4)政府倡导垃圾分类,其好处是 (写一点)。
答案以及解析
1.答案:C
解析:C项,沉淀池中的反应能发生的原因是:溶解性,故C项错误; A项,由流程图中可知,石灰浆在高速旋转雾化器中与、反应生成,其中S元素与O元素的化合价发生改变,故A项正确; B项,在沉淀池中为了有利于的生成,通常先通入后通,目的是通入后溶液显碱性,有利于吸收,有利于的生成,故B项正确; D项,石灰浆在高速旋转雾化器中与、反应生成,发生的化学方程式为:,故D项正确。
2.答案:B
解析:A、由图可知,图中发生的反应有:氧化钙和二氧化硫反应生成亚硫酸钙,该反应符合“多变一”的特点,属于化合反应,碳酸钙高温煅烧生成氧化钙和二氧化碳,符合“一变多”的特点,属于分解反应,亚硫酸钙和氧气反应生成硫酸钙,符合“多变一”的特点,属于化合反应,不符合题意;
B、二氧化硫中硫元素显+4价,亚硫酸钙中硫元素显+4价,硫酸钙中硫元素显+6价,硫元素的化合价发生了改变,符合题意;
C、该过程可用氧化钙吸收二氧化硫,减少酸雨的形成,不符合题意;
D、由图可知,整个过程的反应为碳酸钙、二氧化硫和氧气反应生成硫酸钙和二氧化碳,该反应的化学方程式为:,不符合题意。
故选B。
3.答案:(1)AB
(2);还原
(3)无机物向有机物(或氧化物向碳氢化合物)
(4);是;不是;48:5
(5)有效降低造成的温室效应(合理即可);减少对传统化石能源的依赖(合理即可)
解析:(1)A项,催化剂可以改变化学反应速率,正确;B项,化学反应前后催化剂的质量不变,正确;C项,化学反应前后催化剂的化学性质不改变,错误。
(2)在一定温度、一定压强和催化剂存在的条件下,环节Ⅰ除生成CO外,还生成了一种化合物水,对应的化学方程式为。该反应中,二氧化碳中的
部分氧元素被氢气夺去,二氧化碳发生了还原反应。
(3)从物质类别的角度看,环节Ⅱ实现了无机物向有机物或氧化物向碳氢化合物的转化。
(4)观察c和d两种物质的分子结构模型,可知c、d物质的分子式都是;c和d的化学式相同但结构不同,故不属于同种物质;d物质中碳元素和氢元素的质量比为(12×8):(1×10)=48:5。
(5)“二氧化碳变汽油”的研究成果,可有效降低造成的温室效应,减少对传统化石能源的依赖。
4.答案:(1)吸收空气中的二氧化碳
(2)
(3)
(4)
(5)在300℃条件下,氢气与空气接触可能会引起爆炸
解析:(1)根据题给信息可知吸收池中加入碳酸钾溶液的作用是吸收空气中的二氧化碳。
(2)由题给信息可知,碳酸氢盐可在加热条件下发生分解反应,可写出相应的化学方程式。
(3)结合题图反应物、生成物及反应条件可写出相应的化学方程式。
(4)通过题给流程图可知碳酸钾既是反应物也是生成物,所以可循环利用的物质是。
(5)如果空气不经过吸收池和分解池,直接通入合成塔,在300℃条件下氢气与空气接触可能会引起爆炸。
5.答案:(1)
(2)和
(3)会与废水中的硫酸发生反应,消耗废水中的硫酸,减少铁与硫酸的反应
(4);大
解析:(1)步骤I中硫酸与氢氧化钙反应生成硫酸钙和水,化学方程式为。
(2)硫酸是由氢离子与硫酸根离子构成的,硫酸铜是由铜离子与硫酸根离子构成的,所以废水①中一定含有的阳离子是氢离子与铜离子。
(3)由题中信息可知,步骤I中加入的少量只与废水中的硫酸发生反应,这样就减少了铁与硫酸的反应,降低了铁的消耗量,使铁可以与硫酸铜充分反应。
(4)步骤Ⅱ中已经除去了大量的铜离子,但废水③仍不是达标废水。在步骤Ⅲ中加入后,生成CuS沉淀和达标废水,所以废水③不达标的主要原因是其中还含有较多的;经过处理,废水中的硫酸被除去,所以达标废水的pH比废水①的pH大。
6.答案:(1)
(2)过滤
(3)化合反应;
(4)人工降雨(合理即可);能耗大、成本高(合理即可)
解析:(1)二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,化学方程式为。
(2)在“分离室”中,将NaOH溶液与固体进行分离的基本操作是过滤。
(3)该氧化物为氧化钙,氧化钙与水反应生成氢氧化钙,符合“多变一”的特点,属于化合反应;X溶液为碳酸钠溶液,将氧化钙加入碳酸钠溶液中发生两个反应:氧化钙与水反应生成氢氧化钙,氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,据此书写化学方程式。
(4)干冰(固体二氧化碳)升华时吸收大量的热,可用于人工降雨等;通过图中一系列的反应可以看出,该“碳捕捉”技术的缺点是反应复杂且能耗大、成本高。
7.答案:(1)引流
(2)-2;
(3);复分解反应
(4)盐;采用密封、阴凉、防水等保存方法
(5)降温结晶
解析:(1)过滤需要玻璃棒引流,故玻璃纤维的作用是过滤,该操作在实验室里要使用玻璃棒的作用为引流。
(2)硫化氢的化学式为,氢元素的化合价为+1价,设硫元素的化合价为x,化合物中各元素的正负化合价代数和为0,,,故硫元素的化合价为-2价。硫化氢气体能溶于水,其水溶液呈酸性,称为氢硫酸,则其pH<7。
(3)吸收塔中氢氧化钠溶液与硫化氢溶液发生硫化钠和水,该反应的化学方程式为,反应符合两种化合物相互交换成分生成另两种化合物,故其基本类型为复分解反应。
(4)硫化钠是硫离子和钠离子构成的,故产品硫化钠的物质类别属于盐。硫化钠固体在空气中易氧化并易溶于水,保存硫化钠的正确方法为采用密封、阴凉、防水等保存方法。
(5)硫化钠的溶解度随着温度升高明显增大。D操作中精制过程,从硫化钠的饱和溶液中分离出硫化钠晶体,采用的结晶方法是降温结晶。
8.答案:(1)
(2)①
(3)Ni
解析:(1)由题图可以看出,在空气反应器中,进入的是金属镍,问时还有空气,但是空气中的氨气被分流排除了,所以是氧气参加了反应,生成物质是NiO,则金属镍与氧气在一定条件下发生燃烧的化学方程式为。
(2)反应①是单质和化合物反应生成新的单质和新的化合物,属于置换反应。
(3)该反应中能循环利用的物质是Ni。
9.答案:酸雨;流程中需要大量的海水,不能在内陆地区使用 增大使烟气与海水的接触面积和接触时间使反应更快更充分;;;三
解析:(1)二氧化硫和空气中水反应生成酸性物质导致酸雨,故含SO2的烟气不经处理排放到空气中可能带来的环境问题是酸雨。该工厂的处理方法无法大规模推广的原因是流程中需要大量的海水,不能在内陆地区使用。
(2)吸收塔中让烟气从底部进入与自上而下的海水相向流动的原因是增大反应物间的接触面积和接触时间,使反应更充分。
(3)化合反应是多种物质生成一种物质的反应,由流程图可知,反应后酸性变强,且有氧气参与,故曝气池中的一种酸化合反应生成了硫酸的反应为。
(4)pH>7溶液显碱性,pH=7溶液显中性,pH<7溶液显酸性;稀释池中的由3变为7,酸性变为中性,故主要原因是减少。
(5)设该空气中的质量为
故该空气中的浓度级别为三级。
10.答案:(1)Ca(OH)2+SO2=CaSO3↓+H2O
(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;Fe+H2SO4=FeSO4+H2↑
(3) 降温结晶; 防止硫酸亚铁被氧化
(4) 保护环境
解析:(1)氢氧化钙与二氧化硫反应生成亚硫酸钙和水。
(2)溶解过程中,铁锈的成分氧化铁与稀硫酸反应生成硫酸铁和水,铁能与稀硫酸反应生成硫酸亚铁和氢气。
(3)要得到FeSO4晶体,可以将所得FeSO4溶液在氮气环境中蒸发浓缩、降温结晶、过滤,其中氮气的化学性质稳定,能防止硫酸亚铁被氧化。
(4)垃圾分类能起到保护环境的作用。
专题1环境保护类工艺流程题-中考化学热点预测工艺流程题微专题(全国通用): 这是一份专题1环境保护类工艺流程题-中考化学热点预测工艺流程题微专题(全国通用),文件包含专题1环境保护类工艺流程题-中考化学热点预测工艺流程题微专题全国通用解析版docx、专题1环境保护类工艺流程题-中考化学热点预测工艺流程题微专题全国通用原卷版docx等2份试卷配套教学资源,其中试卷共15页, 欢迎下载使用。
2022届中考化学复习增分策略题型专练08 工艺流程题(含答案): 这是一份2022届中考化学复习增分策略题型专练08 工艺流程题(含答案),共60页。试卷主要包含了海水的综合利用,提纯回收类,制备类,环境污染类等内容,欢迎下载使用。
(4)变质类探究——2022届中考化学科学探究题型专练: 这是一份(4)变质类探究——2022届中考化学科学探究题型专练,共11页。试卷主要包含了00g等内容,欢迎下载使用。












