




初中化学沪教版九年级下册第7章 应用广泛的酸、碱、盐综合与测试课时练习
展开
这是一份初中化学沪教版九年级下册第7章 应用广泛的酸、碱、盐综合与测试课时练习,文件包含第7章应用广泛的酸碱盐综合测评卷-2021-2022学年九年级化学下册精品课堂课同步检测卷沪教版解析版docx、第7章应用广泛的酸碱盐综合测评卷-2021-2022学年九年级化学下册精品课堂课同步检测卷沪教版原卷版docx等2份试卷配套教学资源,其中试卷共16页, 欢迎下载使用。
可能用到的相对原子质量:H-1 C-12 O-16 Ca-40
一、单选题(每小题3分,共48分)
1.分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液,观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色。则它们的pH由小到大的排列是( )
A.甲、乙、丙B.甲、丙、乙
C.乙、甲、丙D.丙、甲、乙
【答案】B
2.下列关于氢氧化钠的描述中不正确的是( )
A.曝露在空气中易潮解B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红D.对皮肤有强烈的腐蚀作用
【答案】C
3.下列为一些常见食物的近似pH,胃酸过多的人空腹时最适宜吃的食物是( )
A.苹果:2.9~3.3B.橘子:3.0~4.0
C.葡萄:3.5-4.5D.玉米粥:6.8~8.0
【答案】D
4.氯化钠是一种常见的化学物质。下列说法不正确的是( )
A.氯化钠是常见的食品调味剂B.氯化钠可用于生产氯气、烧碱
C.蒸发海水即可获得纯净的氯化钠固体D.氯化钠可用于腌制食品
【答案】C
5.按一定标准对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,符合“氧化物、酸、碱、盐”顺序排列的是( )
A.HClO、H2CO3、Mg(OH)2、MgCl2B.CO2、HCl、CaCO3、Na2SO4
C.H2O、HNO3、Ca(OH)2、NH4ClD.SO3、NaHSO4、NaOH、Ca(HCO3)2
【答案】C
用一种试剂来鉴别NaCl、Ca(OH)2、稀H2SO4三种溶液,可以选用下列物质中的( )
A.紫色石蕊试液B.无色酚酞试液
C.铁粉D.二氧化碳
【答案】A
7.化肥对提高农作物的产量具有重要作用。下列化肥中,属于复合肥的是( )
A.KNO3B.CO(NH2)2
C.K2CO3D.Ca3(PO4)2
【答案】A
8.下列各组物质,要借助酸碱指示剂才能判断反应发生的是( )
A.石灰石与盐酸B.NaOH+HCl
C.BaCl2+H2SO4D.Fe2O3+HCl
【答案】B
9.下列常用来改良酸性土壤的物质是( )
A.熟石灰B.硫酸
C.烧碱D.食盐
【答案】A
10.黄蜂的毒液呈碱性,若被黄蜂蜇了,涂抹下列物质可缓解疼痛的是( )
A.食盐水(pH≈7 )B.牙膏(pH≈9)
C.肥皂(pH≈10 )D.米醋(pH≈3)
【答案】D
11.张亮同学在实验室中测定某未知溶液的pH,他的实验操作如下:先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取待测试液于pH试纸上进行测定,你认为张亮同学这样测得的结果与该溶液的实际pH比较( )
A.不变B.偏低
C.偏高D.无法判断
【答案】D
12.有关物质之间的部分转化关系如图所示。其中“—”表示物质之间能发生化学反应,“→”表示物质之间的转化关系。下列说法中正确的是( )
物质X是一种常见的酸
B.反应②一定有盐参加
C.图中的所有反应均不属于置换反应
D.向 Ca(OH)2溶液中加入 CaO,所得溶液的溶质质量分数一定增大
【答案】C
13.向一定量的硫酸铜和稀硫酸的混合溶液中滴加氢氧化钠溶液,反应过程中产生的沉淀质量与加入的氢氧化钠溶液质量关系如下图所示。下列说法不正确的是( )
A.A点溶液中的溶质有2种B.E点溶液中的溶质有3种
C.AB段有沉淀生成D.F点溶液的pH>7
【答案】B
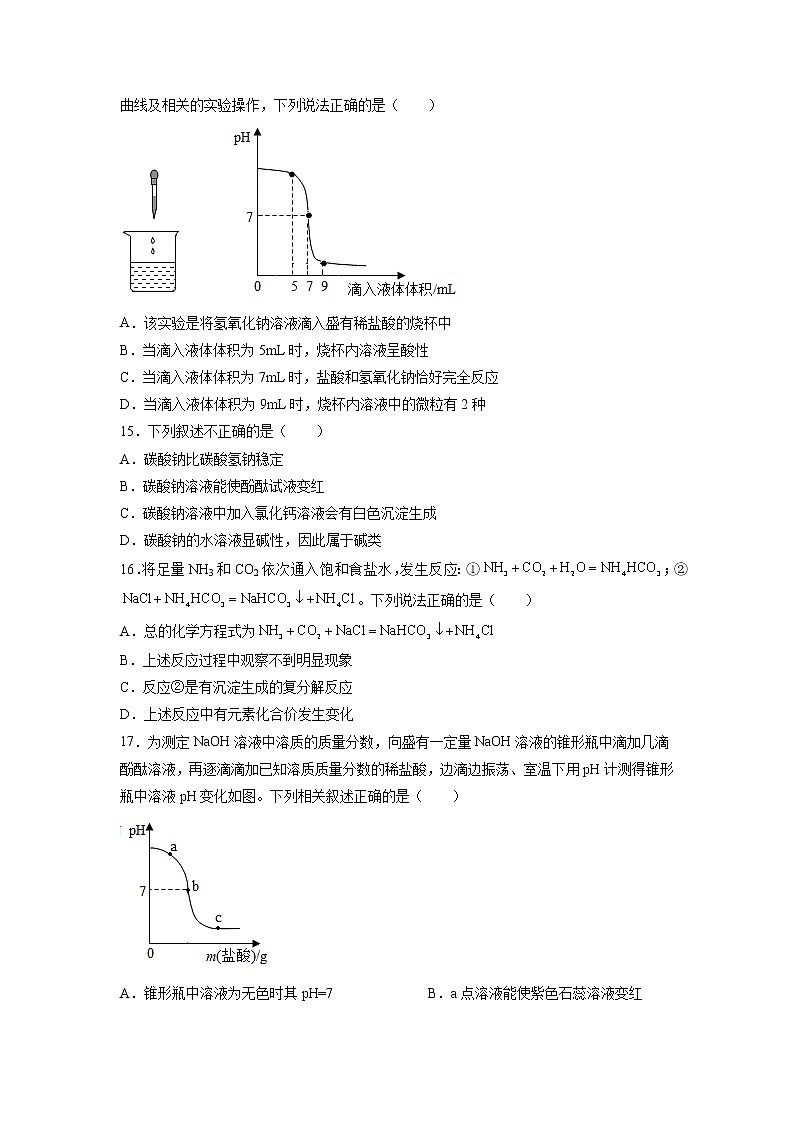
14.如图表示稀盐酸和氢氧化钠溶液发生反应时,烧杯中溶液的pH随滴入液体体积的变化曲线及相关的实验操作,下列说法正确的是( )
A.该实验是将氢氧化钠溶液滴入盛有稀盐酸的烧杯中
B.当滴入液体体积为5mL时,烧杯内溶液呈酸性
C.当滴入液体体积为7mL时,盐酸和氢氧化钠恰好完全反应
D.当滴入液体体积为9mL时,烧杯内溶液中的微粒有2种
【答案】C
15.下列叙述不正确的是( )
A.碳酸钠比碳酸氢钠稳定
B.碳酸钠溶液能使酚酞试液变红
C.碳酸钠溶液中加入氯化钙溶液会有白色沉淀生成
D.碳酸钠的水溶液显碱性,因此属于碱类
【答案】D
16.将足量NH3和CO2依次通入饱和食盐水,发生反应:①;②。下列说法正确的是( )
A.总的化学方程式为
B.上述反应过程中观察不到明显现象
C.反应②是有沉淀生成的复分解反应
D.上述反应中有元素化合价发生变化
【答案】C
17.为测定NaOH溶液中溶质的质量分数,向盛有一定量NaOH溶液的锥形瓶中滴加几滴酚酞溶液,再逐滴滴加已知溶质质量分数的稀盐酸,边滴边振荡、室温下用pH计测得锥形瓶中溶液pH变化如图。下列相关叙述正确的是( )
A.锥形瓶中溶液为无色时其pH=7 B.a点溶液能使紫色石蕊溶液变红
C.b点时盐酸与NaOH恰好完全反应D.c点溶液的溶质有NaCl和NaOH
【答案】C
18.向一定量盐酸和氯化钙混合溶液中逐滴加入碳酸钠溶液,用数字化实验设备测得溶液pH变化情况如图。下列有关说法错误的是( )
A.AB段反应现象为有气泡产生
B.BC段反应现象为有白色沉淀生成
C.CD段溶液中含有的溶质为碳酸钠和氯化钙
D.CD段溶液pH大于7是因碳酸钠溶液显碱性
【答案】C
第 = 2 \* ROMAN \* MERGEFORMAT II卷(非选择题 共46分)
二、填空题(本大题共5个小题,共46分)
19.以碳酸钠溶液为例的反应关系(如下图)体现了盐类物质的化学性质,结合此图回答问题:
(1)碳酸钠俗称________或_______。
(2)反应①的化学方程式为__________。
(3)为了验证性质②将碳酸钠溶液与酚酞溶液混合,溶液由无色变为______,证明碳酸钠溶液显______(填“酸”或“碱”)性。
(4)反应③和④的基本反应类型为_______。
(5)反应⑤将二氧化碳通入碳酸钠溶液会生成碳酸氢钠,该反应的化学方程式为_______。
【答案】(1) 纯碱 ; 苏打 ;(2);(3)红; 碱 ;(4)复分解反应;(5)Na2CO3+H2O+CO2=2NaHCO3
20.自然界中,有许多植物色素在不同的酸碱性溶液中呈现不同的颜色,这些植物色素也可以作为酸碱指示剂。自制酸碱指示剂可用到以下仪器:
(1)仪器a的名称为_______。
(2)从紫甘蓝叶中提取植物色素的操作步骤如下:
①取适量紫甘蓝叶放在研钵中研碎;
②用水和酒精(体积比1:1)浸泡,_______(填“过滤”或“蒸发”),取液备用;
③将紫甘蓝提取液分别滴入白醋、石灰水、蒸馏水中,颜色变化如下表:
(3)请用紫甘蓝提取液,选用题中给出的仪器,用最少量的试剂鉴别失去标签的稀盐酸和氢氧化钠溶液。写出你的实验操作过程及结论。
【答案】(1)烧杯 (2)过滤 (3)各取几滴待测液于点滴板上,分别滴加几滴紫甘蓝提取液,显红色者为稀盐酸,显绿色者为氢氧化钠溶液
21.综合复习时,同学们又来到化学实验室进行实验,加强对酸的化学性质的整体认识。他们将适量的稀盐酸分别滴加到六只试管中进行实验(如图所示),请回答下列问题:
(1)上述六只试管中有气泡产生的是______(填序号),相关反应的化学方程式为_______(只写出一个)。
(2)能证明“C试管中发生了化学反应”的现象是____________。
(3)有一只试管中的物质不与稀盐酸反应,原因是________。
【答案】 (1)BD ;或NaHCO3+HCl=NaCl+CO2↑+H2O;(2)溶液由红色变为无色;(3)在金属活动顺序中铜位于氢后面,所以不与稀盐酸反应
22.图1是关于氢氧化钠化学性质的思维导图,请据图回答问题。
(1)性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈______色。
(2)性质②,将氢氧化钠溶液滴入稀盐酸中、图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是______(填化学式)。
(3)依据性质③,除去硫酸厂在生产过程中产生的二氧化硫气体,化学方程式为______。
(4)性质④,将氢氧化钠固体和某种盐混合研磨,能放出有刺激性气味的气体。推测这种盐可能是______。
【答案】红 NaCl、NaOH 铵盐
23.有一包固体物质,可能含有硫酸钠、碳酸钠、氯化钙、氯化钾、氯化铁和氢氧化钠中的一种或几种。为探究这包固体物质组成,进行了以下实验。
(1)据①可知固体中一定不含有______。
(2)取白色沉淀B于烧杯中并逐滴加入稀硝酸,烧杯中沉淀质量随滴加稀硝酸质量的变化如图乙所示,由此确定原固体中一定含有______。
(3)取无色溶液C向其中通入二氧化碳气体,产生白色沉淀, 无色溶液C中一定含有的离子是______ (填离子符号)。
(4)为确定原固体中可能含有的物质是否存在的实验方案是______ (写明操作、现象和结论)。
【答案】氯化铁(或FeCl3) 碳酸钠和硫酸钠(或:Na2CO3和Na2SO4) 取适量无色溶液C于试管中,加入硝酸银溶液,再加入过量的稀硝酸,仍然有白色沉淀,证明有氯化钾。
三、实验探究题(本大题共1个小题,共12分)
22.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入稀盐酸一会后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。
Ⅰ、写出该中和反应的化学方程式:___________。
Ⅱ、探究烧杯内溶液中溶质的成分。
(提出问题)该烧杯内溶液中的溶质是什么?
(猜想)猜想一:可能是CaCl2和Ca(OH)2;
猜想二:可能只有CaCl2;
猜想三:___________。
(查阅资料)氯化钙溶液呈中性。
(进行实验)
(反思与拓展)
(1)实验步骤2中产生白色沉淀的化学方程式为___________。
(2)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是___________(写一条)。
(3)要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的一种物质,该物质可以是___________(写化学式)
【答案】Ca(OH)2+2HCl=CaCl2+2H2O 可能是CaCl2和HCl 溶液不变红色 先有气泡产生CaCl2+Na2CO3=CaCO3↓+2NaCl 腐蚀铁质下水管或污染水源 CaCO3
四、计算题(本大题共1个小题,共10分)
23.某化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。请根据以上信息回答下列问题:
(1)写出反应的化学方程式 ;
(2)该反应中产生二氧化碳的总质量为 g;
(3)列出求解该样品中参加反应的碳酸钙质量(x)的比例式 ;
(4)石灰石样品中碳酸钙的质量分数为 ;
(5)某同学想用上述石灰石样品250t,可制得含杂质的生石灰的质量是 。
【答案】(1)(2)8.8(3)20g(4)80%(5)162t
【解析】(1)石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:;(2)根据质量守恒定律,化学反应前后,物质的总质量不变,生成二氧化碳的质量为:
25g+100g+110.8g﹣227g=8.8g;
(3)解:设该样品中参加反应的碳酸钙质量为x
x=20g
(4)故石灰石样品中碳酸钙的质量分数为;
(5)解:设生成二氧化碳的质量是y
y=88t
故可制得含杂质的生石灰的质量为250t-88t=162t。物质
白醋
石灰水
蒸馏水
显色情况
红色
绿色
蓝色
实验步骤
实验现象
实验结论
步骤1:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡。
___________。
猜想一不正确
步骤2:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量。
___________,过一会有白色沉淀产生。
猜想二不正确,猜想三正确
相关试卷
这是一份初中化学沪教版九年级下册第6章 溶解现象综合与测试当堂检测题,文件包含第6章溶解现象综合测评卷-2021-2022学年九年级化学下册精品课堂同步检测卷沪教版解析版docx、第6章溶解现象综合测评卷-2021-2022学年九年级化学下册精品课堂同步检测卷沪教版原卷版docx等2份试卷配套教学资源,其中试卷共19页, 欢迎下载使用。
这是一份初中化学沪教版九年级下册第9章 化学与社会发展综合与测试同步达标检测题,文件包含第9章化学与社会发展综合测评卷-2021-2022学年九年级化学下册精品课堂课同步检测卷沪教版解析版docx、第9章化学与社会发展综合测评卷-2021-2022学年九年级化学下册精品课堂课同步检测卷沪教版原卷版docx等2份试卷配套教学资源,其中试卷共13页, 欢迎下载使用。
这是一份综合复习与测试卷(综合测评卷)-2021-2022学年九年级化学下册精品课堂课同步检测卷(沪教版)·,文件包含综合复习与测试卷综合测评卷-2021-2022学年九年级化学下册精品课堂课同步检测卷沪教版解析版docx、综合复习与测试卷综合测评卷-2021-2022学年九年级化学下册精品课堂课同步检测卷沪教版原卷版docx等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。










