





2021学年第二节 金属的化学性质授课课件ppt
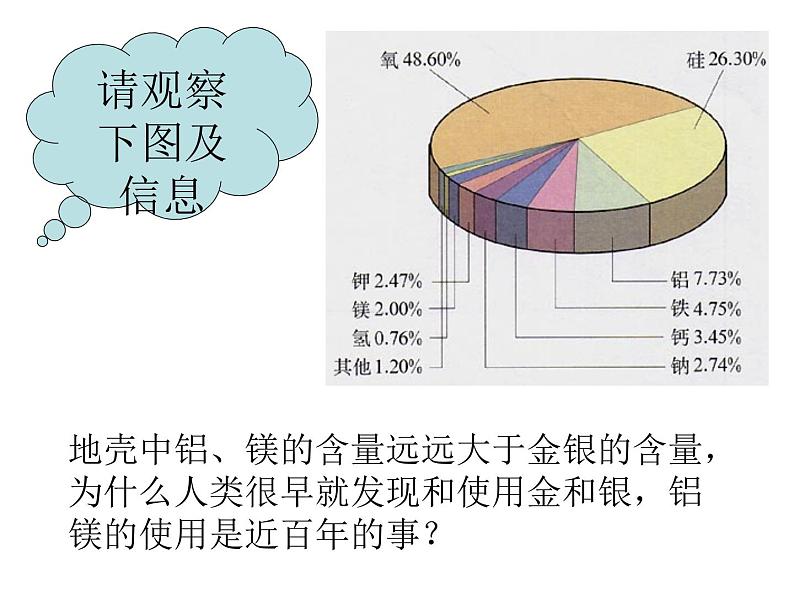
展开金 属 的 化 学 性 质
写出上述反应的化学方程式:
俗语“真金不怕火炼”说明什么?
小结:1、镁条和铝片在常温下就能和空气中的氧气发生氧化反应。
4Al+3O2=2Al2O3 2Mg+O2=2MgO
2、铜片和铁丝在高温时能与氧气反应。
1.大多数金属都能与___反应,反应剧烈程度 ____(相同,不相同);
2.金属的活动性:说明 _______ 较活泼,________次之, ______很不活泼
活动性顺序为:Mg、Al>Fe>Cu>Au
(2)为何不宜用钢刷来擦洗铝制餐具呢?
若用钢刷擦洗铝制品,容易把氧化薄膜除掉,从而起不到保护作用。
金属铝在常温下发生缓慢氧化, 形成一层致密的氧化物薄膜,从而阻止铝的进一步氧化,因而铝具有较好的抗腐蚀性。
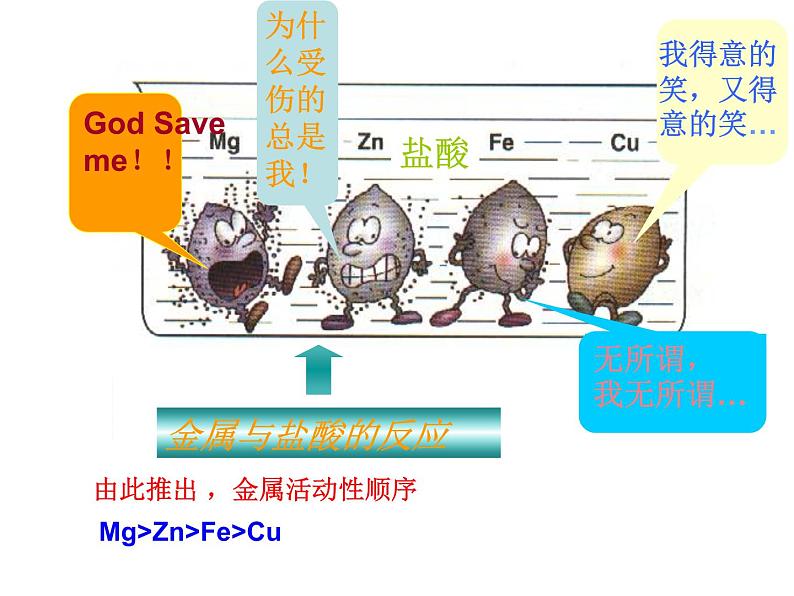
在试管中分别加入少量镁带、锌粒、铜片、铁钉,再分别加少量稀盐酸,观察各组物质是否反应,有没有气泡,有没有放热现象,反应速度。
相 信 你 会 做
由此推出 ,金属活动性顺序
Mg>Zn>Fe>Cu
Mg + H2 SO4 == MgSO4 + H2 ↑
Mg + 2HCl == MgCl2 + H2 ↑
Zn + H2 SO4 == Zn SO4 + H2 ↑
Zn + 2HCl == ZnCl2 + H2 ↑
Fe + H2 SO4 == Fe SO4 + H2 ↑
Fe + 2HCl == FeCl2 + H2 ↑
剧烈反应,产生大量气泡
反应缓慢,有气泡产生,溶液由无色变为浅绿色
1、将下列金属与稀盐酸接触,无气泡产生的是( )A.Fe B.Mg C.Zn D.Cu2、下列反应不属于置换反应的是( )A.Zn+H2SO4==ZnSO4+H2↑ B.CO+CuO = Cu+CO2C.C+2CuO==2Cu+CO2↑ D.Fe+CuSO4==FeSO4+Cu
在试管中分别加入少量铁丝,再分别加少量硫酸铜溶液,观察各组物质是否反应,并说出反应现象。
Fe + CuSO4 ==== FeSO4 + Cu
现象:铁钉表面有红色物质生成,蓝色溶液变成浅绿色
实验一:说明___的活动性强于_____
2Al + 3 CuSO4 == Al2( SO4)3+ 3Cu
Cu + 2AgNO3 == Cu(NO3)2 + 2Ag
实验二:说明 ____的活动性强于 _____
实验三:说明_____的活动性弱于_____
结论:金属活动性顺序__________________________
三、金属与化合物溶液的反应
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
1.在金属活动性顺序里:金属的位置越 ______ ,它的活动性就越强。
2.通过实验一,你能得出,在金属活动性顺序里:位于 ____ 前面的金属才能与盐酸、稀硫酸反应。
3.通过实验二,你能得出,在金属活动性顺序里:位于_____ 的金属能与位于____ 的金属化合物溶液反应。
(K、Ca、Na除外!)
(我们把氢前的金属称为活泼金属,氢后的金属称为不活泼金属。)
一种_____和一种______反应,生成另一种_____和另一种 _____ 的反应叫做置换反 应
讨论:下列反应方程式有何共同特征?
Mg + H2 SO4 == MgSO4 + H2 ↑ Zn + H2 SO4 == Zn SO4 + H2 ↑Fe + 2HCl == FeCl2 + H2 ↑Fe + Cu SO4 == Fe SO4 + Cu
你还能举出哪些置换反应的例子吗?
2. C + 2CuO 高温 2Cu+CO2 ↑
3. H2 + CuO 加热 H2O + Cu
1.Zn + 2HCl == ZnCl2 + H2 ↑
初中北京课改版第二节 金属的化学性质课前预习ppt课件: 这是一份初中北京课改版第二节 金属的化学性质课前预习ppt课件,共23页。PPT课件主要包含了金属材料的发展,铝有很好的抗腐蚀性能,金属与氧气的反应,镁条燃烧,铁丝燃烧,铜片在空气中加热,镁与盐酸,锌与盐酸,铁与盐酸,铜与盐酸等内容,欢迎下载使用。
初中化学北京课改版九年级下册第10章 金属第二节 金属的化学性质教课内容课件ppt: 这是一份初中化学北京课改版九年级下册第10章 金属第二节 金属的化学性质教课内容课件ppt,共18页。PPT课件主要包含了订正作业教师介绍,金属于氧气的反应,不相同,MgAl,FeCu,无变化,反应的剧烈程度如何,氢气H2,铜Cu,化合物等内容,欢迎下载使用。
2021学年第10章 金属第二节 金属的化学性质多媒体教学ppt课件: 这是一份2021学年第10章 金属第二节 金属的化学性质多媒体教学ppt课件,共31页。PPT课件主要包含了活动天地,高温炼金,思考讨论,说明金化学性质稳定,金属与氧气的反应,不反应,无所谓我无所谓,为什么受伤的总是我,实验现象,探究结论等内容,欢迎下载使用。













