

所属成套资源:高考化学一轮复习成套课时学案
高考化学一轮复习第2章物质及其变化第1讲物质的分类及转化学案
展开这是一份高考化学一轮复习第2章物质及其变化第1讲物质的分类及转化学案,共11页。
第1讲 物质的分类及转化
[课程标准]
1.认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类。
2.认识同类物质具有相似的性质,一定条件下各类物质可以相互转化。
3.能利用电离、离子反应、氧化还原反应等概念对常见的反应进行分类和分析说明。
4.能从物质类别、元素价态的角度,依据复分解反应和氧化还原反应原理,预测物质的化学性质和变化。
5.认识胶体是一种常见的分散系,能举例说明胶体的典型特征。
考点一 物质的组成与分类
1.物质的组成
(1)理解几组概念
名称 | 含义 |
原子、分 子和离子 | ①原子是化学变化中的最小微粒。 ②分子是保持物质化学性质的最小微粒,一般分子由原子通过共价键构成,但稀有气体是单原子分子,不存在化学键。 ③离子是带电荷的原子或原子团 |
元素 | 具有相同核电荷数(即质子数)的同一类原子的总称,在自然界中存在游离态和化合态两种形式 |
单质和 化合物 | ①单质是由同种元素组成的纯净物。 ②化合物是由不同种元素组成的纯净物 |
纯净物和 混合物 | ①纯净物:由同种单质或化合物组成的物质。 ②混合物:由几种不同的单质或化合物组成的物质 |
同素异 形体 | 由同种元素形成的几种性质不同的单质。物理性质差别较大;同素异形体之间的转化属于化学变化 |
[点拨] ①只含一种元素的物质不一定是单质,如O2和O3的混合物、金刚石和石墨的混合物等。只含一种元素的纯净物才是单质。
②常见的混合物
a.气体混合物:空气、水煤气(CO和H2)、爆鸣气(H2和O2)、天然气(主要成分是CH4)、焦炉气(主要成分是H2和CH4)、高炉煤气、石油气、裂解气。
b.液体混合物:氨水、氯水、王水、天然水、水玻璃、福尔马林、浓硫酸、盐酸、汽油、植物油、胶体。
c.固体混合物:大理石、碱石灰、漂白粉、高分子、玻璃、水泥、合金、铝热剂。
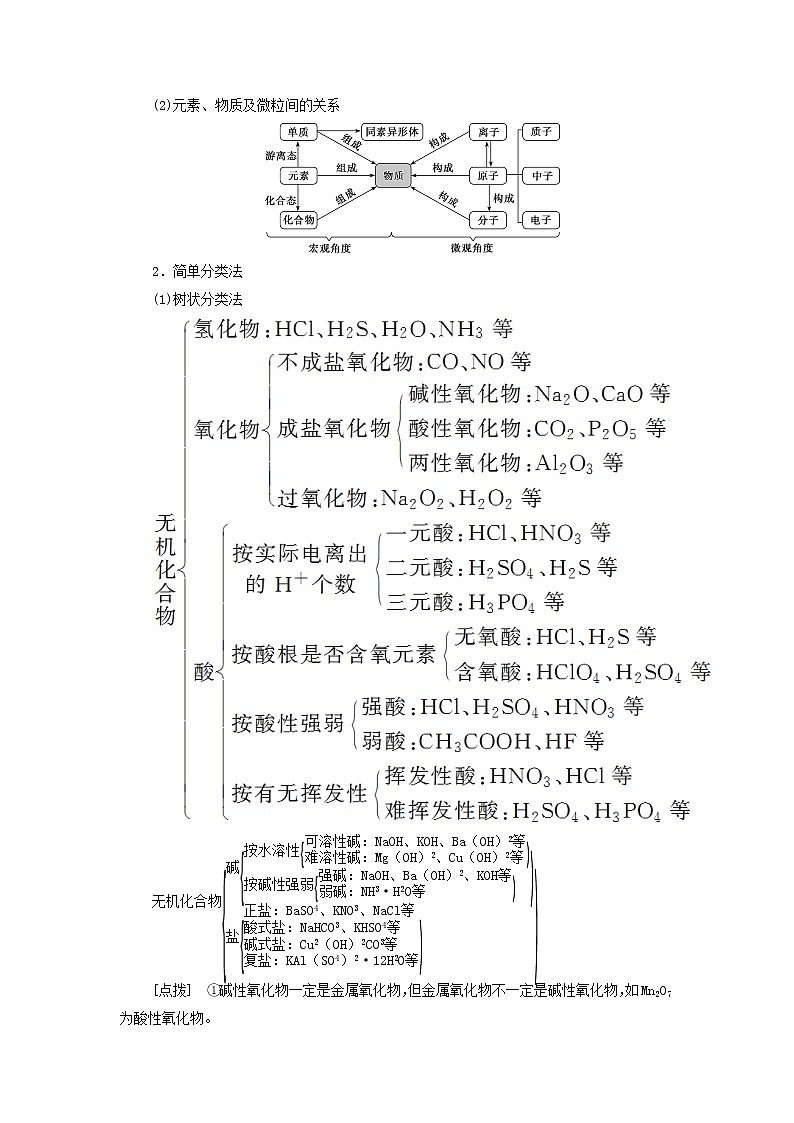
(2)元素、物质及微粒间的关系
2.简单分类法
(1)树状分类法
[点拨] ①碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物,如Mn2O7为酸性氧化物。
②酸性氧化物不一定是非金属氧化物,如Mn2O7;非金属氧化物也不一定是酸性氧化物,如CO、NO。
③酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱,如SiO2、Fe2O3。
(2)交叉分类法——从不同角度对物质进行分类
应用示例如下:
题组一 物质的组成
1.(2021·益阳高三调研)《神农本草经》记载:“水银……熔化(加热)还复为丹。”《黄帝九鼎神丹经》中的“柔丹”“伏丹”都是在土釡中加热Hg制得的。这里的“丹”指的是( )
A.合金 B.氧化物
C.氯化物 D.硫化物
解析:选B。汞和空气中的氧气在加热条件下发生反应生成氧化汞,故为氧化物。
2.化学与社会、生活联系密切。下列有关说法不正确的是( )
A.天然气、沼气、液化石油气都是清洁能源,它们的主要成分都是烃类
B.加碘食盐中添加的含碘物质是KI
C.碘酒、“84”消毒液、75%的酒精都可用于消毒
D.生活中常用的淀粉、蔗糖、葡萄糖的组成元素相同
解析:选B。天然气、沼气的主要成分是甲烷,液化石油气的主要成分是丙烷和丁烷,都属于烃类,A项正确;加碘食盐中添加的含碘物质是KIO3,B项错误;“84”消毒液的有效成分是次氯酸钠,碘酒、“84”消毒液、75%的酒精都可用于消毒,C项正确。
题组二 物质的分类
3.(2019·浙江4月选考)下列属于碱的是( )
A.C2H5OH B.Na2CO3
C.Ca(OH)2 D.Cu2(OH)2CO3
解析:选C。C2H5OH属于醇,Na2CO3属于盐,Ca(OH)2属于碱,Cu2(OH)2CO3属于碱式盐,故选C。
4.下列各物质所属类别的判断均正确的一组是( )
选项 | 混合物 | 碱 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | 液氨 | 苛性钠 | 胆矾 | 氧化铁 | 二氧化碳 |
B | 纯盐酸 | 烧碱 | 食盐 | 氧化钠 | 二氧化氮 |
C | “84”消毒液 | 纯碱 | 石灰石 | 氨 | 水 |
D | 聚乙烯塑料 | 熟石灰 | 苏打 | 生石灰 | 二氧化硫 |
解析:选D。A中的液氨是液态氨,属于纯净物,A错误;B中的二氧化氮不是酸性氧化物(不是对应酸的酸酐),B错误;C中的纯碱是碳酸钠,不属于碱,氨为氢化物,不是氧化物,水与碱不反应,不属于酸性氧化物,C错误;D中的物质所属类别均正确,D正确。
对物质正确分类的关键——明确分类标准
考点二 物质的性质与变化
1.物质的性质与变化的相关概念及关系
[点拨] 原子是化学变化中的最小微粒,原子核遭到破坏的过程不属于化学变化,核裂变、核聚变虽有新物质生成,但均不属于化学变化。
2.常见的物理变化和化学变化
| 物理变化 | 化学变化 |
三馏 | 分馏、蒸馏 | 干馏 |
三色 | 焰色试验 | 显色反应、指示剂变色反应 |
五解 | 潮解 | 分解、电解、水解、裂解 |
十八化 | 熔化、汽化、 液化、升华 | 氢化、氧化、水化、风化、炭化、钝化、煤的气化、煤的液化、皂化、歧化、卤化、硝化、酯化、裂化 |
[点拨] (1)升华、萃取、分液、吸附、盐析、金属导电、电离、渗析等均为物理变化。
(2)脱水、蛋白质变性、同素异形体互变、熔融盐导电、电解质溶液导电等均为化学变化。
3.化学反应的分类
4.单质、氧化物、酸、碱、盐的转化关系
题组一 物理变化和化学变化
1.(2021·广东省选择考模考)“古诗文经典已融入中华民族的血脉”。下列诗文中隐含化学变化的是( )
A.月落乌啼霜满天,江枫渔火对愁眠
B.掬月水在手,弄花香满衣
C.飞流直下三千尺,疑是银河落九天
D.举头望明月,低头思故乡
解析:选A。A.“渔火”为物质燃烧发的光,燃烧属于化学变化,A符合题意;B.捧起泉水、月影倒映在水中、花香溢满衣衫均描述的是物理变化,B与题意不符;C.“飞流直下三千尺”为水的自由落体运动,为物理变化,C与题意不符;D.“举头望明月”,月光为反射的太阳光,为物理变化,D与题意不符。
2.下列各组变化中,前者是物理变化,后者是化学变化的是( )
A.碘的升华、石油的分馏
B.用NH4Cl溶液除铁锈、食盐水导电
C.蛋白质溶液中加饱和(NH4)2SO4溶液、蓝色的胆矾常温下变白
D.热的饱和KNO3溶液降温析出晶体、用二硫化碳洗涤试管内壁上的硫
解析:选C。选项A、D都是物理变化,不符合题意。选项B,前者是化学变化,电解质溶液的导电过程就是电解的过程,电解必然会产生新物质,故食盐水导电是化学变化,不符合题意。选项C,蛋白质的盐析是物理变化;胆矾变白,说明胆矾失去结晶水,发生的是化学变化,符合题意。
题组二 化学反应类型及物质的转化
3.下图是某反应在密闭容器中反应前后的分子状况示意图,“”和“”分别表示不同的原子。下列对该过程的相关描述正确的是( )
A.有一种物质过量 B.发生的是分解反应
C.发生的是置换反应 D.生成了两种产物
解析:选A。由题图可知,该反应为与化合生成了,而反应物过量。
4.盐是一种常见的物质,下列物质通过反应可直接形成盐的是( )
①金属单质 碱性氧化物
③碱 非金属单质
⑤酸性氧化物 酸
A.①②③ B.①④⑥
C.②⑤⑥ D.①②③④⑤⑥
解析:选D。金属单质与酸反应生成对应的盐和氢气;碱性氧化物与酸反应生成盐和水;非金属单质和金属单质化合可得到盐;酸性氧化物或酸与碱反应可生成盐。
考点三 分散系 胶体
1.分散系
(1)概念:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。
(2)分类:根据分散质粒子的直径大小将分散系分为溶液、胶体和浊液,直观表示如下:
[点拨] 胶体区别于其他分散系的本质特征是分散质粒子的直径大小(1~100 nm)。
(3)三种分散系比较
分散系 | 溶液 | 胶体 | 浊液 |
分散质粒子 的直径大小 | <1__nm | 1~100__nm | >100__nm |
外观特征 | 均匀、透明 | 均匀、透明或半透明 | 不均匀、不透明 |
稳定性 | 稳定,静置无沉淀 | 较稳定 | 不稳定,静置有沉淀 |
分散质能否透过滤纸 | 能 | 能 | 不能 |
分散质能否透过半透膜 | 能 | 不能 | 不能 |
分类 | 饱和溶液、不饱和溶液 | 固溶胶、液溶 胶、气溶胶 | 悬浊液、乳浊液 |
实例 | 食盐水、蔗糖溶液 | Fe(OH)3 胶体 | 泥水、油水 |
[点拨] 胶体粒子一般是离子、分子或难溶物的聚集体,1 mol FeCl3水解形成的Fe(OH)3胶粒数目远小于NA,但有些高分子,一个分子就可能形成一个胶体粒子。
2.胶体的性质及应用
(1)丁达尔效应:当可见光束通过胶体时,胶体中的现象为出现一条光亮的“通路”,产生丁达尔效应的原因是胶体粒子对光线有散射作用。可用此性质鉴别溶液和胶体。
(2)介稳性:胶体的稳定性介于溶液与浊液之间,在一定条件下能稳定存在,属于介稳体系,但改变条件就有可能发生聚沉。
(3)聚沉:在一定条件下,胶体粒子聚集成较大的颗粒,形成沉淀从分散剂中析出。此性质常用于制作豆腐、净水等。使胶体聚沉的常用方法有①加入电解质溶液;②加入胶粒带相反电荷的胶体;③加热或搅拌。
(4)电泳:由于胶体粒子带有电荷,在电场作用下,胶体粒子在分散剂中做定向移动的现象。此性质可用于工业上的静电除尘。
3.Fe(OH)3胶体的制备
(1)操作:将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入FeCl3饱和溶液。继续煮沸至液体呈红褐色,停止加热,即可制得Fe(OH)3胶体。
(2)化学方程式:FeCl3+3H2OFe(OH)3(胶体)+3HCl。
题组一 三种分散系的比较
1.下列分散系中的分散质能透过滤纸,但不能透过半透膜的是( )
A.蛋白质溶液 B.FeCl3 溶液
C.生理盐水 D.AgCl悬浊液
解析:选A。蛋白质溶液属于胶体,能透过滤纸,不能透过半透膜,A正确;FeCl3溶液属于溶液,既能透过滤纸又能透过半透膜,B错误;生理盐水属于溶液,既能透过滤纸又能透过半透膜,C错误;AgCl悬浊液属于浊液,既不能透过滤纸,也不能透过半透膜,D错误。
2.下列关于溶液和胶体的叙述正确的是( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
解析:选D。A项,胶体粒子带电荷,而胶体呈电中性。B项,当溶质能电离产生阴、阳离子时,阴、阳离子才会分别向两极移动,当溶质以分子形式存在不发生电离时,即使在电场作用下,溶质分子也不会做定向移动;有的胶体中的分散质粒子不带电,在电场作用下不会做定向移动。C项,溶液中溶质粒子的运动是没有规律的。
题组二 胶体的性质及其应用
3.将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体,此液体不具有的性质是( )
A.光束通过该液体时形成光亮的“通路”
B.插入石墨电极通直流电后,有一极附近液体颜色加深
C.向该液体中加入硝酸银溶液,无沉淀产生
D.将该液体加热、蒸干、灼烧后,有氧化物生成
解析:选C。将饱和FeCl3溶液滴入沸水中,可制得Fe(OH)3胶体,光束通过胶体时会形成光亮的“通路”,即产生丁达尔效应,A项正确;Fe(OH)3胶体粒子吸附正电荷而带正电,通直流电后,在阴极附近液体颜色加深,B项正确;向Fe(OH)3胶体中加入电解质溶液,会发生聚沉现象,C项错误;将Fe(OH)3胶体加热、蒸干、灼烧后,会得到Fe2O3,D项正确。
4.下列解释与胶体性质无关的是( )
A.向饱和氯化铁溶液中逐滴加入烧碱溶液,产生红褐色沉淀
B.豆制品厂用石膏或盐卤点制豆腐
C.水泥厂用先进的静电除尘技术除去空气中的粉尘
D.洪灾发生地的农民用明矾净化河水作为生活用水
解析:选A。A.向氯化铁溶液中逐滴加入NaOH溶液,会发生复分解反应产生红褐色沉淀氢氧化铁,与胶体性质无关;B.用石膏或盐卤点制豆腐,利用的是胶体聚沉形成的凝胶,与胶体性质有关;C.水泥厂用先进的静电除尘技术除去空气中的粉尘,利用的是电泳现象,与胶体性质有关;D.用明矾净化河水,是利用铝离子水解生成的氢氧化铝胶体具有吸附作用,与胶体性质有关。
1.(2020·浙江7月选考)下列物质对应的组成不正确的是( )
A.干冰:CO2
B.熟石灰:CaSO4·2H2O
C.胆矾:CuSO4·5H2O
D.小苏打:NaHCO3
解析:选B。干冰的组成为CO2,A项正确;熟石灰的组成为Ca(OH)2,B项错误;胆矾的组成为CuSO4·5H2O,C项正确;小苏打的组成为NaHCO3,D项正确。
2.(2019·高考海南卷)下列说法正确的是( )
A.MgO和Al2O3都属于两性氧化物
B.悬浊液和乳浊液的分散质均为液态
C.Fe3O4和Pb3O4中的金属都呈现两种价态
D.葡萄糖溶液和淀粉溶液都具有丁达尔效应
解析:选C。MgO是碱性氧化物,A错误;悬浊液的分散质是固体小颗粒,B错误;Fe3O4可表示为FeO·Fe2O3,Fe元素化合价为+2、+3价;Pb3O4可表示为2PbO·PbO2,Pb元素化合价为+2、+4价,因此二者中的金属都呈现两种价态,C正确;葡萄糖分子是小分子,葡萄糖溶液中溶质分子的直径小于1 nm,所以葡萄糖溶液不能产生丁达尔效应,D错误。
3.(2019·浙江4月选考)下列属于置换反应的是( )
A.4NH3+5O24NO+6H2O
B.2Na2SO3+O2===2Na2SO4
C.2Na2O2+2CO2===2Na2CO3+O2
D.2KI+Cl2===2KCl+I2
解析:选D。置换反应指一种单质与一种化合物反应,生成另一种单质和另一种化合物的化学反应。D项中Cl2与KI反应生成I2和KCl,属于置换反应,其余选项均不是,故选D。
4.(2019·高考天津卷)化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是( )
A.利用废弃的秸秆生产生物质燃料乙醇
B.利用石油生产塑料、化纤等高分子材料
C.利用基本的化学原料生产化学合成药物
D.利用反渗透膜从海水中分离出淡水
解析:选D。利用废弃的秸秆生产乙醇的过程中,秸秆中的纤维素水解生成葡萄糖,葡萄糖再转化成乙醇,A项不符合题意;利用石油生产塑料、化纤等高分子材料的过程中,发生加聚反应或缩聚反应,B项不符合题意;利用基本的化学原料生产化学合成药物的过程中,发生了化学反应,C项不符合题意;利用反渗透膜从海水中分离出淡水,属于物理变化,D项符合题意。
1.改革开放以来,化学科学技术的发展大大提高了我国人民的生活质量。下列过程没有涉及化学变化的是( )
A.太阳能分解水制取氢气 | B.从海底开采可燃冰获取燃料 |
C.新能源汽车燃料电池供电 | D.运载“嫦娥五号”的火箭发射 |
解析:选B。水分解产生氢气和氧气,有新物质产生,发生的是化学变化,A不符合题意;从海底开采可燃冰获取燃料,没有新物质产生,发生的是物理变化,B符合题意;新能源汽车燃料电池供电,化学能转化为电能,有新物质产生,发生的是化学变化,C不符合题意;运载“嫦娥五号”的火箭发射,化学能转化为热能、机械能,有新物质产生,发生的是化学变化,D不符合题意。
2.有人设想将碳酸钙通过特殊的加工方法使之变为纳米碳酸钙(碳酸钙粒子直径是几纳米至几十纳米),这将使建筑材料的性能发生巨变。下列关于纳米碳酸钙的推测正确的是( )
A.纳米碳酸钙的水溶液会浑浊不清
B.纳米碳酸钙分散到水中能产生丁达尔效应
C.纳米碳酸钙的化学性质已与原来的碳酸钙完全不同
D.纳米碳酸钙的粒子不能透过滤纸
解析:选B。纳米碳酸钙的水溶液属于胶体,是澄清透明的液体,故A错误;纳米碳酸钙分散到水中形成胶体,能产生丁达尔效应,故B正确;纳米碳酸钙的化学性质与原来的碳酸钙相同,故C错误;胶体粒子能透过滤纸,所以纳米碳酸钙的粒子能透过滤纸,故D错误。
3.(2021·三亚高三模拟)下列说法中正确的是( )
A.Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物
B.碱石灰是NaOH和CaO的混合物,其中CaO属于碱性氧化物
C.FeO、Fe2O3均为碱性氧化物,与氢碘酸反应均只发生复分解反应
D.将Fe(OH)3胶体和泥水分别进行过滤,分散质均不能通过滤纸孔隙
解析:选B。能与酸反应生成盐和水的氧化物是碱性氧化物,Na2O、Na2O2为相同元素组成的金属氧化物,前者属于碱性氧化物,后者不属于碱性氧化物,A错误;碱石灰是NaOH和CaO的混合物,其中CaO属于碱性氧化物,B正确;FeO、Fe2O3均为碱性氧化物,与氢碘酸反应时前者只发生复分解反应,后者发生氧化还原反应,铁离子具有氧化性,碘离子具有还原性,C错误;将Fe(OH)3胶体和泥水分别进行过滤,胶体中分散质能通过滤纸孔隙,泥水中分散质不能通过滤纸孔隙,D错误。
相关学案
这是一份2024年高考化学一轮总复习 第1单元 第1讲 物质的分类及转化 学案(含高考真题和课后作业)(教师版 ),共26页。学案主要包含了物质的组成,物质的分类等内容,欢迎下载使用。
这是一份人教版高考化学一轮复习第1章物质及其变化第1节物质的分类及转化学案含答案
这是一份人教版高考化学一轮总复习第1章第1节物质的分类及转化课时学案,共16页。












