









第11单元 盐 化肥(课件+练习)-2022年中考化学一轮复习讲练测
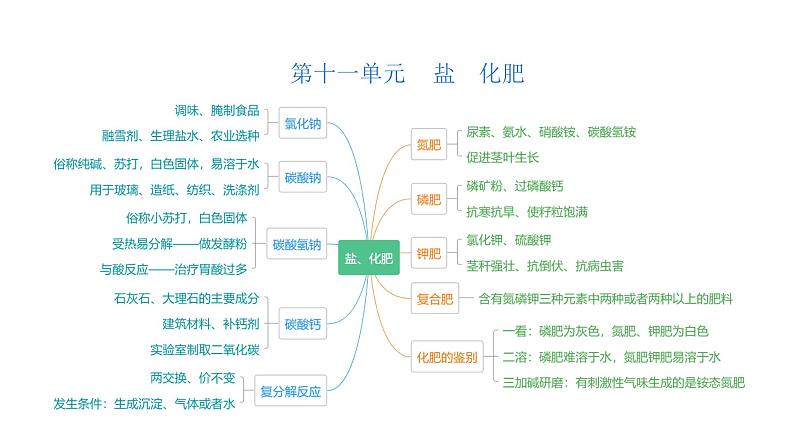
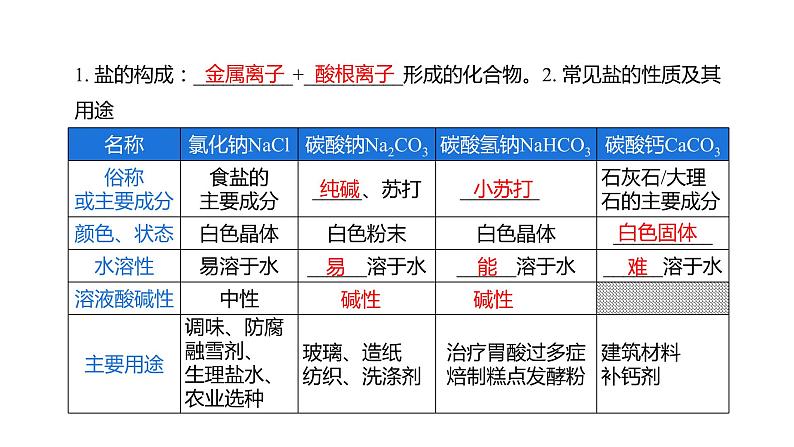
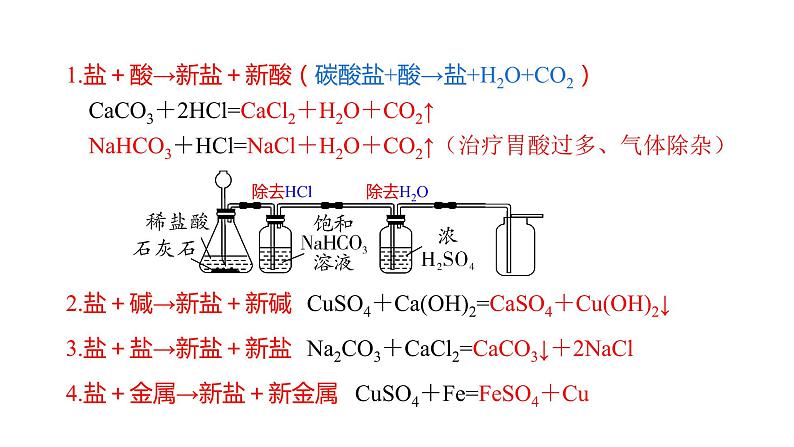
展开第十一单元 盐 化肥
姓名:___________班级:___________考号:___________
1.(2021·黑龙江二模)下列过程中不发生化学变化的是( )
A.钟乳石的形成 B.铁钉生锈 C.氢氧化钠潮解 D.食盐溶于水
【答案】C
【解析】A、溶洞形成过程中,碳酸钙和水、二氧化碳反应生成碳酸氢钙,碳酸氢钙分解生成碳酸钙、水和二氧化碳,属于化学变化,故选项不符合题意;B、铁钉生锈过程中,铁和水、氧气反应生成铁锈,属于化学变化,故选项不符合题意;C、氢氧化钠潮解是因为氢氧化钠吸收了空气中的水蒸气,而在氢氧化钠表面形成溶液的过程,属于物理变化,故选项符合题意;D、制取汽水时,柠檬酸和碳酸氢钠反应生成柠檬酸钠、二氧化碳、水等物质,属于化学变化,故D不符合题意。故选:C。
2.(2021·广西河池)制作包子、蛋糕所用发酵粉的主要成分含有碳酸氢钠。碳酸氢钠的俗称是( )
A.小苏打 B.苏打 C.苛性钠 D.火碱
【答案】A
【解析】碳酸氢钠俗称小苏打,故选A。
3.(2021·山东滨州)“火碱、烧碱、纯碱、苛性钠、小苏打”所代表的物质(或主要成分)共有( )
A.一种 B.二种 C.三种 D.四种
【答案】C
【解析】火碱、烧碱、苛性钠都是氢氧化钠的俗名,纯碱是碳酸钠的俗名,小苏打是碳酸氢钠的俗名。
所以一共有3种物质,故选C。
4.(2021·辽宁鞍山)下列有关盐的用途说法不正确的是( )
A.氯化钠可用于配制生理盐水 B.碳酸钙可用作补钙剂
C.亚硝酸钠可用于腌制蔬菜 D.小苏打可用于焙制糕点
【答案】C
【解析】A、生理盐水是0.9%的氯化钠溶液,所以氯化钠可用于配制生理盐水,故选项正确;B、碳酸钙能与胃液中的盐酸反应生成可被人体吸收的氯化钙,所以碳酸钙可用作补钙剂,故选项正确;C、亚硝酸钠有毒,会危害人体健康,所以不能用亚硝酸钠腌制蔬菜,故选项错误;D、小苏打受热时会分解产生二氧化碳气体,所以小苏打可用于焙制糕点,故选项正确。故选C
5.(2021·江苏南通)下列有关物质的性质与用途具有对应关系的是( )
A.氮气不易溶于水,可用作保护气
B.碳酸钙能与盐酸反应,可用作补钙剂
C.一氧化碳具有可燃性,可用于工业炼铁
D.氢氧化钙为白色固体,可用于改良酸性土壤
【答案】B
【解析】A、氮气化学性质稳定,可用作保护气,错误。
B、碳酸钙含有钙元素,能与胃液中盐酸反应生成氯化钙,被人体吸收,可用作补钙剂。正确。
C、一氧化碳具有还原性,可用于工业炼铁,错误。
D、氢氧化钙呈碱性,可用于改良酸性土壤,错误。故选B。
6.(2020·怀化)下图是某实验小组做粗盐提纯实验的部分操作示意图。下列有关实验叙述错误的是( )
A.④中缺少玻璃棒引流溶液
B.①中玻璃棒的作用是搅拌,加速粗盐溶解
C.上述操作顺序为③①②④
D.当②蒸发皿中出现较多固体时,停止加热
【答案】C
【解析】A、由图可知,④是过滤,过滤应遵循“一贴、二低、三靠”的原则,④中缺少玻璃棒引流溶液,不符合题意;B、①中玻璃棒的作用是搅拌,加速粗盐溶解,说法正确,不符合题意;C、粗盐提纯的步骤:称量、溶解、过滤、蒸发,故操作顺序为③0④②,符合题意;D、当②蒸发皿中出现较多固体时,停止加热,利用余热使滤液蒸干,不符合题意。故选C。
7.下列化肥中属于复合肥料的是( )
A.NH4HCO3 B.KCl C.CO(NH2)2 D.NH4H2PO4
【答案】D
【解析】A、碳酸氢铵中含有氮、磷、钾三种元素中的氮元素,属于氨肥,故A选项不符合题意;B、氯钾中含有氮、磷、钾三种元素中的钾元素,属于钾肥,故B选项不符合题意;C、尿素中含有氮、磷、钾三种元素中的氮元素,属于氮肥,故C选项不符合题意;D、磷酸二氢铵中含有氮、磷、钾三种元素中的磷、钾两种,属于复合肥,故D选项符合题意;故答案选D。
8.(2020·柳州)硝酸铵是一种氨肥,易溶于水,受热易分解,遇碱时放出氨气,在高温或受猛烈撞击时易爆炸,下列使用硝酸铵的做法不正确的是( )
A.储存和运输时密封防潮 B.结块时用铁锤砸碎再用
C.施用时不宜与碱混和使用 D.给农作物施肥后及时盖土
【答案】B
【解析】A、因为硝酸铵易溶于水,易潮解而结块,受热易分解,所以储存和运输时密封防潮,不符合题意;B、因为硝酸铵在猛烈撞击时易爆炸,所以结块时不能用铁锤砸碎,符合题意;C、硝酸铵是一种铵态氮肥,与显碱性的物质混合时能反应生成氨气,从而降低肥效,所以不能与碱混合使用,不符合题意;D、因为硝酸铵易溶于水,受热易分解,所以给农作物施肥后及时盖土不能露天施肥,不符合题意。故选B。
9.(2021·辽宁锦州)下列各组物质在水中能大量共存,并形成无色溶液的是( )
A.CuSO4、KCl、H2SO4 B.NaCl、HNO3、AgNO3
C.HC1、Ca(OH)2、NaC1 D.HC1、NaNO3、Na2SO4
【答案】D
【解析】A、硫酸铜、氯化钾、硫酸三种溶液不反应,但是硫酸铜溶液是蓝色的,不符合题意;B、氯化钠能与硝酸银反应生成氯化银白色沉淀,不能共存,不符合题意;C、盐酸和氢氧化钙反应生成氯化钙和水,不能共存,不符合题意;D、盐酸、硝酸钠、硫酸钠不能形成沉淀、气体和水,可以大量共存,且是无色溶液,符合题意。故选D。
10.(2021·甘肃兰州)下列物质之间的转化不能通过化学反应一步实现的是( )
A.H2O→Ca(OH)2 B.KNO3→K2SO4
C.CO2→CO D.Na2CO3→NaOH
【答案】B
【解析】A、水与氧化钙反应生成氢氧化钙,能通过一步反应实现;B、硝酸钾不能与其他物质反应,生成硫酸钾,不能通过一步反应实现;C、二氧化碳与碳在高温下反应生成一氧化碳,能通过一步反应实现;D、碳酸钠与氢氧化钙反应生成氢氧化钠,能通过一步反应实现。故选:B。
11.类推是学习中常用的思维方法.现有以下类推结果:①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应:②氯化钠的水溶液显中性,所以盐溶液一定显中性;③单质只含有一种元素,所以含一种元素的物质一定属于单质;④有机物都含碳元素,但是含碳元素的化合物不一定都是有机物;⑤燃烧一般伴有发光发热现象,所以发光发热的变化就是燃烧;⑥碳酸盐与盐酸反应放出气体,但是与盐酸反应放出气体的物质不一定是碳酸盐.其中错误的是( )
A.③④ B.④⑥ C.①②③④ D.①②③⑤
【答案】D
【解析】①生成盐和水的反应不一定是中和反应。例如,石灰水和二氧化碳反应生成碳酸钙(盐)和水,此不是中和反应,此项说法错误;②盐溶液不一定显中性,例如,碳酸钠是盐,但其水溶液显碱性,此项说法错误;③含一种元素的物质不一定属于单质,可能为混合物,如氧气和臭氧的混合物中只含有氧元素,而非单质,此项说法错误;④含有碳元素的化合物不一定是有机物。例如,碳酸钙中含有碳元素,它是无机物,此项说法正确;⑤有发光、放热现象的变化不一定是燃烧,例如电灯通电时发光、放热,但是不属于燃烧,此项说法错误;⑥与盐酸反应放出气体的物质不一定是碳酸盐,例如锌和盐酸反应能生成氢气和氯化锌,此项说法正确;故选D。
12.(2021·甘肃兰州)下列实验操作不能达到实验目的的是( )
【答案】A
【解析】A、除去NaNO3溶液中的KCl,加入适量AgNO3溶液,KCl与AgNO3反应生成氯化银沉淀和硝酸钾,引入新杂质,符合题意;B、除去CO2中混有的少量HCl气体,依次通入装有足量饱和NaHCO3溶液和浓硫酸的洗气瓶,HCl气体溶于水形成盐酸,盐酸与NaHCO3反应生成氯化钠、二氧化碳和水,浓硫酸可以吸收水,不符合题意;C、鉴别真假黄金,灼烧,假黄金变黑(假黄金的成分是黄铜:铜和锌,铜和氧气反应产生黑色的氧化铜),真黄金不变,不符合题意;D、检验0,中是否混有CO2,通入澄清石灰水,如果变浑浊,说明含有CO2,不符合题意。故选A。
13.(2020·重庆)某同学将一定量的Na2CO3与Ba(OH)2溶液混合,要想检验反应后Ba(OH)2是否过量,应选用的试剂是( )
A.酚酞 B.CuCl2溶液 C.Na2CO3溶液 D.NaCl溶液
【答案】C
【解析】A、Na2CO3、Ba(OH)2与生成的氢氧化钠均能使酚酞溶液变红,不能用酚酞溶液检验反应后Ba(OH)2,是否过量,A不正确;B、Ba(OH)2与生成的氢氧化钠均能和CuCl2,溶液反应生成氢氧化铜蓝色沉淀,不能用氯化铜溶液检验反应后Ba(OH)2是否过量,B不正确;C、滴加Na2CO3溶液,若生成白色沉淀,则说明溶液中含有钡离子,碳酸钠溶液可以检验反应后Ba(OH)2是否过量,选项C正D、无论Ba(OH)2是否过量,加入NaCl溶液均无明显现象,氯化钠溶液不能检验反应后Ba(OH)2是否过量,选项D不正确。故选C。
14.(2020·濮阳二模)现有一定质量的CuO、Cu(OH)2的固体混合物,加入100g9.8%的稀硫酸恰好完全反应,则反应后所得溶液中溶质的质量为( )
A.19.6g B.16g C.9.8g D.9.6g
【答案】B
【解析】硫酸中溶质的质量为100g×9.8%=9.8g,其中硫酸根的质量为器9.8g×=9.6g氧化铜、氢氧化铜和硫酸恰好反应,生成的溶质只有硫酸铜;硫酸铜的质量=9.6g÷=16g,因此反应后所得溶液中溶质的质量为16g故选B
15.我国北方有许多盐碱湖,湖水中溶有大量的食盐(NaC1)和纯碱(Na2CO3),那里的农民冬天捞碱,夏天晒盐,你知道为什么吗?
【答案】碳酸钠的溶解度受温度影响很大,冬季温度低,碳酸钠结晶析出;食盐的溶解度受温度影响很小,夏季温度高水分蒸发快食盐结晶析出
【解析】由于纯碱的溶解度随温度的降低而减小,且受温度的影响较大,而氯化钠的溶解度受温度很小,冬天捞碱是因纯碱的溶解度随温度的降低而减小,且受温度的影响较大;夏天晒盐是因氯化钠的溶解度受温度很小,且夏季温度高水分蒸发快食盐结晶析出。
16.为了除去KC1中含有的K2SO4、CaCl2、MgC12三种杂质,小明设计如下操作步骤:①加水溶解后,依次加入过量的BaCl2溶液、过量的Na2CO3溶液,过量的Ca(OH)2溶液;②过滤;③向滤液中加入适量稀盐酸;④蒸发滤液得到氯化钾固体。
(1)指出步骤中所加的试剂顺序的不足之处。
(2)改正步骤中所加试剂的顺序后,整个提纯过程中共发生多少个有沉淀生成的复分解反应?
(3)在蒸发过程中,玻璃棒的作用是什么?
【答案】(1)应最后加入过量的K2CO3溶液 (2)5
(3)搅拌,防止因局部温度过高,造成液滴飞溅
【解析】(1)镁离子用氢氧根离子沉淀,加入过量的氢氧化钙溶液可以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钾溶液转化为沉淀,但是加入碳酸钾溶液要放在加入的氯化钡溶液之后,这样碳酸钾会除去反应剩余的氯化钡;步骤①中所加的试剂顺序的不足之处是:氢氧化钙不能放在碳酸钾之后,否则过量的氢氧化钙无法除去,即:应最后加入过量的K2CO3溶液。
(2)改正步骤①中所加试剂的顺序后,整个提纯过程中共发生了有沉淀生成的复分解反应:1.氯化钡溶液与硫酸钾溶液(硫酸钡沉淀);2.氢氧化钙溶液与氯化镁溶液(氢氧化镁沉淀);3.过量碳酸钾与氯化钙(碳酸钙沉淀);4.过量碳酸钾与氯化钡(碳酸钡有沉淀);5.过量碳酸钾与氢氧化钙溶溶液(碳酸钙沉淀)。所以,一共有5个沉淀生成的复分解反应。
(3)蒸发过程中,玻璃棒的作用是搅拌,以防止局部温度过高,造成液体飞溅。
17.(2021·西藏)北京冬奥会将于2022年举行。如图所示,“五环”中相交两环中的物质间能够发生化学反应,其中A、B、C、D分别是NaOH、Fe、CuO、CuCl2中的一种,C溶液能使紫色石蕊溶液变蓝。
(1)C的化学式是 ;
(2)写出B与C反应的化学方程式: ;A与B的反应属于 (填基本反应类型)。
【答案】(1)NaOH
(2)CuCl2+2NaOH=Cu(OH)2↓+2NaCl 置换反应
【解析】根据“五环”中相交两环中的物质间能够发生化学反应,A、B、C、D分别是NaOH、Fe、CuO、CuCl2中的一种,C溶液能使紫色石蕊溶液变蓝,所以C是氢氧化钠,氢氧化钠会与氯化铜反应,所以B是氯化铜,氯化铜会与铁反应,所以A是铁,D是氧化铜。
(1)由分析可知,C的化学式是NaOH;
(2)B与C的反应是氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,化学方程式为:CuCl2+2NaOH=Cu(OH)2↓+2NaCl;A与B的反应是铁和氯化铜反应生成氯化亚铁和铜,是单质和化合物生成单质和化合物的反应,属于置换反应。
18.有一包白色固体混合物,可能由CuSO4、Na2CO3、Na2SO4、BaCl2中的一种或几种组成,为确定其组成,兴趣小组的同学进行了下列实验:
(1)取少量固体溶于足量的水,过滤得到白色固体A和无色滤液B,则原固体中一定不含有 。
(2)向白色固体A中加入足量的稀盐酸,固体全部溶解,且有气泡生成,则原固体中一定有 ;一定不含有 。
【答案】(1)CuSO4 (2)Na2CO3、BaCl2 Na2SO4
【解析】(1)硫酸铜溶液蓝色,取少量固体溶于足量的水,过滤得到白色固体A和无色滤液B,则原固体中一定不含有硫酸铜,碳酸钠和硫酸钠都可以和氯化钡生成沉淀,一定含氯化钡,碳酸钠和硫酸钠至少含有一种,故填:CuSO4。(2)向白色固体A中加入足量的稀盐酸,固体全部溶解,且有气泡生成,沉淀是碳酸钠和氯化钡生成的碳酸钡沉淀,一定不含硫酸钡沉淀,则原固体中一定含碳酸钠和氯化钡,一定不含硫酸钠,故填:Na2CO3、BaCl2;Na2SO4。
19.海水中含有氯化钠、氯化钙等物质,下面是从海水中提取氯化钠的大致过程以及氯化钠和氯化钙的溶解度表。请按要求回答问题:
(1)海水属于 。(填物质类别)
(2)10℃时,氯化钠的溶解度是 ,20℃时,氯化钠饱和溶液中溶质质量分数 (填“大于”等于”小于”)氯化钙饱和溶液中溶质质量分数。
(3)粗盐经过溶解、过滤、,可除去沙制得精盐,用饱和氯化钠溶液浸洗精盐,可除去其中的少量氯化钙,其原因是 。
(4)下列说法正确的是( )
A.海水进入贮水池,海水的成分基本不变
B.蒸发池中,溶质质量逐渐增加
C.结晶池中,溶质质量分数逐渐变大
D.析出晶体后的母液是氯化钠的饱和溶液
【答案】(1)混合物(2)35.8g 小于
(3)蒸发结晶饱和氯化钠溶液不能再溶解精盐中的氯化钠,但能继续溶解氯化钙等杂质
(4)AD
【解析】(1)海水中含有水、氯化钠、氯化钙等物质属于混合物;
(2)10℃时,氯化钠的溶解度是35.8g;对于饱和溶液,溶质质量分数=×100%,所以对于饱和溶液,溶解度越大,溶质质量分数越大。20℃时,氯化钙的溶解度大于氯化钠的溶解度,所以氯化钠饱和溶液中溶质的质量分数小于氯化钙的饱和溶液中溶质的质量分数;
(3)氯化钠在水中的溶解度随温度的变化影响不大,故可用蒸发结晶来提纯,粗盐经过溶解、过滤、蒸发结晶,可除去泥沙制得精盐;用饱和氯化钠溶液浸洗精盐,是因为饱和氯化钠溶液不能再溶解精盐中的氯化钠,但能继续溶解氯化钙等杂质,再过滤、干燥,能除去少量氯化钙等杂质,也防止氯化钠溶解。
A、海水进入贮水池,海水的成分基本不变,故选项正确;B、在蒸发池中,溶剂水的质量在不断减少,海水中溶质的质量不变,故选项错误;C、在结晶池中,在温度不变时,一直是氯化钠的饱和溶液,即氯化钠质量分数不变,故选项错误;D、析出晶体后的母液是氯化钠的饱和溶液,故选项正确。故选AD。
20.(2021·天津)现有一定质量的碳酸钠和氯化钠的固体混合物,其中含氯元素7.1g。向该混合物中加入138.1g一定溶质质量分数的稀盐酸,恰好完全反应,得到氯化钠溶液并生成4.4g气体。计算:
(1)原固体混合物中氯化钠的质量;
(2)反应后所得溶液中溶质的质量分数。
【答案】(1)11.7g
解:由题干信息可知,原固体混合物中氧化钠的质量为7.1g÷(×100%)=11.7g;
答:原固体混合物中氯化钠的质量为11.7g。
(2)15%
解:设参加反应的碳酸钠质量为x,生成氯化钠的质量为y
Na₂CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
x=10.6g
y=11.7g
反应后所得溶液中溶质的质量分数为==15%
答:反应后所得溶液中溶质的质量分数为15%。
第11单元 盐和化肥(课件)2025年中考化学一轮复习讲练测: 这是一份第11单元 盐和化肥(课件)2025年中考化学一轮复习讲练测,共60页。PPT课件主要包含了考点一几种常见的盐,考点二粗盐的提纯,考点三盐的化学性质,考点四复分解反应,考点五化学肥料等内容,欢迎下载使用。
最新中考化学一轮复习讲练测课件+综合检测(人教版) 第11单元 盐和化肥(课件): 这是一份最新中考化学一轮复习讲练测课件+综合检测(人教版) 第11单元 盐和化肥(课件),文件包含2023年中考化学一轮复习讲练测人教版第11单元盐和化肥课件pptx、第十一单元盐化肥-2023年中考化学一轮复习讲练测人教版原卷版docx、第十一单元盐化肥-2023年中考化学一轮复习讲练测人教版解析版docx等3份课件配套教学资源,其中PPT共60页, 欢迎下载使用。
专题08+盐 化肥(课件)-2024年中考化学一轮复习讲义+测试+练习+课件(全国通用): 这是一份专题08+盐 化肥(课件)-2024年中考化学一轮复习讲义+测试+练习+课件(全国通用),共47页。












